BAB II TINJAUAN PUSTAKA 2. 1 Anatomi Ginjal
Transcript of BAB II TINJAUAN PUSTAKA 2. 1 Anatomi Ginjal

5
BAB II
TINJAUAN PUSTAKA
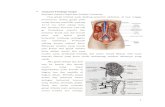
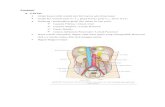
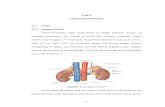
2. 1 Anatomi Ginjal
Permukaan ginjal ditutupi oleh organ capsula fibrosa. Ginjal terdiri atas 2
bagian yaitu satu buah disisi kanan dan satu buah disisi kiri. Bentuk ginjal seperti
biji kacang yang terletak dibagian belakang peritoneum. Kedua ginjal terletak di
belakang peritoneum, yang mana sisi kanan terletak pada dinding posterior
abdomen dan sisi kiri terletak pada columna vertebralis. Kedua ginjal memiliki
warna coklat kemerahan. Letak ginjal kanan sedikit lebih rendah dari ginjal kiri,
karena diatas ginjal kanan terdapat tempat lobus hepatis yang besar (wiliam &
wilkins, 2015).
Gambar 2.1. Anatomi ginjal (Guyton & Hall, 2016).
Pada umumnya ginjal orang dewasa memiliki ukuran sekitar 12 cm, lebar 6
cm dan tebal 3 cm serta berat rata-rata ginjal yaitu 150 g. Permukaan bagian luar
ginjal cembung sedangkan permukaan bagian dalam cekung dan mempunyai
celah vertikal yang disebut hilus ginjal. Pada bagian superior masing-masing
ginjal terdapat kelenjar adrenal atau suprarenal serta terdapat beberapa jaringan
pendukung yang mengelilingi ginjal (Marieb & Brito, 2018). Masing-masing
ginjal memiliki daerah lekukan yang disebut Hilum dan terletak di sisi medial
ginjal (Guyton & Hall, 2016). Hilum renal merupakan celah untuk lewatnya
pembuluh darah dan ureter yang masuk ataupun keluar ginjal. Sedangkan Sinus
renalis merupakan suatu akses ke rongga internal (Paulsen & Waschke, 2018).

6
Ginjal dilindungi oleh capsula fibrosa yang berfungsi untuk melindungi struktur
dalam ginjal yang halus. Ginjal dibagi menjadi dua bagian yaitu cortex dan
medula. Medula terdiri dari 8-10 jaringan berbentuk kerucut yang disebut
piramida ginjal. Piramida ginjal diawali dari perbatasan antara cortex dan medula
dan berakhir di papila, yang berbentuk corong dari ujung atas ureter (Guyton &
Hall, 2016).
2. 2 Fungsi Ginjal
Ginjal berfungsi untuk mensekresikan sebagian besar sisa metabolisme.
Peran penting dari ginjal yaitu mengatur keseimbangan air dan elektrolit di dalam
tubuh serta mempertahankan keseimbangan asam-basa darah (William &
Wilkins,2015). Aliran darah yang mengalir ke ginjal sekitar 22% atau sekitar
1100 ml/menit. Pembentukan urin diawali dengan arteri renal yang masuk ke
ginjal melalui hilum yang kemudian bercabang sehingga terbentuk arteri
interlobaris, arteri arkuata, arteri interlobularis (arteri radial), dan arteri arteriol
aferen yang mengarah ke glomerulus. Terbentuknya arteriol aferen yaitu dengan
menyatunya kapiler-kapiler glomerulus yang membawa darah menuju jaringan
kapiler pertibular. Sirkulasi ginjal memiliki dua lapisan kapiler, kapiler
glomerulus dan kapiler pertibular yang letaknya berada diantara arteriol aferen,
yang mana arteriol aferen ini berfungsi untuk mengatur tekanan hidrostatik pada
dua kapiler tersebut. Kapiler glomerulus memiliki tekanan hidrostatik yang tinggi
sekitar 60 mmHg, sehingga dapat mengakibatkan filtrasi cairan yang cepat,
sedangkan kapiler pertibular memiliki tekanan hidrostatik yang lebih rendah dari
kapiler glomerulus yaitu sekitar 13 mmHg sehingga mengakitkan terjadi
kecepatan reabsobsi cairan yang cepat (Guyton & Hall, 2016).

7
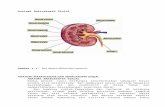
Gambar 2.2 Anatomi nefron ginjal (Himmelfarb & Ikizler, 2018).
Setiap ginjal manusia mengandung sekitar 800 ribu sampai 1 juta nefron,
yang memiliki masing-masing fungsi yaitu mampu membentuk urin. Jumlah
nefron dapat berkurang secara bertahap karena ginjal yang tidak dapat
meregenarsi nefron baru, sehingga menyebabkan cedera ginjal, penyakit dan
penuaan normal. Setiap nefron terdiri atas dua bagian yaitu korpus ginjal (badan
malphigi) dan tubulus renalis. Korpus ginjal terdiri dari glomerulus yang
dikelilingi oleh capsula Bowman sedangkan Tubulus Renalis terdiri atas Tubulus
Kontortus Proksimal, Lengkung Henle Dan Tubulus Kontortus Distal (Guyton &
Hall, 2016).
Glomerulus merupakan jaringan kapiler yang terbentuk dari arteriol afferen
dan arteriol eferen. Arteriol afferen dapat membantu mempertahankan tekanan
darah yang tinggi di dalam glomerulus karena memiliki diameter yang lebih besar
dari diameter arteriol efferen. Capsula Bowman ialah ujung perluasan tubulus
renalis yang menutupi glomerulus. Capsula Bowman terdiri dua lapisan yaitu
lapisan dalam lapisan luar. Lapisan dalam dari capsula bowman memiliki pori dan
sangat permeable, sedangkan lapisan luar capsula bowman tidak berpori dan tidak
permeable. Celah antara dua lapisan tersebut berisi filtrat ginjal, cairan yang
berasal dari darah dalam glomerulus, dan selanjutnya diubah menjadi urin
(Scanlon & Sanders, 2015).

8
2.2.1 Pembentukan Urin
Pembentukan urine melalui tiga proses utama. Proses pertama yaitu filtrasi
glomerulus yang terjadi di korpus ginjal, proses kedua dan ketiga ialah reabsorbsi
tubulus dan sekresi yang terjadi di tubulus renalis (Scanlon & Sanders, 2015).
2.2.1.1 Filtrasi Glomerulus
Filtrasi glomerulus merupakan langkah awal pembentukan urin yang mana
proses ini ialah keluarnya zat-zat terlarut dari kapiler yang disebabkan oleh
tekanan darah mendorong plasma, serta protein kecil keluar dari glomeruli dan
masuk ke kapsula bowman. Lapisan dalam kapsula bowman memiliki tekanan
yang sangat rendah yaitu sekitar 20 % - 25 % darah yang keluar dari glomeruli
dan masuk ke kapsula bowman sehingga menjadi filtrat ginjal di dalam kapsula
bowman.
Sel-sel darah dan protein yang berukuran besar tidak dapat keluar dari
glomeruli, sehingga tetap berada dalam plasma darah. Namun, zat-zat sisa serta
bahan bermanfaat seperti nutrien dan mineral dapat larut dalam plasma sehingga
dapat masuk ke filtrat ginjal. Perbedaan antara plasma darah dan filtrat ginjal
yaitu filtrat ginjal memiliki protein lebih sedikit dan tidak memiliki sel darah
didalamnya.
Laju filtrasi glomerulus (GFR) merupakan jumlah filtrat ginjal yang
dihasilkan dalam 1 menit. GFR dapat menghasilkan filtrat rata-rata 100-125
mL/menit. Jika aliran darah melalui ginjal berubah maka, laju filtrasi glomerulus
pun akan berubah, dimana ketika aliran darah meningkat maka GFR pun kan
meningkat serta menghasilkan filtrat yang lebih banyak. Namun, jika aliran
darah menurun maka hasil GFR pula akan menurun, sehingga mengahasilkan
filtrat yang sedikit serta output urin berkurang (Scanlon & Sanders, 2015).
2.2.1.2 Reabsorpsi tubulus
Ginjal membentuk filtrat dalam waktu 24 jam sebanyak 150 sampai 180
Liter dan mengeluarkan urin normal sebanyak 1 sampai 2 Liter. Pada proses ini
terjadi penyerapan kembali glukosa, asam amino, vitamin dan ion-ion positif.
Proses reabsorpsi berlangsung dengan transport aktif di tubulus kontortus
proksimal, sedangkan ion-ion negatif direabsorpsi dengan transport pasif di
tubulus kontortus distal. Oleh karena itu, sebagian besar filtrat tidak menjadi

9
urin, di mana sekitar 99% filtrat direabsorpsi kembali ke dalam plasma darah
dan hanya 1 % filtrat yang masuk ke pelvis ginjal dan dikeluarkan menjadi urin
(Scanlon & Sanders, 2015).
2.2.1.3 Sekresi tubulus
Hasil metabolik obat serta zat-zat sisa seperti amonia dan kreatinin
disekresikan ke dalam filtrat dan dikeluarkan menjadi urin. Pad proses ini, zat-
zat sisa disekresikan dari darah di kapiler peritubuler menuju ke filtrat di tubulus
renalis (Scanlon & Sanders, 2015)
2.2.2 Eksresi Hasil Metabolik, Bahan Kimia Asing, Obat-Obatan Dan Metabolit
Hormon
Ginjal merupakan alat utama untuk menghilangkan sisa-sisa metabolisme
dalam tubuh. Zat sisa metabolisme yng dihilangkan berupa urea, kreatinin,
asam urat, bilirubin, dan metabolit dari berbagai hormon. Ginjal juga dpat
menghilangkan sebaian besar racun dan zat asing yang dicerna oleh tubuh
seperti obat-obatan, pestisida dan zat tambahan makanan. (Guyton & Hall,
2016).
2.2.3 Mengatur keseimbangan cairan dan elektrolit
Eksresi cairan dan elektrolit didalam tubuh tetap dipertahankan sesuai
dengan asupan untuk menjaga homeostasis. Jika asupan di dalam tubuh lebih
banyak dari eksresi maka jumlah zat dalam tubuh juga meningkat, begitupun
jika asupan di dalam tubuh kurang dari eksresi maka jumlah zat dalam tubuh
juga berkurang. Asupan air dan elektrolit diatur oleh kebiasan makan dan
minum seseorang, sehingga tingkat eksresi ginjal menyesuaikan dengan asupan
dari berbagai zat yang masuk ke dalam tubuh. Respon ginjal terhadap
peningkatan asupan natrium terjadi 10 kali lipat dari 30 mEq/hari menjadi 300
mEq/ hari. Dalam waktu 2 sampai 3 hari setelah peningkatan asupan natrium,
eksresi ginjal mengalami peningkatan sekitar 300 mEq/hari sehingga asupan
dan keluaran cepat terbentuk kembali (Guyton & Hall, 2016).
2.2.4 Mengatur keseimbangan asam basa
Ginjal juga berperan dalam menjaga pH darah dan cairan tubuh tetap pada
batas normal. Nilai pH darah yaitu kisaran 7,35-7,45. Suatu keadaan dikatakan
asidosis ialah ketika pH darah < 7,35 dan sebaliknya jika pH darah > 7,45

10
maka dikatakan alkalosis (Sherwood,2014). Keseimbangan asam basa juga
mengatur konsentrasi ion H yang berada dalam cairan tubuh. Ion H+ dapat
disekresi ginjal lebih banyak ke dalam filtrat ginjal dan dapat mengembalikan
ion HCO3- ke dalam darah, hal ini terjadi apabila cairan dalam tubuh menjadi
terlalu asam, sehingga proses tersebut dapat membantu meningkatkan pH darah
menjadi normal. Jika cairan tubuh menjadi terlalu basa maka, ginjal akan
mengembalikan ion H+ ke dalam darah dan mengeluarkan ion HCO3- dalam
bentuk urin. Sehingga dapat membantu menurunkan pH darah menjadi normal
kembali (Scanlon & Sanders, 2015).
2.2.5 Mengatur Produksi Eritrosit
Hipoksia merupakan salah satu stimulus penting untuk mensekresi
eritropoetin oleh ginjal. Ginjal dapat mengeluarkan eritropoetin yang dapat
merangsang sel darah merah oleh sel induk hematopoietik di sumsum tulang.
Jika produksi eritropoetin menurun akan menyebabkan anemia yang parah
(Guyton & Hall, 2016).
2.2.6 Sekresi renin
Renin-angiotensin merupakan mekanisme dari renin untuk meningkatkan
tekanan darah. Hasil akhir dari mekanisme ini yaitu Angiotensin II yang
menyebabkan vasokonstriksi serta meningkatkan sekresi aldosteron, sehingga
keduanya dapat membantu meningkatkan tekanan darah. Jika tekanan darah
menurun, enzim renin akan disekresi oleh sel-sel jukstaglomerulus di dinding
arteriol afferen (Scanlon & Sanders, 2015).
2. 3 Tinjauan tentang Chronic Kidney Disease (CKD)
2.3.1 Definisi CKD
Chronic Kidney Disease ialah kerusakan struktur ataupun fungsi ginjal
serta penurunan laju glomerulus atau Glomerular Filtration Rate (GFR) yang
berlangsung selama 3 bulan atau lebih. Chronic kidney disease disebabkan oleh
adanya albuminuria, sedimen urin abnormal seperti hematuria, gangguan
fungsional seperti asidosis, kelainan patologis ginjal seperti imunoglobulin
nefropati, serta kelainan struktural ginjal seperti penyakit ginjal polikistik
(Himmelfarb & Ikizler, 2018). Chronic kidney disease merupakan penyakit
yang merusak ginjal secara progresif dan lambat sehingga menyebabkan
gangguan keseimbangan tubuh dan elektrolit (Widyastuti et al., 2014).

11
Chronic kidney disease juga didefinisikan sebagai penurunan fungsi dan
jumlah nefron secara bertahap. Gejala klinis dapat terjadi jika jumlah nefron
turun sekitar 70 sampai 75% di bawah batas normal. Hal ini pula ditandai
dengan konsentrasi darah pada sebagian elektrolit dan pada volume cairan
tubuh dapat bertahan normal sampai jumlah nefron yang berfungsi turun
menjadi 20 sampai 25 persen dari batas normal (Guyton & Hall, 2016).
Berdasarkan Kidney Disease Outcomes Quality Initiative (KDOQI) 2012
bahwa laju filtrasi glomerulus <60 mL/ menit/ 1.73 m2 merupakan definisi
adanya gagal ginjal kronis. Angka tersebut dapat menimbulkan CKD dan
meningkatkan resiko komplikasi pada penyakit tersebut (Himmelfarb &
Ikizler, 2018). Jika laju filtrasi glomerulus <15 mL/menit/ 1,73 m2 maka
disebut penyakit ginjal stadium akhir atau gagal ginjal kronik stadium 5
(Dipiro et al, 2015). Pasien pada stadium akhir terapi yang diberikan yaitu
terapi pengganti ginjal berupa perotoneal dialisis, transplantasi ginjal atau
Hemodialisis. Hemodialisis merupakan terapi yang sangat dianjurkan untuk
pasien yang telah terdiagnosis gagal ginjal stadium ke-5 atau stadium akhir
(Suwitra, 2014).
2.3.2 Epidemiologi CKD
Penyakit gagal ginjal kronik menjadi salah satu penyakit yang dialami
masyarakat dengan prevalensi yang tinggi. Di negara maju prevalensi penyakit
gagal ginjal kronik mencapai 10-13%. Menurut studi Perhimpunan Nefrologi
Indonesia bahwa sekitar 12,5% populasi di Indonesia mengalami penurunan
fungsi ginjal (chris et al., 2014). Prevalensi CKD meningkat seiring dengan
bertambahnya penduduk serta bertambahnya pasien hipertensi dan diabetes
mellitus (Depkes, 2017).
Berdasarkan Indonesian Renal Registry (IRR) 2018 tercatat bahwa data 10
periode pasien aktif dan pasien baru yang menjalani hemodialisis sebagai
berikut :

12
Diagram 1. Pasien baru dan pasien aktif HD kronik di Indonesia tahun
2007-2018.
Diagram diatas terlihat pada tahun 2018 jumlah pasien aktif dan pasien
baru yang menjalani hemodialisis terjadi peningkatan yang pesat. Jumlah
pasien baru pada tahun 2018 meningkat dua kali lipat dari tahun 2017,
begitupun dengan jumlah pasien aktif yang meningkat pesat dibanding tahun-
tahun sebelumnya (Indonesian Renal Registry,2018).
Menurut United States Renal Data System (USRDS) pasien CKD stadium
5 meningkat 5% sampai 10% setiap tahunnya. Empat penyebab umum
terjadinya CKD stadium 5 menurut USRDS adalah diabetes mellitus,
hipertensi, glomerulonefritis, dan penyakit ginjal polikistik. Hal ini dibuktikan
dengan angka kejadian tiap penyakitnya, diabetes mellitus sebanyak 150
kasus/juta, hipertensi sebanyak 80 kasus/juta, glomerulonefritis sebanyak 22
kasus/juta, dan penyakit ginjal polikistik sebanyak 5 kasus/juta. Risiko CKD
lebih tinggi terjadi pada individu yang berusia diatas 65 tahun dan memiliki ras
kulit hitam (Dipiro et al., 2017). Penyebab kematian terbanyak pasien
hemodialisis yaitu dengan penyakit kardiovaskuler sebanyak 42% dan
penyebab kematian pasien tidak diketahui sebanyak 31%, hal tersebut
dikarenakan pasien meninggal diluar rumah sakit (Indonesian Renal Registry,
2018).
2.3.3 Etiologi CKD
Penyakit gagal ginjal kronik juga disebabkan oleh beberapa faktor yaitu
usia lanjut, hipertensi, diabetes mellitus, penyakit kardiovaskular, serta indeks
massa tubuh yang lebih tinggi (>30 kg/m2) (United States Renal Disease

13
System,2018). Penelitian sebelumnya juga menunjukkan bahwa resiko gagal
ginjal kronik umumnya dialami oleh penderita hipertensi, diabetes mellitus
serta wanita yang berusia diatas 60 tahun. Berdasarkan National Health And
Nutrition Examination Survey 2016, nilai GFR <60 ml/ menit/ 1,73 m2 dan
nilai ACR >30 mg/g menunjukkan adanya tanda-tanda gagal ginjal kronik.
CKD disebabkan oleh beberapa faktor yaitu susceptibility factors (faktor
kerentanan), initiation factors (faktor inisiasi) dan progression factors (faktor
perkembangan). Susceptibility factors berupa usia lanjut, ras atau etnis
minoritas, penurunan massa ginjal, dan riwayat keluarga. Faktor-faktor ini
belum terbukti dapat menyebabkan penurunan fungsi ginjal. Initiation factors
merupakan kondisi yang secara langsung dapat menyebabkan penurunan fungsi
ginjal dan dapat dimodifikasi dengan terapi farmakologis. Kategori yang
termasuk dalam faktor inisiasi yaitu diabetees mellitus, hipertensi, penyakit
autoimun, penyakit ginjal polikistik, glomerulonefritis dan nefropati human
immunodeficiency (HIV). Progression factors merupakan faktor kerusakan
ginjal lebih lanjut. Pada umumnya faktor ini mempercepat penurunan fungsi
ginjal pada individu yang telah terdiagnosis memiliki kerusakan pada ginjal.
Progression factors ini meliputi penderita proteinuria, hipertensi, glikemia
pada penderita diabetes, hiperlipidemia, obesitas dan merokok (Dipiro et al.,
2017).
2.3.3.1 Diabetes Mellitus
Diabetes mellitus merupakan Initiation Factors dan Progression Factors.
Diabetes mellitus tipe I memiliki prevalensi 40% untuk terkena penyakit gagal
ginjal kronik, sedangkan diabetes mellitus tipe II memiliki prevalensi lebih
besar dari diabetes mellitus tipe I yaitu sebesar 50%. Dalam hal ini, individu
dengan diabetes mellitus tipe II lebih mudah terkena CKD. Sebuah studi dari
Uji Coba Intervensi Faktor Resiko Ganda mengatakan bahwa sekitar 3% dari
300.000 orang dengan diabetes mellitus dapat berkembang menjadi penyakit
gagal ginjal kronik stadium 5. Maka dari itu, individu dengan diabetes mellitus
memiliki resiko 12 kali lipat terkena penyakit gagal ginjal kronik stadium 5
(Dipiro et al., 2017).

14
2.3.3.2 Hipertensi
Hipertensi dapat meningkatkan resiko penyakit gagal ginjal kronik.
Penyakit gagal ginjal kronik dapat terjadi pada 40% individu hipertensi
dengan nilai GFR 90 ml/ menit/ 1,73 m2, 50% pada individu hipertensi
dengan nilai GFR 60 ml. Menit/ 1,73 m2, dan 75% pada individu dengan nilai
GFR 30 ml/ menit/ 1,73 m2. Rata-rata akhir dari tekanan darah arteri yang
rendah menghasilkan penurunan nilai GFR yang lebih rendah (Dipiro et al.,
2017)..
Tabel II.1 Jumlah Pasien Penyakit Gagal Ginjal Kronik Tahap 5 Berdasarkan
Diagnosa Etiologi di Indonesia (Alfiatin et al., 2014).
Etiologi Jumlah
E1 (Glumerulopati Primer) (GNC) 5447
E2 (Nefropati Diabetika) 14998
E3 (Nefropati Lupus) (SLE) 386
E4 (Penyakit Ginjal Hipertensi) 19427
E5 (Ginjal Polikistik) 498
E6 (Nefropati Asam Urat) 751
E7 (Nefropati Obstruksi ) 1800
E8 (Pielonefritis Chronic) (PNC) 1641
E9 (Lain-lain) 2768
E10 (Tidak Diketahui) 6224
Diagram 2. Diagnosa Etiologi Pasien Penyakit Gagal Ginjal Kronik Stadium5
(Indonesian Renal Registry, 2018).

15
Pada tahun 2018 ini proporsi etiologi terbanyak dari pasien Chronic kidney
disease stage 5 ialah hipertensi dengan kode E4 sebanyak 36% dan urutan
kedua nefropati diabetik dengan kode E2 sebanyak 28%. Etiologi kategori
tidak diketahui yang ditandai dengan kode E10 menunjukkan proporsi 12%,
sedangkan kategori Lain-lain dengan kode E9 sebanyak 5% (Indonesian Renal
Registry, 2018).
2.3.4 Faktor resiko CKD
Ketika mengalami gangguan fungsi ginjal, terdapat beberapa faktor
progresivitas penyakit gagal ginjal kronik sebagai berikut :
Tabel II.2 Faktor-faktor dalam progresivitas CKD (chris et al., 2014).
Tidak dapat dimodifikasi Dapat dimodifikasi
Usia Hipertensi
Jenis kelamin Proteinuria
Ras (ras Afrika-Amerika lebih
cepat)
Albuminuria
Genetik Glikemia
Hilangnya massa ginjal Obesitas
Dislipidemia
Merokok
Kadar asam urat
Usia merupakan salah satu dari faktor risiko penyakit gagal ginjal kronik.
Secara klinis pasien dengan usia >60 tahun memiliki risiko mengalami gagal
ginjal kronik 2,2 kali lebih besar dibanding pasien dengan usia <60 tahun. Hal
ini disebabkan semakin bertambahnya usia, semakin menurun pula fungsi
ginjal pada seseorang, sehingga menyebabkan penurunan fungsi ginjal secara
progresif serta serta keluhan ringan sampai keluhan berat (Pranandari &
Supadmi, 2015).
Obesitas merupakan salah satu faktor risiko yang dapat dimodifikasi.
Obesitas dpat meningkatkan risiko CKD melalui peradangan, stres oksidatif,
disfungsi endotel, hipervolemia, dan gangguan adipokin. Studi epidemiologi
Swedia menyatakan bahwa pada usia 20 tahun dan memiliki kelebihan berat

16
badan dengan indeks massa tubuh >25 kg/m2 beresiko 3 kali lipat terkena CKD
(Kazancioǧlu, 2013).
Berdasarkan hasil penelitian Pranandari & Supadmi, 2015 menyatakan
bahwa secara klinis, laki-laki 2 kali lebih besar mempunyai risiko terkena
penyakit gagal ginjal kronik dibanding perempuan. Kemungkinan hal ini
disebabkan karena perempuan lebih patuh dan disiplin dalam hal meminum
obat serta dalam hal mengatur pola hidup sehat.
Data klinis menunjukkan bahwa pasien hipertensi mempunyai risiko 3,2
kali lebih besar terkena penyakit gagal ginjal kronik. Hal ini disebabkan karena
penyakit hipertensi dapat meningkatkan tekanan intraglomerular sehingga
menyebabkan penurunan struktural dan fungsional dari glomerulus(Pranandari
& Supadmi, 2015). Data klinis 5 tahun terakhir menunjukkan 2,3% dari 8683
peserta uji coba mengalami kehilangan fungsi ginjal yang signifikan yang
ditandai dengan pengukuran kreatinin serum diatas 1,5 mg/ dl (Kazancioǧlu,
2013).
Diabetes mellitus mempunyai risiko 4,1 kali lebih besar terkena penyakit
gagal ginjal kronik. Penyebab utama terjadi gagal ginjal terminal ialah
nefropati diabetika (Pranandari & Supadmi, 2015). Menurut data Turkish
Sociaty of Nephrology bahwa populasi pasien diabetes mellitus dengan
hemodialisis sebesar 37,3%. Data USRDS pula menyatakan bahwa sebagian
besar pasien gagal ginjal kronik disebabkan oleh nefropati diabetik. Penyebab
penyakit gagal kronik pada pasien diabetes mellitus karena terjadinya
hiperfiltrasi, produk akhir glikosilasi serta oksigen reaktif (Kazancioǧlu, 2013).
Merokok dapat meningkatkan risiko CKD ditandai dengan proinflamasi,
stres oksidatif, disfungsi endotel, glomerulosklerosis dan atrofi tubular.
Merokok dengan jumlah yang banyak yaitu >20 batang per hari lebih cepat
meningkatkan risiko CKD, sedangkan pada studi lain menyatakan bahwa
merokok dengan tambahan 5 batang rokok per hari dapat meningkatkan serum
kreatinin sebesar >0,3 mg/dl (Kazancioglu, 2013). Pada fase akut, merokok
dapat mengakibatkan peningkatan tekanan darah, takikardi dan penumpukan
katekolamin dalam sirkulasi. Selain itu, dapat menyebabkan pembuluh darah
mengalami vasokonstriksi seperti pada pembuluh darah koroner, sehingga

17
terjadi peningkatan pembuluh darah ginjal yang mengakibatkan penurunan laju
filtrasi glomerulus dan fraksi filtrasi (Pranandari & Supadmi, 2015).
2.3.5 Manifestasi klinik CKD
Penyakit gagal ginjal kronik biasanya asimtomatik. Pada CKD stadium 1
dan stadium 2 tanda dan gejala serta gangguan metabolisme tidak terlihat,
namun terlihat pada CKD stadium 3 sampai stadium 5. Menurut Tanto et al,
2014 Tanda dan gejala CKD antara lain :
a. Gangguan keseimbangan cairan : edema perifer, efusi pleura, hipertensi,
asites;
b. Gangguan elektrolit dan asam basa : tanda dan gejala hiperkalemia, asidosis
metabolik, hiperfosfatomia;
c. Gangguan intestinal dan nutrisi : metallic taste, mual, muntah, gastritis, ulkus
peptikum, malnutrisi;
d. Kelainan kulit : kulit terlihat pucat, kering , pruritus, pigmentasi kulit,
ekimosis
e. Gangguan neuromuskular : kelemahan otot, fasikulasi, gangguan memori,
ensefalopati uremikum;
f. Gangguan metabolik endokrin : dislipidemia, gangguan metabolisme glukosa,
gangguan hormon seks;
g. Gangguan hematologi : anemia, gangguan hemostasis.
Pada penyakit gagal ginjal kronik tingkat penurunan nilai GFR dapat
bervariasi karena terdapat perbedaan pada penyakit yang mendasarinya, luas
kerusakan ginjal, responsifitas pengobatan serta kepatuhan dalam pengobatan.
Menurut KDOQI (Kidney Disease Outcomes Quality Initiative) bahwa gagal
ginjal kronik sebagai tanda klinis adanya proteinuria (Dipiro et al., 2017).
Selain itu, gambaran klinis lainnya dapat terlihat nyata jika ureum darah lebih
dari 200 mg/dl, hal ini disebabkan oleh konsentrasi ureum darah yang
merupakan indikator adanya retensi sisa-sisa metabolisme protein didalam
tubuh (Bargman & Skorecki, 2015).

18
2.3.6 Patofisiologi
Kerusakan struktural awal ginjal terjadi karena adanya penyakit primer
yang dapat mempengaruhi ginjal. Kerusakan ginjal pula dapat disebabkan oleh
faktor heterogen seperti, nefropati diabetik, pada nefrosklerosis hipertensi,
arteriol ginjal memiliki arteriol hyalinosis, dan kista ginjal terdapat pada
penyakit ginjal polikistik. Hal yang mendasari penyakit ini ialah hilangnya
massa nefron, hipertensi kapiler glomerulus, dan proteinuria (Dipiro et al.,
2017).
Paparan terhadap faktor resiko inisiasi dapat menyebabkan hilangnya
massa nefron, sehingga terjadi hipertrofi yang dapat mengkompensasi
hilangnya fungsi ginjal dan massa nefron. Hipertrofi ini dapat menyebabkan
perkembangan hipertensi intraglomerular yang dimediasi oleh angitensin II.
Angiotensin II merupakan vasokontriktor dari arteriol aferen dan eferen, tetapi
lebih berpengaruh pada arteriol eferen yang dapat menyebabkan peningkatan
pada kapiler glomerular sehingga terjadi peningkatan fraksi filtrasi (Dipiro et
al., 2017).
Peningkatan tekanan kapiler intraglomerular dapat menyebabkan
kerusakan fungsi ukuran selektif dari penghalang permeabilitas glomerulus,
sehingga menghasilkan peningkatan pada ekskresi albumin atau proteinuria.
Proteinuria dapat menyebabkan hilangnya nefron secara progresif yang
disebabkan oleh keruskan sel secara langsung. Hal ini menyebabkan terjadinya
jaringan parut interstitium, hilangnya unit nefron secara progresif, dan
pengurangan GFR (Dipiro et al, 2015). Hiperfiltasi, sklerosis dan progresifitas
penurunan fungsi nefron terjadi karena adanya peningkatan aktivitas sistem
renin-angiotensin-aldosteron. Beberapa pengaruh yang berperan terhadap
progresifitas penyakit ginjal kronik ialah albuminuria, hipertensi,
hiperglikemia, dan dislipidemia (Suwitra, 2014).
Penyakit ginjal kronik stadium awal belum menunjukkan tanda-tanda
spesifik namun, pada keadaan basal GFR menunjukkan nilai normal atau
kemungkinan meningkat. Penurunan fungsi nefron yang progresif terjadi
secara perlahan yang ditandai dengan peningkatan kadar urea dan kreatinin
serum. GFR dengan niali sebesar 60% pasien belum menunjukkan keluhan

19
(asimtomatik), tetapi sudah terjadi peningkatan kadar urea dan serum kreatinin.
Penderita baru merasakan keluhan ketika nilai GFR sebesar 30% yang ditandai
dengan keluhan pasien berupa nokturia, badan lemah, mual, nafsu makan
kurang serta penurunan berat badan. Ketika nilai GFR dibawah 30% tanda-
tanda nyata dari pasien baru terlihat seperti peningkatan tekanan darah, anemia,
gangguan metabolisme fosfor dan kalsium, infeksi saluran cerna, gangguan
keseimbangan air, serta gangguan keseimbangan elektrolit berupa natrium dan
kalium. Pada nilai GFR dibawah 15% akan terjadi komplikasi yang serius, dan
pasien segera diberikan terapi pengganti ginjal (renal replacement therapy)
seperti dialisis atau transplantasi ginjal (Suwitra, 2014).
Gambar 2.3.5 patofisiologi CKD (Dipiro et al., 2017).
2.3.7 Klasifikasi CKD
Stadium Chronic Kidney Disease diklasifikasikan menjadi 2 hal,
berdasarkan kategori GFR (G1-G5) dan kategori Albuminuria (A1-A3) sebagai
berikut:

20
Tabel II.3 Klasifikasi CKD berdasarkan 2 kategori: kategori GFR dan kategori
Albuminuria (Jadoul & Martin, 2018).
Kategori
GFR
Nilai GFR (ml/menit/1,73
m2) Keterangan
G1 >90 Normal atau tinggi
G2 60-89 Sedikit menurun
G3a 45-59 Sedikit menurun hingga
cukup menurun
G3b 30-44 Cukup menurun hingga
sangat menurun
G4 15-29 Sangat menurun
G5 <15 Gagal ginjal
Kategori
Albuminuria
AER (mg/24
jam)
ACR
(mg/g)
Keterangan
A1 <30 <30 Normal hingga sedikit
meningkat
A2 30-300 30-300 Cukup meningkat
A3 >300 >300 Sangat meningkat
Keterangan : GFR = Glomeruler Filtration Rate
AER = Albumin Excretion Rate
ACR = Albumin To Creatinin Ratio
Penurunan fungsi ginjal ditunjukkan dengan nilai GFR atau ACR seperti
tabel diatas. Seseorang dengan nilai GFR <60 ml/menit/1,73 m2 menunjukkan
terjadinya penurunan fungsi ginjal disertai nilai ACR >30 mg/g, nilai ACR ini
digunakan untuk melihat ekskresi albumin urin (United States Renal Data
System, 2018).
Nilai GFR > 90 ml/ menit/ 1,73 m2 dengan nilai ACR < 30mg/g
menunjukkan fungsi ginjal dalam keadaan normal atau resiko gagal ginjal
kronik sangat rendah. Namun, ketika nilai GFR turun menjadi 45-59 ml/ menit/
1,73 m2 dengan nilai ACR 30-300 mg/g akan menunjukkan resiko gagal ginjal
kronik yang cukup tinggi. Nilai GFR yang memiliki resiko tinggi sebagai

21
penyakit gagal ginjal kronik ditunjukkan dengan nilai GFR < 30 ml/ menit/
1,73 m2 dengan nilai ACR > 300 mg/g (United States Renal Data System,
2018).
Menurut Suwitra 2014, Klasifikasi CKD juga dibedakan berdasarkan Laju
Filtrasi Glomerulus (LFG), dengan menggunakan rumus Cockcroft-Gault
sebagai berikut :
GFR = (𝟏𝟒𝟎−𝒖𝒔𝒊𝒂 ) 𝒙 𝑩𝒆𝒓𝒂𝒕 𝑩𝒂𝒅𝒂𝒏
𝟕𝟐 𝒙 𝑲𝒓𝒆𝒂𝒕𝒊𝒏𝒊𝒏 𝑷𝒍𝒂𝒔𝒎𝒂 (𝒎𝒈/𝒅𝒍)𝒙 𝒌𝒐𝒏𝒔𝒕𝒂𝒏𝒕𝒂
Keterangan : konstanta : 0,85 (jika perempuan)
1 (jika laki-laki)
Rumus ini mengestimasi klirens kreatinin berdasarkan kadar serum kreatinin,
usia, jenis kelamin, dan berat badan. Pada wanita rumus ini disesuaikan dengan
kadar kreatinin wanita yaitu 15% lebih rendah karena jumlah massa otot.
Kekurangan yang dimiliki oleh rumusi ini ialah :
a. GFR diatas 60 ml/menit kurang akurat menggunakan rumus ini
b. Dapat terjadi overestimasi GFR karena rumus ini hanya memperhitungkan
klirens kreatinin dibanding laju filtrasi glomerulus
c. Tidak dapat dikalibrasikan dengan metode pemeriksaan kretinin baru karena
saat pemeriksaan mengukur kadar kreatinin, rumus ini menggunakan
metode pemeriksaan lama.
Adapun rumus lain yang digunakan untuk menghitung Laju Filtrasi
Glomerulus (LFG) yaitu menggunakan rumus Studi Modification of Diet in
Renal Disease (MDRD). Rumus ini menggunakan 4 variabel yaitu kadar serum
kreatinin, usia, jenis kelamin serta ras. Rumus ini telah direkomendasikan oleh
The National Kidney Disease Education Program of The National Institute of
Diabetes and Digestive and Kidney Disease untuk memprediksi nilai laju
filtrasi glomerulus.
GFR (ml/ menit/ 1,73 m2) = 186 x Scr (mg/dl) – 1,154 x usia – 0,203 x 0,742
(jika perempuan) x 1,210 (jika ras Afrika –Amerika).

22
2.3.8 Diagnosa dan Pemeriksaan CKD
Nilai GFR dan kreatinin serum merupakan sarana untuk mendiagnosa
adanya penyakit gagal ginjal kronik atau CKD. Fungsi ginjal pada orang
dewasa dikatakan normal yaitu ditandai dengan nilai Glomerular Filtration
Rate (GFR) >90 ml/ menit/ 1,73 m2. Setiap individu didiagnosis mempunyai
penyakit gagal ginjal kronis ialah individu dengan nilai GFR <60 ml/ menit/
1,73 m2, yang juga ditandai dengan gejala seperti proteinuria, hematuria,
ataupun kerusakan struktural dan fungsional ginjal lainnya (Dipiro et al.,
2017).
Dalam hal ini menurut Tanto et al, 2014 terdapat beberapa pemeriksaan
penunjang terhadap penyakit gagal ginjal kronik atau CKD antara lain :
a. Pemeriksaan darah lengkap : ureum meningkat, kreatinin serum meningkat.
Estimasi perhitungan GFR dapat diketahui dari kadar kreatinin serum yang
menggunakan rumus Cockrof-Gault atau studi MDRD;
b. Pemeriksaan elektrolit : hiperkalemia, hipokalsemia, hiperfosfatemia;
c. Pemeriksaan kadar glukosa darah, profil lipid ;
d. Analisis gas darah : asidosis metabolik (pH menurun, HCO3 menurun);
e. Urinalisis dan pemeriksaan albumin urin;
f. Sedimen urin : sel tubulus ginjal, sedimen eritrosit, sedimen leukosit,
sedimen granuler kasar, serta adanya eritrosit yang dismorfik ;
g. Pemeriksaan protein urin kuantitatif 24 jam ;
h. Pencitraan : USG ginjal ; BNO-IVP
i. Biopsi ginjal : pemeriksaan ini dalam kondisi tertentu dan untuk
memudahkan diagnosis penyakit gagal ginjal kronik apabila pemeriksaan
klinis, laboratorium, dan pencitraan menunjukkan bukti yang belum pasti ;
j. Pemeriksaan lain untuk komplikasi seperti EKG, foto polos toraks, dan
ekokardiografi.
Tabel II.4 Data laboratorium (Said et al., 2020).
Jenis pemeriksaan Nilai normal
Hemoglobin 11,0 – 14,7 g/dl
Hematokrit 35.2 – 46 µL
Eritrosit 3,72 – 5,06

23
Leukosit 3,17 – 8,40
Trombosit 167 – 390
MCV 87,1 – 102,4 %
MCH 26,8 – 32,4 pg
MCHC 29,6 – 32,5 %
SGOT/AST < 31 U/L
SGPT/ALT < 31 U/L
Albumin 3,5 – 5,2 g/dl
Ureum 15 – 40 mg/dl
Kreatinin 0,6 – 1,3 mg/dl
Asam urat 2,5 – 5,5 mg/dl
Natrium (Na+) 135 – 150 mEq/L
Kalium (K+) 3,6 – 5,5 mEq/L
Klorida (Cl-) 94 -111 mEq/L
LDL < 130 mg/dl
HDL > 35 mg/dl
Kolestrol total < 200 mg/dl
Trigliserida < 200 mg/dl
2.3.9 Komplikasi CKD
2.3.9.1 Anemia
Anemia merupakan konsentrasi hemoglobin (Hb) atau hematokrit (Hct).
Anemia dapat terjadi pada 80-90% pasien penyakit ginjal kronik. Penyakit
gagal ginjal kronik dapat disebabkan oleh adanya defisiensi eritropoetin,
defisiensi besi, kehilangan darah (misalnya pendarahan saluran cerna dan
hematuri), massa hidup eritrosit yang pendek karena terjadinya hemolisis,
defisiensi asam folat, penekanan sumsum tulang oleh substansi urenik, proses
inflamasi akut ataupun kronik (Tarigan & Juli, 2014). Data dari studi CKiD
menunjukkan bahwa hemoglobin mulai menurun secara signifikan pada GFR
<43 mL/ menit/ 1,73 m2 yang diukur dengan iohexol clearance (yang setara
dengan GFR 58 mL/ menit/ 1,73 m2 ketika diperkirakan dengan rumus

24
Schwartz) , dengan penurunan hemoglobin 0,3 g / dL setiap penurunan GFR 5
ml/menit /1,73 m2. Estimasi anemia pada pasien gagal ginjal kronik ditandai
dengan hemoglobin kurang dari 0,3 g/dl (Himmelfarb & Ikizler, 2018).
Terapi yang dianjurkan pada anemia ialah pemberian eritropoitin (EPO).
Terapi pemberian eritropoitin (EPO) dimulai pada pasien CKD dengan
konsentrasi Hb sekitar 9 g/ dl dan 10 g/ dl (90 dan 100 g/ L ; 5,59 dan 6,21
mmol/ L). Penyebab utama resistensi terhadap pengobatan anemia dengan EPO
ialah kekurangan zat besi. Maka dari itu, suplemen zat besi menjadi salah satu
suplemen yang diperlukan oleh sebagian besar pasien CKD sebagai pengisi
ulang cadangan besi yang telah habis karena meningkatnya kebutuhan zat besi
dan kehilangan darah yang terus-menerus. Terapi besi dengan rute parenteral
digunakan untuk meningkatkan respon terhadap terapi EPO dan dapat
menyesuaikan dosis sesuai dengan target yang diinginkan. Terapi besi rute oral
mempunyai absorpsi yang buruk dan ketidakpatuhan dalam mengkonsumsi.
Selain itu, pemberian zat besi dengan rute IV tidak dapat berkolrelasi dengan
efek farmakodinamik karena mempunyai profil farmakokinetik yang berbeda,
sehingga menimbulkan efek samping berupa reaksi alergi, hipotensi, pusing,
dispnea, sakit kepala, nyeri punggung bawah, artralgia, sinkop, dan radang
sendi. Efek samping yang paling umum dari pemberian eritropoitin (EPO)
ialah hipertensi (Dipiro et al., 2017).
Dosis penggunaan EPO sebagai berikut :
- Fase koreksi : 2000-4000 IU subkutan, 2-3 kali / minggu selama 4 minggu
dengan target diinginkan Hemoglobin (Hb) naik 1-2 g/dl atau Hematokrit
(Hct) naik menjadi 2-4% ;
- Apabila target belum mencapai target EPO yang diinginkan maka, EPO
dinaikkan 50% ;
- Apabila Hemoglobin naik >2,5 g/dl atau Hematokrit naik menjadi 8% dalam
4 minggu maka, dosis diturunkan sebanyak 25% (chris et al., 2014).
2.3.9.2 Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD)
Pada populasi pasien CKD sering terjadi gangguan metabolisme mineral
dan tulang (Mineral and Bone Disorder) dan termasuk kelainan pada hormon

25
paratiroid (PTH), kalsium, fosfor, produk kalsium fosfor vitamin D, pergantian
tulang, serta klasifikasi jaringan lunak.
Kadar normal fosfor dan kalsium serum pada setiap individu dengan ginjal
yang sehat dipelihara melalui interaksi 3 hormon yaitu hormon paratiroid
(PTH), 1,25 (OH) 2D (kalsitriol, metabolit aktif vitamin D), dan faktor
pertumbuhan fibroblast 23 (FGF 23). Hormon ini bekerja pada 3 organ utama
yaitu tulang, ginjal, dan usus. Gangguan umum pasien CKD diawali dengan
ginjal mempunyai peran penting dalam pengaturan kadar fosfor dan kadar
kalsium serum normal, sehingga dapat mengubah vitamin D menjadi kalsitriol
serta merespon hormon paratiroid (PTH) dan faktor pertumbuhan fibroblast 23
(FGF 23). Kemudian kelainan etabolisme mineral dapat terjadi pada awal CKD
ataupun pada stadium 2, sehingga dapat berkembang sesuai dengn
memburuknya fungsi ginjal (Kendrick, 2018).
Keseimbangan kadar fosfor dan kadar kalsium serum dipelihara melalui
interaksi hormon yang kompleks, sehingga menimbulkan efek pada tulang,
saluran gastrointestinal (GI), ginjal, dan kelenjar paratiroid. Apabila penyakit
ginjal berlanjut, aktivasi vitamin D pada ginjal pula akan terganggu, yang
kemudian dapat mengurangi absorpsi kalsium oleh usus, sehingga
menghasilkan sekresi PTH yang dirangsang oleh penurunan konsentrasi
kalsium darah (Dipiro et al., 2017).
Pengobatan yang digunakan ialah pembatasan fosfor, dialisis, dan
paratiroidektomi merupakan terapi nonfarmakologis untuk manajemen
hiperfosfatemia dan CKD-MBD. Dibawah ini terdapat pedoman dari KDOQI
mengenai rentang kalsium, fosfor, produk kalsium-fosfor, serta PTH utuh yang
berdasarkan tahap CKD.
Tabel 4. Pedoman untuk kalsium, fosfor, produk kalsium-fosfor, dan hormon
paratiroid berdasarkan tahap CKD (Dipiro et al, 2017).

26
2.3.9.3 Gangguan Keseimbangan Kalium
Fungsi ginjal dalam keadaan normal akan mengekskresi 98% dari intake
klium harian dan juga berperan penting dalam maintenance homeostasis
kalium. Pada pasien CKD, gangguan elektrolit yag rentan terjadi ialah
hiperkalemia. Hiperkalemia merupakan gangguan elektrolit yang paling umum
terjadi pada pasien CKD dengan bukti penelitian retrospektif nilai n= 240.000.
Penyebab hiperkalemia adalah penurunan filtrasi glomerulus dan sekresi
elektrolit kalium.
Hiperkalemia sering ditandai dengan konsentrasi kalium serum >5,3
mEq/L. hiperkalemia ringan ditandai dengan konsentrasi kalium 5.4 mEq/ L
sampai < 6 mEq/L, hiperkalemia sedang konsentrasi kalium 6 mEq/L sampai
<7 mEq/ L, dan hiperkalemia berat ditandai dengan konsentrasi kalium > 7
mEq/ L (Dhondup & Qian, 2017). Terapi hiperkalemia pada pasien CKD
antara lain :
Kalsium 6,8 mmol, setara dengan 10 ml CaCl (10%) atau 30 ml larutan
kalsium glukonat (10%) + 50-250 ml hypertonic saline (10%) + 50-100
mmol natrium bikarbonat + 10 unit insulin reguler sevara IV
40 mg Furosemid secara oral, namun pemberian diuretik tidak efektif pada
pasien dengan nilai GFR <40 ml/ menit/ 1,73 m2
Fludrocortison asetat > 0,1 mg per hari
Dialisis, misal hemodialisis dan peritoneal dialysis. Pasien CKD kronis
dengan terapi hemodialisis, keterlambatan pengobatan selama 2 hari dapat
memberikan hasil yang buruk pada terapi (National Kidney Foundation,
2016).

27
2.3.9.4 Asidosis metabolik
Pada kondisi fisiologis, tubulus ginjal dapat mereabsorbsi bikarbonat yang
telah difiltrasi setiap hari. Selain itu, tubulus ginjal juga dapat menetralisir
pembentukan asam dalam tubuh. Seiring dengan penurunan fungsi ginjal dan
penurunan pembentukan bikarbonat, produksi asam endogen pada CKD tidak
berubah, sehingga menjadi salah satu pemicu adanya asidosis metabolik
(Dhondup & Qian, 2017).
Pada pasien CKD, asidosis metabolik dikaitkan dengan peningkatan
katabolisme protein otot dan promosi PEW (Protein energy wasting). Asidosis
metabolik dapat merangsang oksidasi asam amino esensial dan meningkatkan
kebutuhan protein untuk pasien yang menjalankan dialisis. Bikarbonat oral atau
atau intradialitik merupakan suplemen yang sering dikaitkan dengan
peningkatan asupan protein dan energi, peningkatan kadar albumin serum, dan
dapat memperlambat perkembangan CKD stadium 3 sampai 4.
Penatalaksanaan pada pasien asidosis metabolik dengan CKD yaitu diberikan
bikarbonat untuk memperbaiki asidemia. Pada pasien CKD yang belum
menjalani dialisis bikarbonat serum stabil dengan nilai > 24 mmol/L (Ikizler,
2014 ; (Dipiro et al., 2017).
2.3.9.5 Hipertensi
Secara progresif, hipertensi merupakan penyebab utama dari hilangnya
fungsi ginjal. Hipertensi sering terjadi ketika salah satu arteri ginjal
menyempit. Hipertensi esensial yang berlangsung lama dapat menyebabkan
kerusakan pada interlobular serta arteriola aferen dan eferen, yang ditandai
dengan fibrosis dan hialinisasi dinding pembuluh darah. Penyempitan arteri
dan erteriol aferen akan menyebabkan berkurangnya aliran darah menuju
glomerulus sehingga terjadi iskemia glomerular dan glomerulosklerosis.
Kondisi ini menurunkan aliran plasma yang dapat memicu iskemia tubular
sehingga menyebabkan terjadinya gagal ginjal kronik (M. Adi Firmansyah,
2013 ; Ali et al, 2017).
2. 4 Penatalaksanaan Terapi CKD
Tujuan terapi CKD adalah untuk meminimalkan perkembangan CKD
ataupun keparahan komplikasi yang terjadi pada CKD, dan juga dapat

28
meminimalisasi prevalensi ESRD (End Stage Renal Disease) (Dipiro et al.,
2017). Penatalaksaan penyakit gagal ginjal kronik antara lain:
- Terapi spesifik terhadap penyakit yang mendasarinya misal hipertensi dan
diabetes melitus
- Terapi dan pencegahan terhadap kondisi komorbid
- Memperlambat perburukan fugsi ginjal
- Terapi dan pencegahan terhadap penyakit kardiovaskular
- Terapi dan pencegahan terhadap komplikasi CKD
- Terapi pengganti ginjal verupa dialisis atau transplantasi ginjal (Suwitra,
2014).
Tabel II.5 Rencana tatalaksana penyakit ginjal kronik berdasarkan
derajatnya (Suwitra, 2014).
Derajat LFG (ml/menit/1,73 m2) Rencana tatalaksana
1 >90 Terapi penyakit dasar, kondisi komorbid,
evaluasi pemburukan fungsi ginjal,
memperkecil risiko kardiovaskular
2 60 – 89 Menghambat perburukan fungsi ginjal
3 30 – 59 Evaluasi dan terapi komplikasi
4 15 – 29 Persiapan untuk terapi pengganti ginjal
5 < 15 Terapi pengganti ginjal
a. Terapi Spesifik Terhadap Penyakit yang Mendasarinya
Terapi ini paling tepat dilaksanakan sebelum terjadi penurunan laju filtrasi
glomerulus. Pemeriksaan secara ultrasonografi, biopsi, dan histopatologi pada
ginjal yang masih dalam keadaan normal dapat menentukan indikasi yang tepat
terhadap terapi spesifik (Suwitra, 2014).
b. Terapi dan Pencegahan terhadap Kondisi Komorbid
Kondisi komorbid pasien gagal ginjal kronik dapat diketahui melalui
pengawasan dan pencatatan penurunan nilai GFR. Hal ini dilakukan untuk
mencegah perburukan kondisi pasien. Faktor-faktor komorbid yang dimaksud
antara lain : gangguan keseimbangn cairan, hipertensi, infeksi traktus urinarius,

29
obstruksi traktus urinarius, obat-obatan nefrotoksik, bahan radiokontras,
ataupun peningkatan aktivitas penyakit yang mendasarinya (Suwitra, 2014).
c. Menghambat Perburukan Fungsi Ginjal
Hiperfiltrasi glomerulus merupakan penyebab utama terjadinya
perburukan fungsi ginjal. Terdapat dua cara untuk mengurangi hiperfiltrasi
glomerulus yaitu pembatasan asupan protein dan terapi farmakologis.
Pembatasan asupan protein dilakukan pada nilai GFR < 60 ml/ menit/ 1,73
m2. Dalam hal ini protein yang diberikan merupakan protein yang memiliki
kandungan biologis tinggi. Pemberian protein pada pasien CKD pre-dialisis
sekitar 0,6-0,75 g/kg BB ideal/ hari, pemberian protein pada pasien CKD yang
menjalani hemodialis sekitar 1,2 g/kg BB ideal/ hari, selanjutnya pada pasien
CKD dengan dialisis peritoneal sekitar 1,2-1,3 g/ kg BB ideal/ hari, dan pada
pasien yang menjalani transplantasi ginjal protein yang diberikan sekitar 1,3
g/kg BB ideal/ hari, namun pada 6 minggu pertama pasca transplantasi ginjal
protein dilanjutkan sekitar 0,8-1 g/kg BB ideal/ hari (Tanto et al, 2014).
Apabila asupan protein berlebih dapat mengakibatkan perubahan hemodinamik
ginjal, sehingga dapat meningkatkan aliran darah dan tekanan intraglomerulus
(intraglomerulus hyperfiltration), yang kemudian akan memperburuk fungsi
ginjal. Pembatasan asupan protein sering dihubungkan dengan pembatasan
fosfat, hal ini disebabkan karena protein dan fosfat berasal dari sumber yang
sama. Pembatasan fosfat dilakukan untuk mencegah terjadinya hiperfosfatemia
(Suwitra, 2014).
Terapi farmakologis yang penting ialah untuk mengurangi hipertensi
intraglomerular. Hipertensi intraglomerulus dan hipertrofi glomerulus dapat
dikurangi dengan mengontrol tekanan darah. Terdapat beberapa obat
antihipertensi yang sering digunakan untuk mengurangi perburukan fungsi
ginjal antara lain : Angiotensin Converting Enzym (ACE Inhibitor), Angitensin
Reseptor Blocker (ARB), dan Calsium Chanel Blocker (CCB). Terapi
farmakologis ini dikaitkan dengan derajat proteinuria, hal ini dikarenakan
proteinuria juga sebagai faktor risiko terjadinya perburukan fungsi ginjal
(Suwitra, 2014).

30
Tabel II.6 Pembatasan asupan protein dan fosfat pada CKD (Suwitra, 2014).
GFR Asupan protein g/kg/hari Asupan fosfat
g/kg/hari
>60 Tidak dianjurkan Tidak dibatasi
25 – 60 0,6-0,8 g/ kg/ hari, termasuk
nilai biologi tinggi > 0,35 g/
kg/ hari
< 10 g
5 – 25 0,6-0,8 g/ kg/ hari, termasuk
nilai biologi tinggi > 0,35 g/
kg/ hari atau tambahan asam
amino esensial atau asam
keton sebanyak 0,3 g
< 10 g
< 60 0,8 g/ kg/ hari (+1 g protein
atau 0,3 g/ kg tambahan asam
amino esensial atau asam
keton)
< 9 g
d. Terapi dan Pencegahan Terhadap Penyakit Kardiovaskular
Penyakit kardiovaskular merupakan penyebab dari kematian dengan
persentasi 40-45% pasien penyakit ginjal kronik. Dalam hal ini pencegahan
dan terapi yang dilakukan ialah pengendalian hipertensi, pengendalian
diabetes, pengendalian dislipidemia, pengendalian anemia, pengendalian
hiperfosfatemia, dan terapi pada gangguan keseimbangan elektrolit dan
kelebihan cairan (Suwitra, 2014).
e. Pembatasan Cairan dan Elektrolit
Pembatasan cairan dan elektrolit dilakukan untuk mencegah terjadinya
edema dan penyakit kardiovaskular. Jumlah air yang masuk kedalam tubuh
harus seimbang dengan jumlah air yang keluar, baik keluar melalui urin
maupun insensible water loss. Adapun pembatasan asupan elektrolit yang
harus dikontrol ialah asupan kalium dan natrium. Pembatasan asupan kalium
dilakukan untuk mencegah terjadinya hiperkalemia, maka dari itu harus
dibatasi penggunaan obat-obat yang mengandung kalium dan makanan yang

31
mengandung kalium. Pembatasan asupan natrium dilakukan untuk mencegah
terjadinya hipertensi dan edema. Pemberian garam natrium disesuaikan dengan
tingginya tekanan darah dan derajat edema yang terjadi (Suwitra, 2014).
f. Transplantasi Ginjal
Transplantasi ginjal dilakukan pada pasien CKD stadium 5 atau stadium
akhir yang ditandai dengan nilai GFR <15 ml/ menit/ 1,73 m2 (Suwitra, 2014).
Transplantasi ginjal berfungsi dapat meningkatkan angka kematian dan
meningkatkan kualitas hidup pasien CKD (Armelia et al, 2017). Pada
persiapan transplantasi ginjal dilakukan beberapa pemeriksaan yang meliputi
pemeriksaan fisik, pemeriksaan laboratorium, pemeriksaan penunjang seperti
fungsi dan anatomi ginjal serta saluran kemih (Pardede et al., 2016).
2. 5 Hipertensi pada CKD
Definisi hipertensi menurut European Society Hypertention (ESH) dan
European Society Cardiology (ESC) tahun 2018 bahwa dikatakan hipertensi
ketika tekanan darah sistolik mencapai > 140 mmHg dan tekanan darah
diastolik > 90 mmHg. Pada penyakit gagal ginjal kronis, hipertensi dikaitkan
dengan retensi natrium sehingga menyebabkan hipervolemia. Hipervolemi
terjadi karena gangguan pada ekskresi natrium dan ekskresi air dengan urin,
mengakibatkan peningkatan tekanan darah guna meningkatkan ekskresi untuk
mempertahankan isovolemia. Ginjal iskemi yang berhubungan dengan fibrosis
ginjal dan jaringan parut mengakibatkan peningkatan pada sistem renin-
angiotensin-aldosteron (Covic et al., 2017). Sistem renin-angiotensin
aldosteron merupakan sistem hormonal enzimatik yang bersifat multikompleks
dan memiliki peran penting terhadap peningkatan tekanan darah pengaturan
keseimbangan cairan tubuh dan elektrolit (Tessy, 2018). Aktivasi sistem renin-
angiotensin-aldosteron dapat menyebabkan vasokonstriksi yang dimediasi oleh
angiotensin II serta retensi garam yang dimediasi oleh aldosterone,
mengakibatkan peningkatan resistensi perifer lokal dan peningkatan volume
darah (Turgut et al, 2017).
Hipertensi muncul pada 40% individu dengan nilai GFR 90 ml/ menit/1,73
m2, 55% pada individu dengan GFR 60 ml/ menit/ 1,73 m2, dan 75% pada
individu dengan GFR 30 ml/ menit/ 1,73 m2 (Dipiro et al., 2017). Hipertensi
merupakan salah satu penyakit kardiovaskular yang menjadi faktor utama

32
terjadinya penyakit gagal ginjal kronik. Sekitar 70% sampai 80% pasien
dengan CKD stadium 1 sampai stadium 4 mempunyai hipertensi dengan
prevalensi hipertensi yang dapat meningkat seiring dengan penurunan nilai
GFR, sehingga 80% sampai 90% pasien menjalankan dialisis yang dikarenakan
oleh hipertensi (Sarnak & Weiner, 2018).
Gambar 2.5 algoritma hipertensi pada pasien CKD (Palm & Nordquist, 2011).
2. 6 Antihipertensi pada Chronic Kidney Disease (CKD)
Menurut Joint National Commite (JNC) VIII bahwa pencegahan, evaluasi,
dan perawatan tekanan darah untuk pasien CKD harus sesuai ketentuannya
yiatu < 140/ 90 mmHg. Pengontrolan tekanan darah tinggi pada pasien CKD
lebih sulit dibanding pasien yang tidak memiliki CKD. Maka dari itu,
diperlukan tiga atau lebih obat antihipertensi untuk mencapai tujuan tekanan
darah yang normal (Dipiro et al., 2017).

33
Gambar 2.6 algoritma antihipertensi pada pasien CKD (Dipiro et al., 2017).
Gambar 2.6. Efek antihipertensi pada Renal Blood Flow (RBF) dan Glomerular
Filtration Rate (GFR) (Dipiro et al., 2017).

34
2.6.1 Diuretik
Diuretik dapat menurunkan volume darah dan cairan ekstraseluler dengan
cara meningkatkan ekskresi natrium, air dan klorida, sehingga terjadi
penurunan curah jantung dan tekanan darah. Pada mekasnisme lainnya,
terdapat beberapa diuretik yang dapat menurunkan resistensi perifer sehingga
menambah efek hipotensi. Hal ini diakibatkan oleh penurunan natrium di ruang
interstisial dan di dalam sel otot polos pembuluh darah yang kemudian
menghambat influks kalsium (Nafrialdi, 2012). Diuretik merupakan adekuat
untuk hipertensi esesial ringan sampai ringan , dan diuretik efektik terhadap
penurunan tekanan darah sebesar 10-15 mmHg. Namun, pada hipertensi berat
diuretik digunakan dalam kombinasi dengan obat vasodilator guna untuk
mengatasi kecenderungan retensi natrium (Katzung, 2017) .
Diuretik golongan tiazid dapat diberikan ke pasien yang memiliki
hipertensi ringan sampai sedang, serta memiliki fungsi ginjal dan jantung yang
normal. Mekanism kerja dari obat golongan tiazid ialah menghambat transport
bersama (symport) Na-Cl di tubulus distal ginjal, mengakibatkan peningkatan
pada ekskresi Na+ dan Cl-. Pada hipertensi berat diperlukan diuretik kuat. Obat
golongan ini memiliki mekanisme kerja yang cepat dan efek diuretiknya lebih
kuat dari golongan tiazid, maka dari itu obat golongan ini digunakan pada
pasien hipertensi yang memiliki gangguan fungsi ginjal (kreatinin serum > 2,5
mg/dl) dan gagal jantung. Diuretik hemat kalium berfungsi untuk menghindari
deplesi kalium yang berlebih. Apabila diuretik hemat kalium diberikan pada
pasien dengan gagal ginjal dapat menimbulkan hiperkalemia (Nafrialdi, 2012).
2.6.2 Calsium Chanel Blocker (CCB)
Calsium Chanel Blocker (CCB) merupakan pengobatan yang digunakan
pada hipertensi, angina, dan takikardia supraventrikular. Mekanisme kerja
Calsium Chanel Blocker (CCB) ialah menghambat influks kalsium pada sel
otot polos pembuluh darah dan miokard serta dapat menurunkan resistensi
perifer dan tekanan darah. Dengan demikian, efek samping yang diperoleh
ialah retensi cairan dan edema pada pergelangan kaki yang dapat menimbulkan
masalah pada pasien CKD. CCB golongan dihidropiridin berfungsi untuk
menghilangkan autoregulasi ginjal pada pasien CKD, dan golongan non

35
dihidropiridin dapat mengurangi proteinuria (Segall, 2017). Penggunaan
nifedipin dapat menyebabkan penurunan resistensi perifer yang disertai oleh
reflek takikardia dan vasokonstriksi (Nafrialdi, 2012). Pasien yang diberikan
obat golongan dihidropiridin dapat mengaktifkan refleks simpatis yang disertai
takikardia ringan yang dapat mempertahankan atau meningkatkan curah
jantung (Katzung, 2017)
Secara efektif golongan CCB dapat menurunkan tekanan darah pada
pasien dialisis tanpa memerlukan dosis tambahan pasca dialisis. Berdasarkan
Randomized Conrtolled Trial (RCT) bahwa amlodipin dapat menurunkan
tekanan darah sistolik sebesar 10 mmHg lebih banyak dari plasebo, tanpa
adanya peningkatan risiko hipotensi intradialitik. Sebuah RCT juga
membandingkan penggunaan amlodipin dengan plasebo pada 251 pasien
hipertensi dengan hemodialisis menyatakan bahwa tidak menemukan
perbedaan dari penyebab kematian selama 30 bulan ini. Namun, secara
signifikan amlodipin dapat mengurangi penyebab kematian dan kejadian
kardiovaskular. Pada pasien lansia dengan CKD, penggunan golongan CCB
yang disarankan ialah nikardipin dan nimodipin. Hal ini dikarenakan
berkurangnya aliran darah ke hati pada pasien lansia (Segall, 2017).
Tabel II.7 Dosis antihipertensi golongan CCB (Martin & Talbert, 2013)
Obat (Merek) Kisaran dosis
harian (mg/hari) Dosis per hari
CCB – Dihidropiridin
Amlodipine (Norvasc) 5 – 10 1
Felodipine (Plendil) 5 – 20 1
Isradipine (DynaCirc) 5 – 10 2
Isradipine SR (DynaCirc
SR) 5 – 20 1
Nicardipine sustained
release (Cardene SR) 60 – 120 2
Nifedipine long acting
(Procardia XL) 30 – 90 1
Nisoldipine (Sular) 10 – 40 1

36
CCB – Nondihidropiridine
Diltiazem (Cardizem SR,
others) 120 – 320 2
(Cardizem CD,
others) 120 – 320 2
Verapamil (Calan SR,
Isoptin SR) 120 – 480 1
(Covera HS) 180 – 480 1 saat istirahat
(Verelan PM) 100 – 400 1 saat istirahat
2.6.3 Angiotensin Receptor Blocker (ARB)
ARB mempunyai mekanisme kerja dengan memblok aktivitas kimia
angiotensin II. Angiotensin II merupakan vasokonstriktor kuat yang mana
dapat menyebabkan pembuluh darah menyempit, sehingga mengakibatkan
peningkatan tekanan darah dan aliran darah sedikit yang melalui ginjal. ARB
dan ACEI merupakan pengobatan lini pertama pada pasien hipertensi dengan
CKD, terlepas dari tingkat proteinuria dan status diabetes. Akan tetapi,
beberapa guidelines menunjukkan bahwa obat-obatan golongan ini lebih baik
pada pasien CKD dengan mikroalbumin atau makroalbumin, yang mana dapat
dikaitkan dengan hasil ginjal dan kardiovaskular (Segall, 2017).
Reseptor angiotensin II terdiri dari dua kelompok besar yaitu AT 1 dan
AT2. Reseptor AT 1 terutama berada di otot polos pembuluh darah dan di otot
jantung. Selain itu, reseptor AT 1 juga terdapat di ginjal, otak dan kelenjar
adrenal. Seluruh efek fisiologis dari Angiotensin II memiliki peran utama
dalam homeostasis kardiovaskular dengan perantara reseptor AT 1. ARB
mempunyai efek yang sama dengan ACE Inhibitor tapi, karena tidak berefek
pada metabolisme bradikinin, maka obat ini tidak memiliki efek samping yang
sama dengan ACE Inhibitor (Nafrialdi, 2012). Secara total obat-obatan
golongan ini dapat menghambat efek angiotensin dibandingkan golongan ACE
Inhibitor, karena terdapat enzim-enzim diluar ACEI yang dapat menghasilkan
angiotensin II (Katzung, 2017).

37
Tabel II.8 Dosis Obat antihipertensi golongan ARB (Martin & Talbert, 2013).
Obat (Merek) Kisaran dosis
harian (mg/hari) Dosis per hari
Candesartan (Atacand) 8 – 32 1 atau 2
Eprosartan (Teveten) 600 – 800 1 atau 2
Irbesartan (Avapro) 150 – 300 1
Losartan (Cozaar) 50 – 100 1 atau 2
Olmesartan (Benicar) 20 – 40 1
Telmisartan (Micardis) 20 – 80 1
Valsartan (Diovan) 80 – 320 1
2.6.4 Angiotensin Converting Enzym Inhibitor (ACEI)
Angiotensin Converting Enzym Inhibitor (ACEI) bekerja dengan
menghambat perubahan Angiotensin I menjadi Angiotensin II yang
menyebabkan terjadinya vasodilatasi dan penurunan sekresi aldosteron. ACE
Inhibitor mempunyai efek vasodilatasi dan dapat menghambat degradasi
bradikinin sehingga menyebabkan peningkatan kadar bradikinin dalam darah.
Vasodilatasi dapat menurunkan tekanan darah, sedangkan berkurangnya
aldosteron akan mengakibatkan ekskresi air, natrium, dan ekskresi kalium
(Nafrialdi, 2012).
Tabel II.9 Dosis obat antihipertensi golongan ACEI (Martin & Talbert, 2013).
Obat (Merek) Kisaran dosis
harian (mg/hari) Dosis per hari
Benazepril (Lotensin) 10 – 40 1 atau 2
Captopril (Capoten) 12,5 – 150 2 atau 3
Enalapril (Vasotec) 5 – 40 1 atau 2
Fosinopril (Monopril) 10 – 40 1
Lisinopril (Prinivil,
Zestril) 10 – 40 1
Moexipril (Univasc) 7,5 – 30 1 atau 2
Perindopril (Aceon) 4 – 16 1

38
Quinapril (Accupril) 10 – 80 1 atau 2
Ramipril (Altace) 2,5 – 10 1 atau 2
Trandolapril (Mavik) 1 – 4 1
2. 7 Tinjauan Obat Golongan ACE-I
Angiotensin Converting Enzym Inhibitor (ACEI) merupakan golongan
obat yang sering digunakan untuk pengibatan hipertensi dan gagal jantung.
Obat ini juga dapat mengurangi proteinuria pada sindrom nefrotik dan
nefropati DM. ACE Inhibitor dibedakan menjadi 2 kelompok yaitu 1) yang
bekerja langsung, contohnya kaptopril dan lisinopril; 2) prodrug, contohnya
enalapril, quinapril, perindopril, ramipril, silazapril, benazepril, fosinopril, dan
lainnya. Kelompok obat prodrug ini diubah menjadi bentuk aktif di dalam
tubuh (Nafrialdi, 2012).
Mekanisme kerja ACE Inhibitor yaitu menghambat enzim konversi
peptidil dipeptidase yang menghidrolisis angiotensin I menjadi angiotensin II
dan menonaktifkan bradikinin, sehingga terjadi vasodilatasi dan penurunan
sekresi aldosteron. Secara umum vasodilatasi dapat menurunkan tekanan darah,
sedangkan berkurangnya aldosteron dapat menyebabkan retensi air, natrium,
dan retensi kalium. Vasodiator kuat dapat merangsang pelepasan nitrat oksida
dan prostasiklin (Katzung, 2017). ACE Inhibitor berperan dalam menghambat
pembentukan angiotensin II secara lokal di endotel. Pengurangan produksi
angiotensin II oleh ACE Inhibitor dapat mengurangi sekresi aldosteron di
koteks adrenal, menyebabkan terjadinya ekskresi air dan natrium, sedangkan
pada kalium mengalami retensi sehingga dapat terjadi hiperkalemia terutama
pada gangguan fungsi ginjal (Nafrialdi, 2012).
Peran ACE Inhibitor di ginjal menyebabkan vasodilatasi arteri renalis
sehingga dapat meningkatkan aliran darah ginjal dan dapat memperbaiki laju
filtrasi glomerulus. Pada sirkulasi glomerulus, ACE Inhibitor dapat
menyebabkan vasodilatasi dominan di arteriol eferen sehingga menurunkan
tekanan intraglomerular. Hal ini dapat dimanfaatkan sebagai pengurangan
proteinuria pada nefropati diabetik, memperlambat progresivitas nefropati
diabetik serta dapat menstabilkan fungsi ginjal (Katzung, 2017).

39
ACE Inhibitor sebagai enzim yang secara langsung memblokir angiotensin
I menjadi angitensin II. Selain itu, ACE Inhibitor atau ARB dapat
meningkatkan penekanan pada sistem renin-angiotensin-aldosteron (SRAA)
(Dipiro et al, 2015). Sistem renin-angiotensin-aldosteron memiliki peran dalam
pengaturan tekanan darah dan volume cairan tubuh. Saat terjadi penurunan
volume darah, reaksi pertama tubuh yaitu meningkatnya sekresi renin dari sel
jukstaglomeruler di arteriol aferen ginjal (Nafrialdi, 2012).
Renin merupakan enzim aspartil protease yang secara spesifik
mengkatalisis pelepasan hidrolitik dekapeptida angiotensin I dari
angiotensinogen. Awalnya enzim ini disintesis sebagai prapromolekul yang
diproses menjadi prorenin yang kemudian menjadi renin aktif, renin aktif ialah
glikoprotein yang terdiri dari 340 asam amino. Dalam sirkulasi, renin berasal
dari ginjal. Renin disintesis oleh sel-sel jukstaglomeruler di ginjal dan sebagai
penentu (rate limiting step) aktivitas sistem renin-angiotensin-aldosteron.
Pelepasan renin dari korteks ginjal distimulasi oleh penurunan pada tekanan
arteri ginjal, stimulasi saraf simpatis, dan penurunan penyaluran natrium atau
peningkatan konsentrasi natrium di tubulus distal ginjal. renin bekerja pada
angiotensinogen untuk menginaktifkan prekursor dekapeptida angiotensin I,
kemudian angiotensin I diubah oleh ACE endotel menjadi vasokonstriktor
arteri oktapeptida angiotensin II, selanjutnya diubah menjadi angiotensin III di
kelenjar adrenal. Angiotensin II dan III dapat menstimulasi pelepasan
aldosteron. Angiotensin berperan dalam mempertahankan resistensi vaskuler
yang tinggi pada keadaan hipertensi dengan aktivitas renin plasma yang tinggi
misal stenosis arteri ginjal, beberapa jenis penyakit ginjal intrinsik, hipertensi
maligna serta hipertensi esensial setelah peengobatan pembatasan natrium,
diuretik, atau vasodilator (Katzung, 2017).
Berdasarkan penelitian (Ku et al., 2018) yang menggunakan metode CRIC
(Chronic Renal Insufficiency Cohort) dengan peserta sebanyak 3939, dengan
karakterisktik tertentu yaitu usia rata-rata 58 tahun, indeks massa tubuh rata-
rata 32 kg/m2, serta nilai GFR rata-rata 43 ml/ menit/ 1,73 m2. Penelitian ini
menunjukkan bahwa penggunaan ACEI hanya digunakan pada pasien CKD
stadium awal, dengan prevalensi pada CKD stadium 3 sebesar > 75% yang

40
menggunakan ACEI namun, pada CKD stadium 5 penggunaannya turun
menjadi 37%. Dengan ini membuktikan bahwa penggunaan ACEI menurun
serta tidak lazim pada CKD stadium 4 dan 5, maka dari itu ACEI
direkomendasikan sebagai pengobatan lini pertama.
Gambar 2.7. Mekanisme aksi obat dalam memblok RAAS (Katzung, 2017).
Sebagian besar metabolisme ACE Inhibitor terjadi di hati, kecuali
lisinopril yang tidak mengalami metabolisme di hati. Pada umumnya eliminasi
ACE Inhibitor terjadi di ginjal, kecuali fosinopril yang mengalami eliminasi di
ginjal dan bilier. Dibawah ini terdapat beberapa obat golongan ACE Inhibitor
beserta farmakokinetiknya (Nafrialdi, 2012).
Tabel II.10 Obat golongan ACE Inhibitor dan farmakokinetiknya (Nafrialdi,
2012).
Sediaan Prodrug Metabolit
aktif
Metabolisme
di hati Eliminasi
Kaptopril Tidak - + Ginjal
Lisinopril Tidak - - Ginjal
Perindopril Ya Perindoprilat + Ginjal
Enalapril Ya Enalaprilat + Ginjal
Ramipril Ya Ramiprilat + Ginjal

41
Quinapril Ya Quinaprilat + Ginjal
Silazapril Ya Silazaprilat + Ginjal
Benazepril Ya Benezeprilat + Ginjal
Fosinopril Ya Fosinoprilat + Ginjal +
bilier
2.7.1. Kaptopril
Gambar 2.7.1. Struktur kimia kaptopril (Drugbank, 2020).
Kaptopril adalah ACE Inhibitor yang pertama ditemukan dan sering
digunakan untuk pengobatan hipertensi ringan sampai sedang (biasanya
dikombinasi dengan obat lain, seperti diuretik tiazid) maupun hipertensi berat
(Nafrialdi, 2012). Selain itu, kaptopril merupakan inhibitor kuat dan kompetitif
dari ACE Inhibitor. Enzim ini bekerja dengan mengkonversi angiotensin I
menjadi angiotensin II (Drugbank, 2020). Obat ini berfungsi dapat menurunkan
tekanan darah, mengurangi reabsopsi natrium, memperbaiki cedera ginjal, dan
menekan peradangan ginjal (James et al, 2014).
Kaptopril dapat menyebabkan peningkatan aktivitas renin plasma, hal ini
mungkin disebabkan oleh hilangnya inhibisi umpan balik yang dimediasi oleh
angiotensin II pada pelepasan renin atau stimulasi mekanisme refleks melalui
baroreseptor (Drugbank, 2020). Pada pemberian oral kaptopril direabsorpsi
dengan bioavaibilitas 70-75%. Apabila pemberian kaptopril diberikan secara
bersamaan dengan makanan akan mengurangi reabsorpsi sekitar 30%, maka
dari itu obat ini diberikan 1 jam sebelum makan. Obat ini mengalami
metabolisme di hati, sedangkan eliminasinya melalui ginjal (Nafrialdi, 2012).

42
Dosis awal kaptopril untuk indikasi hipertensi yaitu 12,5 mg 2 kali sehari,
namun pada usia lanjut dosis yang diigunakan 6,25 mg 2 kali sehari; dosis
lazim 25 mg 2 kali sehari, dan dosis maksimum sebesar 50 mg 2 kali sehari.
Selain itu, dosis kaptopril pada nefropati diabetik yaitu 75-100 mg dalam dosis
terbagi, sedangkan pada gangguan ginjal berat, dosis awal 12,5 mg 2 kali
sehari (BPOM RI, 2015). Kaptopril memiliki kontraindikasi pada pasien
hamil, penyakit renovaskuler, stenosis aortik atau obstruksikeluarnya darah
dari jantung, dan hipersensitif terhadap ACE Inhibitor (BPOM RI, 2015).
Adapun efek samping yang sering ditimbulkan yaitu batuk kering yang
persisten, hipotensi, hiperkalemia, proteinuria, edema angioneurotik, gagal
ginjal akut, serta sekitar 10% pengguna kaptopril mengalami makulopapular
atau morbiliform yang bersifat reversibel pada penghentian obat atau dengan
pemberian antihistamin. Hal ini kemungkinan disebabkan oleh adanya gugus
sulfhidril (SH) pada kaptopril yang tidak dimiliki oleh ACE Inhibitor lainnya
(Nafrialdi, 2012).
2.7.2. Lisinopril
Gambat 2.7. Struktur kimia lisinopril (Drugbank, 2020).
Lisinopril dan kaptopril merupakan ACE Inhibitor yang tidak termasuk
prodrug. Lisinopril adalah obat golongan ACE Inhibitor yang sering digunakan
untuk pengobatan hipertensi, gagal jantung, dan infark miokard. Lisinopril
diindikasikan untuk pengobatan hipertensi pada pasien > 6 tahun, untuk
pengobatan infark miokard akut, serta sebagai terapi tambahan untuk gagal
jantung (Drugbank, 2020). Apabila pasien hipertensi sedang menggunakan
obat diuretik, sebaiknya dihentikan terlebih dahulu selama 2-3 hari sebelum
menggunakan lisinopril (BPOM RI, 2015).

43
Dosis awal lisinopril sebesar 10 mg dengan pemakaian 1 kali sehari,
kemudian dosis penunjang lazim sebesar 20 mg 1 kali sehari, dan dosis
maksimal sebesar 80 mg 1 kali sehari. Apabila tekanan darah sistolik kurang
dari 100 mmHg, maka untuk sementara waktu dosis penunjang dikurangi
sampai 2,5 mg, dan juga hentikan pemakaian jika terjadi hipotensi yang
berkepanjangan (BPOM RI, 2015). Reabsorpsi lisinopril yaitu dengan
bioavaibilitas 25%. Absorpsi lisinopril tidak dipengaruhi oleh makanan.
Lisinopril tidak dimetabolisme dan tidak diekskresi. Eliminasi lisinopril sama
seperti ACE Inhibitor lainnya yaitu di ginjal (Drugbank, 2020).
2.7.3. Ramipril
Gambar 2.7.3. Struktur kimia ramipril (Drugbank, 2020).
Ramipril merupakan obat prodrug dari ACE Inhibitor. Dengan demikian,
obat ini diubah dalam bentuk metabolit aktif menjadi ramiprilat. Ramiprilat
dapat digunakan untuk pengobatan hipertensi, gagal jantung kongestif,
nefropati, infark miokard, stroke pada individu yang beresiko tinggi terhadap
kardiovaskuler, memperlambat perkembangan penyakit gagal ginjal pada
individu dengan hipertensi dan untuk mengurangi tingkat mortalitas
(Drugbank, 2020).
Tingkat absorpsi ramipril sekitar 50-60%, dengan bioavaibilitas ramipril
dan ramiprilat masing-masing 28% dan 44% (Drugbank, 2020). Ramipril
dimetabolisme di hati menjadi ramiprilat. Setelah dosis oral ramipril,
konsentrasi plasma puncak ramiprilat terjadi 2 sampai 4 jam. Ramipril
diekskresikan melalui urin 60% dan melalui feses 40%. Waktu paruh efektif
ramiprilat ialah 13 sampai 17 jam. Efek hemodinamik ramipril terlihat sekitar 1
sampai 2 jam dari dosis oral tunggal dan mencapai puncak sekitar 3 sampai 6
jam. Efek hemodinamik ini dapat bertahan selama 24 jam, hal ini yang dapat
memungkinkan pemberian dosis ramipril sekali sehari (Sweetman, 2014).

44
Dalam pengoban hipertensi, dosis awal yang diberikan yaitu 2,5 mg
sampai 5 mg satu kali sehari dengan pemberian secara oral atau 1,25 mg pada
individu dengan penggunaan diuretik atau yang berisiko hipotensi berat. Pasien
yang akan menggunakan ramipril dan masih menggunakan diuretik, sebaiknya
penggunaan diuretik dihentikan 2 sampai 3 hari sebelum memulai penggunaan
ramipril, dan dilanjutkan lagi jika perlu (Sweetman, 2014).
2.7.4. Enalapril
Gambar 2.7. Struktur kimia enalapril (Drugbank, 2020).
Enalapril merupakan prodrug dari metabolit aktif enalaprilat. Obat ini
digunakan untuk pengobatan hipertensi dan gagal jantung. Obat ini juga dapat
diberikan profilaksis pada pasien disfungsi ventrikel kiri asimptomatik untuk
menunda timbulnya gagal jantung simtomatik, dan juga untuk mengurangi
terjadinya iskemik jantung (Sweetman, 2014).
Absorpsi enalapril secara oral sekitar 60%, dengan konsentrasi plasma
puncak (C max) enalapril dapat dicapai dalam 1 jam setelah pemberian dosis
oral, sedangkan konsentrasi plasma puncak (C max) enalaprilat dapat dicapai 3
sampai 4 jam setelah pemberian dosis oral. Enalapril dimetabolisme di hati
menjadi enalaprilat. Enalaprilat terikat protein plasma sebesar 50 sampai 60%.
Enalaprilat diekskresikan dalam urin dan dalam feses. Waktu paruh efektif
enalapril sekitar 1 jam pada pasien dengan fungsi ginjal normal. Efek
hemodinamik enalaprilat mencapai puncak dalam waktu 1 sampai 4 jam, hal
ini dapat berlangsung sekitar 6 jam pada dosis yang telah dianjurkan
(Sweetman, 2014).
Dalam pengobatan hipertensi, dosis oral awal yang diberikan 5 mg satu
kali sehari. Apabila pasien menggunakan diuretik, maka dosis awal yang
disarankan 2,5 mg satu kali sehari. Pasien yang mengkonsumsi diuretik dan
akan mengkonsumsi enalapril sebaiknya, diuretik dihentikan 2 sampai 3 hari

45
sebelum pemakaian enalapril dimulai. Dosis pemeliharaan enalapril 10 mg
sampai 20 mg satu kali sehari, namun pada hipertensi berat dosis yang berikan
sebesar 40 mg (Sweetman, 2014).
2.7.5. Perindopril
Gambar 2.7.5. struktur kimia perindopril (Drugbank, 2020).
Perindopril adalah obat kelompok prodrug dari ACE Inhibitor. Perindopril
digunakan untuk pengobatan hipertensi, gagal jantung. Dan dapat mengurangi
risiko karciovaskuler pada pasien dengan penyakit jantung iskemik. Setelah
dosis oral, perindopril diabsorpsi cepat dengan bioavaibilitas 65-75 %.
Perindopril dimetabolisme di hati menjadi perindoprilat. Konsentrasi plasma
puncak perindopril terjadi 3 sampi 4 jam setelah dosis oralnya. Perindoprilat
sekitar 10 sampai 20% terikat protein plasma. Sebagian besar perindopril
diekskresikan melalui urin. Eliminasi perindoprilat adalah bipasik dengan
waktu paruh distribusi 5 jam dan waktu paruh eliminasi 25 sampai 30 jam atau
lebih, dengan kedua waktu paruh tersebut menunjukkan bahwa kemungkinan
adanya ikatan yang kuat dengan angiotensin-converting enzym (Sweetman,
2014).
Dalam pengobatan hipertensi, perindopril diberikan dengan dosis awal
sebesar 4 mg erbumin atau 5 mg garam arginin dengan pemakaian satu kali
sehari. Apabila pasien mempunyai indikasi lain seperti hipertensi renovaskular,
volume depletion, gagal jantung, ataupun hipertensi berat, maka dosis dapat
dikurangi menjadi 2 atau 2,5 mg dengan pemakaian satu kali sehari. Apabila
pasien menggunakan diuretik, maka harus dihentikan 2 atau 3 hari sebelum
penggunaan perindopril (Sweetman, 2014).

46
2.7.6. Quinapril
Gambar. 2.7.6. Struktur kimia quinapril (Drugbank, 2020).
Quinapril merupakan ACE Inhibitor yang digunakan dalam pengobatan
hipertensi dan gagal jantung. Efek hemodinamik quinapril terlihat 1 jam
setelah dosis oral tunggal, dan efek maksimum terjadi sekitar 2 sampai 4 jam.
Efek hemodinamik quinapril bertahan sekitar 24 jam (Sweetman, 2014).
Quinapril di dalam tubuh di ubah menjadi metabolit aktifnya yaitu
quinaprilat. Absorpsi quinapril dalam dosis oral sekitar 60%. Obat ini
dimetabolisme di hati menjadi quinaprilat. Puncak konsentrasi plasma
quinaprilat terjadi 2 jam dari dosis quinapril. Quinapril diekskresi melalui urin
dan feses setelah dosis oral. Sekitar 96% dosis intravena quinaprilat diekskresi
dalam urin, dengan waktu paruh yang efektif yaitu 3 jam. Farmakokinetik
quinapril dan quinaprilat dipengaruhi oleh gangguan ginjal dan hati. Dengan
demikian, dalam terapi dialisis terdapat beberapa efek terhadap ekskresi
quinapril atau quinaprilat (Sweetman, 2014).
Dalam pengobatan hipertensi dosis awal quinapril yang diberikan 10 mg
satu kali sehari. Jika pasien dengan gangguan ginjal, para lansia, maka dosis
awal yang direkomendasikan sebesar 2,5 mg dengan pemakaian satu kali
sehari. Jika pasien sedang menggunakan diuretik maka, perlu dihentikan 2 atau
3 hari sebelum oasien menggunakan quinapril, kemudian dilanjut lagi
pemakaian diuretik jika perlu (Sweetman, 2014).

47
2.7.7. Fosinopril
Gambar. 2.7.7. Struktur kimia fosinopril (Drugbank, 2020).
Fosinopril merupakan ACE Inhibitor yang digunakan untuk pengobatan
hipertensi dan gagal jantung. Efek hemodinamik fosinopril terlihat 1 jam
setelah dosis oral tunggal dan efek maksimum terjadi 2 sampai 6 jam. Efek
hemodinamik fosinopril berlangsung selama 24 jam. Fosinopril oral diberikan
dalam bentuk garam natriumnya (Sweetman, 2014).
Fosinopril berperan sebagai prodrug dari ACE Inhibitor. Absorpsi
fosinopril dalam dosis oral sekitar 36%. Obat ini dihidrolisis dengan cepat
menjadi fosinoprilat di mukosa gastrointestinal dan hati. Puncak konsentrasi
plasma fosinoprilat terjadi 3 jam setelah dosis oral fosinopril. Obat ini
diekskresi di dalam urin dan feses melalui empedu, dengan waktu paruh efektif
fosinoprilat sekitar 11,5 jam pada pasien hipertensi dan 14 jam pad apasien
gagal jantung.
Dalam pengobatan hipertensi, dosis awal fosinopril natrium diberikan 10
mg satu kali sehari. Sedangkan dosis pemeliharaan berkisar 10 sampai 40 mg
dengan pemakaian satu kali sehari. Jika pasien sedang menggunakan diuretik
maka, perlu dihentikan 2 atau 3 hari sebelum oasien menggunakan quinapril,
kemudian dilanjut lagi pemakaian diuretik jika perlu (Sweetman, 2014).

48
2.7.8. Benazepril
Gambar. 2.7.8. Struktur kimia benazepril (Drugbank, 2020).
Benazepril merupakan ACE Inhibitor yang digunakan dalam pengobatan
hipertensi dan gagal jantung. Efek hemodinamik benazepril terlihat 1 jam
setelah dosis oral tunggal, dan efek maksimum terjadi sekitar 2 sampai 4 jam.
Efek hemodinamik quinapril bertahan sekitar 24 jam. Benazepril diberikan
secara oral sebagai hidroklorida (Sweetman, 2014).
Benazepril di dalam tubuh di ubah menjadi metabolit aktifnya yaitu
benazeprilat. Absorpsi benazepril dalam dosis oral sekitar 37%. Obat ini
dimetabolisme di hati menjadi benazeprilat. Puncak konsentrasi plasma
benazeprilat terjadi 1 sampai 2 jam pada pasien dalam keadaan puasa dan 2
sampai 4 jam pada pasien dalam kondisi normal. Benazeprilat diekskresi dalam
urin, namun diekskresi dalam empedu sekitar 11 sampai 12 jam, dengan waktu
paruh yang efektif 10 sampai 11 jam. Eliminasi benazeprilat diperlambat pada
gangguan ginjal (Sweetman, 2014).
Dalam pengobatan hipertensi dosis awal benazepril hidroklorida yang
diberikan 10 mg satu kali sehari. Pada pasien dengan gangguan ginjal, dosis
awal yang diberikan 5 mg satu kali sehari. Jika pasien sedang menggunakan
diuretik maka, perlu dihentikan 2 atau 3 hari sebelum pasien menggunakan
quinapril, kemudian dilanjut lagi pemakaian diuretik jika perlu. Dosis
pemeliharaan benazepril hidroklorida yaitu 20 mg sampai 40 mg satu kali
sehari yang dapat diberikan dalam 2 dosis terbagi jika dengan dosis tunggal
tidak mencapai target yang diinginkan. Sedangkan pada pengobatan gagal
jantung, dosis awal benazepril hidroklorida yang diberikan 2,5 mg satu kali
sehari dan dosis maksimum sebesar 20 mg satu kali sehari (Sweetman, 2014).