Manjak vitamina b12 u djece – podcijenjena opasnost u ...
Transcript of Manjak vitamina b12 u djece – podcijenjena opasnost u ...

Manjak vitamina b12 u djece – podcijenjena opasnostu svjetlu novih spoznaja
Juras, Karin; Fumić, Ksenija; Ižaković, Senka; Pušeljić, Silvija; Čulić,Vida; Galić, Slobodan; Dasović Buljević, Andrea; Benjak, Vesna; Čolić,Ana; Huljev Frković, Sanda; ...
Source / Izvornik: Liječnički vjesnik, 2011, 133, 39 - 50
Journal article, Published versionRad u časopisu, Objavljena verzija rada (izdavačev PDF)
Permanent link / Trajna poveznica: https://urn.nsk.hr/urn:nbn:hr:239:801625
Rights / Prava: Attribution-NonCommercial-NoDerivatives 4.0 International
Download date / Datum preuzimanja: 2021-10-15
Repository / Repozitorij:
Repository UHC Osijek - Repository University Hospital Centre Osijek

39
MANJAK VITAMINA B12 U DJECE– PODCIJENJENA OPASNOST U SVJETLU NOVIH SPOZNAJA
VITAMIN B12 DEFICIENCY IN CHILDREN– UNDERESTIMATED DANGER IN THE LIGHT OF NEW KNOWLEDGE
KARIN JURAS, KSENIJA FUMI], SENKA I@AKOVI], SILVIJA PU[ELJI], VIDA ^ULI],SLOBODAN GALI], ANDREA DASOVI] BULJEVI], VESNA BENJAK, ANA ^OLI],
SANDA HULJEV FRKOVI], MILJENKA MARADIN, VLADIMIR SARNAVKA, KARMEN BILI],MATTHIAS BAUMGARTNER, IVO BARI]*
Deskriptori: Manjak vitamina B12 – etiologija, dijagnoza, komplikacije, farmakoterapija; Vitamin B12 – metabolizam; Pri-ro|eni poreme}aji metabolizma – genetika
Sa`etak. Vitamin B12 (kobalamin) ima dva aktivna oblika, adenozilkobalamin i metilkobalamin, koji imaju klju~nu ulogu u dvama va`nim metaboli~kim putovima u ljudi i njihov je manjak odgovoran za klini~ke te{ko}e u bolesnika. Kobalamin je nu`dan tijekom cijelog `ivota, no njegova dovoljna koli~ina posebno je bitna u fetalno i dojena~ko doba, kada je iznimno va`an za normalan rast i razvoj djeteta, kao i za normalan razvoj sredi{njega `iv~anog sustava. Zbog vrlo slo`enog prome-ta i metabolizma njegov se manjak mo`e o~itovati pri raznim priro|enim i ste~enim poreme}ajima. Klini~ka slika kojom se o~ituje manjak vitamina B12 obi~no je nespecifi~na, nosi velik rizik od trajnih posljedica za bolesnika, a naj~e{}e se vrlo jednostavno lije~i ako se na vrijeme prepozna. U Republici Hrvatskoj poreme}aji metabolizma kobalamina u djece prerijet-ko se otkrivaju. Zato je cilj ovog rada skrenuti pozornost na nove spoznaje o metabolizmu kobalamina, prikazati bolesnike s tipi~nim klini~kim tijekom i laboratorijskim nalazima te dati smjernice za brzo dijagnosticiranje i lije~enje poreme}aja vitamina B12 u djece.
Descriptors: Vitamin B12 deficiency – etiology, diagnosis, complications, drug therapy; Vitamin B12 – metabolism; Meta-bolism, inborn errors – genetics
Summary. Vitamin B12 (cobalamin) has two active forms, adenosylcobalamin and methylcobalamin which have a key role in two important metabolic pathways in humans and their deficiency is responsible for clinical problems. Cobalamin is es-sential during whole life, but its sufficient amount is extra important in fetal and neonatal period, when it is essential for normal child growth and development as well as for normal development of the central nervous system. Because of very complex transport and metabolism, its deficiency can be manifested in numerous congenital and acquired disorders. Vita-min B12 deficiency mostly has non-specific clinical features, it carries a great risk of permanent consequences, but most frequently it is easily curable if diagnosed on time. In Croatia cobalamin deficiency in children has been diagnosed too rarely. Accordingly, the aim of this paper is to point to the recently gained knowledge on cobalamin metabolism, present typical case reports and to provide guidelines for rapid and proper diagnostic and therapeutic approach.
Lije~ Vjesn 2011;133:39–50
* Medicinski fakultet Sveu~ili{ta u Zagrebu, Zagreb (Karin Juras, dr. med.), Klinika za pedijatriju Medicinskog fakulteta Sveu~ili{ta u Za gre-bu, Klini~ki bolni~ki centar Zagreb (mr. sc. Slobodan Gali}, dr. med.; mr. sc. Andrea Dasovi} Buljevi}, dr. med.; prim. mr. sc. Vesna Benjak, dr. med.; Sanda Huljev Frkovi}, dr. med.; mr. sc. Vladimir Sarnavka, dr. med.; prof. dr. sc. Ivo Bari}, dr. med.), Klini~ki zavod za laboratorijsku dijagnostiku Medicinskog fakulteta Sveu~ili{ta u Zagrebu, Klini~ki bolni~ki centar Zagreb (prof. dr. sc. Ksenija Fumi}, spec. med. biokem.; Karmen Bili}, spec. med. biokem.), Klinika za pedijatriju Klini~kog bolni~kog centra u Osijeku (Senka I`akovi}, dr. med.; mr. sc. Silvija Pu{elji}, dr. med.), Kli-nika za pedijatriju Klini~kog bolni~kog centra u Splitu, Split (doc. dr. sc. Vida ^uli}, dr. med.), Zavod za neonatologiju i intenzivno lije~enje, Klinika za `enske bolesti i porode Medicinskog fakulteta Sveu~ili{ta u Zagrebu, Klini~ki bolni~ki centar Zagreb (Ana ^oli}, dr. med.), Odjel za laborato rijsku dijagnostiku Op}e bolnice u Karlovcu, Karlovac (mr. sc. Miljenka Maradin, spec. med. biokem.), University Children’s Hospital – University of Zürich, Division of Metabolism, CH-8032 Zürich, [vi-carska (prof. dr. sc. Ma tthias Baumgartner, dr. med.)Adresa za dopisivanje: Prof. dr. sc. I. Bari}, Zavod za bolesti metabolizma, Referentni centar Ministarstva zdravstva i socijalne skrbi Republike Hrvat-ske za medicinsku genetiku i metaboli~ke bolesti djece, Klinika za pedija-triju Medicinskog fakulteta Sveu~ili{ta u Zagrebu, Klini~ki bolni~ki centar Zagreb, Ki{pati}eva 12, Rebro, 10000 Zagreb, e-mail: ibaricºkbc-zagreb.hrPrimljeno 17. lipnja 2010., prihva}eno 28. lipnja 2010.
Nove spoznaje i va`nost manjka vitamina B12za zdravlje stanovni{tva
Manjak vitamina B12 (kobalamina) ~est je u svim dobnim skupinama, a rizi~ne skupine ~ine stariji ljudi, vegetarijanci, trudnice, novoro|en~ad i dojen~ad hranjena samo maj~inim mlijekom, te bolesnici s bubre`nim i gastrointestinalnim bo-lestima.1 Simptomi i znakovi kojima se o~ituje obi~no su vrlo nespecifi~ni i nerijetko te{ko prepoznatljivi. Ve}inom se lako lije~e, a nelije~eni mogu zavr{iti ireverzibilnim po-sljedicama.2–5 Za vitamin B12, kao i za klini~ke, hematolo{ke i neurolo{ke poreme}aje koje mo`e izazvati njegov nedosta-tak zna se unatrag 80-ak godina. Posljednjih su godina ot-kriveni novi receptori, enzimi i druge bjelan~evine i geni uklju~eni u apsorpciju, prijenos i unutarstani~ni metaboli-zam kobalamina. To je pridonijelo boljemu shva}anju pore-me}aja vezanih uz funkcionalni manjak kobalamina (naziv koji se rabi za manjak njegovih aktivnih oblika) i otkri}u novih bolesti na slo`enom putu od apsorpcije vitamina B12 do stvaranja njegovih aktivnih oblika unutar stanice: adeno-
PreglediReviews

40
K. Juras i sur. Manjak vitamina B12 u djece Lije~ Vjesn 2011; godi{te 133
zilkobalamina i metilkobalamina.6,7 Otkriveno je da je najra-niji i zato najbolji biljeg u dijagnostici manjka zaliha koba-lamina, kao i pra}enju u~inka lije~enja, holotranskobalamin, dok je koncentracija ukupnog kobalamina u plazmi vrlo neosjetljiv i nespecifi~an biljeg.1 Metilmalonska kiselina i homocistein najneposredniji su pokazatelji manjka njegovih aktivnih oblika, tj. metaboli~kih posljedica njegova manjka koje su ~esto klini~ki prepoznatljive. Podaci koji zabrinja-vaju govore da oko 6% ljudi starijih od 60 godina ima nisku koncentraciju kobalamina u plazmi (< 148 pmol/L), a 20% ih ima grani~no nisku koncentraciju (148–221 pmol/L). Vode}i uzrok manjka kobalamina u starijih ljudi je malap-sorpcija kobalamina vezanoga za bjelan~evine hrane zbog visoke u~estalosti atrofi~noga gastritisa u starijoj populaciji. Prehrambeni manjak kobalamina zbog nekonzumiranja hra-ne `ivotinjskog podrijetla, koja je najve}i izvor vitamina B12, me|u vode}im je uzrocima manjka kobalamina u mla-|ih odraslih i siroma{nih ljudi.8 Klini~ka i laboratorijska o~itovanja manjka kobalamina u odraslih su umor, osjetna neuropatija, atrofi~ni glositis, makrocitoza ili hipersegmen-tacija neutrofila, funikularna mijeloza, hemoliti~ka anemija i pancitopenija. Depresija, senilnost, Alzheimerova bolest, mo`dani udar i Parkinsonova bolest tako|er su povezani s manjkom kobalamina. To se obja{njava hipometilacijskom hipotezom koja pretpostavlja da zbog manjka kobalamina i sukladno tomu njegova aktivnog oblika metilkobalamina dolazi do smanjene funkcije metionin sintetaze. Posljedica su povi{enja homocisteina i S-adenozilhomocisteina, a sni-`enja metionina i S-adenozilmetionina ~ime se sni`ava omjer S-adenozilmetionin/S-adenozilhomocistein (metila-cijski indeks) i remeti metilacija brojnih va`nih spojeva.9,10 Istra`ivanja su pokazala da ~ak 20% trudnica, ~ija je trud-no}a uredna, ima manjak vitamina B12
11–16 te da su koncen-tracije kobalamina u ro|enog djeteta izravno ovisne o kon-centracijama kobalamina u majki tijekom trudno}e.12 Kli-ni~ke manifestacije kojima se o~ituje manjak kobalamina na ishod trudno}e jesu poreme}aj razvoja neuralne cijevi u djeteta,13–16 preuranjeni porod17 i unutarmaterni~ni zastoj ra-sta djeteta.18,19 U razvijenim zemljama usmjerena je pa`nja na mogu}i manjak vitamina B12 u dojene djece i sve se ~e{}e otkrivaju majke i njihova dojen~ad s manjkom vitamina B12. Nutritivni manjak kobalamina naj~e{}i je uzrok njegova manjka u djece, a posebno se u~estalo javlja u dojene dje-ce.20–22 O~ituje se anemijom, razdra`ljivo{}u, nenapredova-njem, zaostatkom u razvoju i razli~itim, katkad ireverzibil-nim, neurolo{kim simptomima i znakovima.23 Prevencija i rano lije~enje su nu`ni ako `elimo izbje}i trajne neurolo{ke posljedice u djeteta.24 Danas se u okviru programa novoro-|ena~kog probira (skrininga) u nekim zemljama tandem-skom spektrometrijom masa mogu otkriti novoro|en~ad s nutritivnim manjkom kobalamina ve} u tre}em danu `ivota, nalazom povi{ene koncentracije propionilkarnitina (C3) koji se mjeri radi otkrivanja propionske i metilmalonske aci-demije, a bude povi{en i u slu~aju manjka kobalamina. Ipak, zbog mogu}ih la`no negativnih rezultata skrininga ne mo`e se isklju~iti manjak kobalamina mjere}i samo koncentraciju C3, ve} bi se morala mjeriti i koncentracija metilmalonske kiseline i homocisteina u plazmi.23 To je me|utim iz teh-ni~kih razloga neizvedivo u sve djece. Za razliku od nutri-tivnog manjka priro|eni poreme}aji metabolizma kobala-mina ~esto se o~ituju te{kom klini~kom slikom, nerijetko i akutnim, za `ivot opasnim metaboli~kim krizama.
Iskustva u na{oj Klinici pokazala su da se u na{oj zemlji nutritivnom manjku kobalamina, pa i ostalim uzrocima funkcionalnog manjka kobalamina u djece posve}uje nedo-
voljno pozornosti. Stoga je cilj ovog rada upozoriti na va`-nost manjka vitamina B12 u djece, istaknuti brojne nove spoznaje vezane uz metabolizam vitamina B12 i dati smjer-nice za pravodoban i brz dijagnosti~ki i terapijski pristup manjku kobalamina u djece. U tu svrhu prikazat }emo i nekoliko pou~nih primjera na{ih bolesnika, kako onih s pri-ro|enim poreme}ajima prometa i metabolizma vitamina B12 tako i tabli~no onih brojnijih s nutritivnim manjkom.
Apsorpcija, transport i unutarstani~ni metabolizam vitamina B12 s pregledom nasljednih poreme}aja
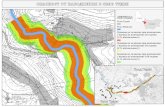
Apsorpcija, transport i unutarstani~ni metabolizam vita-mina B12 vrlo su slo`eni procesi (vidi sliku 1). Poreme}aj u bilo kojem dijelu tih procesa mo`e izazvati manjak jednoga ili obaju aktivnih oblika – adenozilkobalamina i metilkoba-lamina i posljedi~ne klini~ke te{ko}e. Apsorpcija vitamina B12 po~inje nakon uno{enja kobalamina hranom ve} u usti-ma. Ve}i dio vitamina B12 vezan je za bjelan~evine hrane te u takvu obliku dolazi do `eluca, a manji dio slobodnog (ne-vezanog) vitamina B12 apsorbira se kroz sluzni~nu membra-nu te zaobilazi `eludac i potrebu za kiselim pH. U kiselom `elu~anome mediju i pod djelovanjem pepsina kobalamin se osloba|a od bjelan~evina hrane te se brzo ve`e za prijeno-snu bjelan~evinu, glikoprotein haptokorin (HC) ili transko-balamin I ili R-veza~, koja u prisutnosti kiseloga medija posjeduje visok afinitet za kobalamin.9 HC lu~e `lijezde sli-novnice i `elu~ana sluznica u prisutnosti slobodnog koba-lamina u `elucu.25 Kao takav, kompleks kobalamin-HC pu-tuje do tankog crijeva gdje se kobalamin pod djelovanjem proteoliti~nih enzima gu{tera~e i alkalnog medija odvaja od HC-a te se ve`e za `elu~ani glikoprotein, intrinzi~ni ~imbe-nik (IF, engl. intrinsic factor) ili S-veza~. IF lu~e parijetalne `elu~ane stanice i gu{tera~a u prisutnosti hrane te kao odgo-vor na izlu~ivanje histamina, gastrina i pentagastrina. HC ima afinitet i za kobalaminske analoge (naprimjer za kobi-namid), dok IF ponajprije ve`e kobalamin i ima slab afinitet za kobalaminske analoge.6 Kompleks kobalamin-IF otporan je na daljnju razgradnju. Postoji rijetka bolest zbog pri-ro|enog manjka IF-a (kongenitalna perniciozna anemija), koja se o~ituje zaostatkom u rastu, povra}anjem, proljevom ili opstipacijom, anoreksijom, razdra`ljivo{}u te katkad he-patosplenomegalijom ve}inom u prvim godinama ̀ ivota, no mo`e katkad ostati neprepoznata do odrasle dobi. U toj bo-lesti niska je koncentracija kobalamina u plazmi i postoji megaloblasti~na anemija. Normalna je kiselost `elu~ane sluznice i nema protutijela na IF. Opisano je manje od 100 bolesnika.26–29
Oko 1% slobodnog kobalamina apsorbira se pasivnom difuzijom kroz terminalni ileum. Zato ima smisla davati ko-balamin na usta u velikim koli~inama u stanjima poreme-}enog izlu~ivanja IF-a.30,31 Kobalamin u kompleksu s IF-om putuje do distalnog ileuma. Tu se na enterocitima nalazi specifi~ni kompleks receptora »cubam« koji se sastoji od glikoproteina »kubilina« (engl. cubilin) i bjelan~evine »am-nionles« (engl. amnionless*) koji imaju afinitet za kompleks kobalamin-IF.32,33 Uz njih se jo{ na enterocitima nalazi bje-lan~evina (receptor) »megalin« (engl. megalin/gp330/LRP--2-receptor) ~ija je uloga vjerojatno odr`avanje postojanosti kompleksa »cubama«.34 Ona nije uklju~ena u apsorpciju vi-tamina B12 u crijevu, a odgovorna je za reapsorpciju kom-pleksa kobalamin-transkobalamin u bubrezima.35,36 Me|u-djelovanje kompleksa »cubama« i »megalina« ovisno je o
* Naziv potje~e od razvojnog poreme}aja koji se u embrijima pokusnih `ivotinja o~ituje u fazi gastrulacije (manjkom amniona u fazi gastrulacije).

41
Lije~ Vjesn 2011; godi{te 133 K. Juras i sur. Manjak vitamina B12 u djece
kalciju. Megalin jo{ posjeduje i ligand, »bjelan~evinu po-vezanu s receptorom« (engl. receptor-associated protein (RAP)).37–39 Iako klju~ni za apsorpciju kobalamina, »mega-lin« i »kubilin« nisu receptori specifi~ni samo za kobala-min, jer su i receptori za hemoglobin, albumin, transferin i druge bjelan~evine.40 Postoji bolest zbog poreme}aja kom-pleksa receptora »cubam«-megaloblasti~na anemija 1 ili Imerslund-Gräsbeck-Najmanov sindrom. To je rijetka bo-lest koja se o~ituje megaloblasti~nom anemijom u kasnom djetinjstvu i proteinurijom, a katkad i neurolo{kim simpto-mima. Dosad je opisano oko 250 bolesnika, a prvog je opi-sao 1952. godine hrvatski pedijatar Emil Najman.26,41,42 U dojena~ko doba apsorpcija kobalamina nije posredovana samo IF-om, ve} ulogu ima i HC koji se nalazi u mlijeku majke. On potpoma`e ve`u}i se za crijevne receptore, za koje se vjeruje da postoje u vrijeme dok jo{ sustav IF u dojen~eta nije sazrio.43
Kompleks kobalamin-IF ve`e se za kompleks receptora »cubam« i otprema u citoplazmu enterocita gdje se proce-som proteolize kobalamin osloba|a iz kompleksa i predaje u portalnu cirkulaciju u slobodnom obliku. Ondje se 80% kobalamina ve`e za HC, a ostalih 20% za neglikoziranu bjelan~evinu transkobalamin II (TC). TC proizvode endo-
telne stanice krvnih `ila.44 Ve}inom se u cirkulaciji TC na-lazi u apo-obliku (slobodni transkobalamin). Holo-TC je transkobalamin vezan za kobalamin, ima kratko poluvrije-me raspada, 1–2 sata, te se brzo mora unijeti u stanicu.6 Ve-zan za TC vitamin B12 prenosi se do svih stanica u tijelu, a vezan za HC samo do jetrenih stanica. To~na uloga HC-a jo{ se ne zna, a pretpostavlja se da bi mogao biti uklju~en u proces ~i{}enja toksi~nih analoga kobalamina, ili bi mogao {tititi metilkobalamin od fotolize.45 Postoje priro|eni manjci TC-a i HC-a. Priro|eni manjak TC-a rijetka je bolest koja se o~ituje u ranom djetinjstvu zaostajanjem u rastu, megalo-blasti~nom anemijom i katkad neurolo{kim simptomima. Opisano je manje od 50 bolesnika. Budu}i da je ve}ina ko-balamina u cirkulaciji vezana za haptokorin, koncentracija kobalamina u krvi je normalnih vrijednosti.26,46 Priro|eni manjak HC-a rijedak je poreme}aj, za koji nije sigurno o~ituje li se klini~ki. Kobalamin u serumu je nizak, a opisa-no je tek nekoliko bolesnika.46
U stanice holo-TC ulazi nakon vezanja za receptore »me-galin« (LRP2) i TC-Cbl37,47 te endocitozom ulazi u stani~ne lizosome. Unutarstani~ni metabolizam kobalamina sastoji se od sedam koraka do stvaranja kofaktora adenozilkobala-mina i metilkobalamina.7 Najvi{e kobalamina unutar sta nice
CBL – kobalamin/cobalamin, KOMPLEKS CBL-HC/CBL-HC COMPLEX – kobalamin vezan za haptokorin/cobalamin bound to haptocorin, IF – intrinzi~ni ~imbenik/in-trinsic factor, KOMPLEKS CBL-IF/CBL-IF COMPLEX – kobalamin vezan za intrinzi~ni ~imbenik/cobalamin bound to intrinsic factor, KOMPLEKS OHCBL-TCII/OHCBL--TCII COMPLEX – hidroksokobalamin vezan za transkobalamin II/hydroxocobalamin bound to transcobalamin II, RECEPTOR CBL-TCII/CBL-TCII RECEPTOR – recep-tor za kompleks kobalamina-transkobalamina II/cobalamin-transcobalamin II receptor, MS – metionin sintaza/methionine synthase, THF – tetrahidrofolat/tetrahydrofo-late, 5-metil-THF/5-methyl-THF – 5-metiltetrahidrofolat/ 5-methyltetrahydrofolate.
Slika 1. Promet i metabolizam kobalaminaFigure 1. Transport and metabolism of cobalamin
CBL UNESEN HRANOMDIETARY CBL
CBL-PROTEINI HRANECBL-DIETARY PROTEINS
KOMPLEKS CBL-IFCBL-IF COMPLEX
KOMPLEKSOHCBL-TCIIOHCBL-TCIICOMPLEX
OHCBL-TCII(proteoliza/proteolysis)
HIDROLIZA/HYDROLYSIS
SLOBODNI CBLFREE CBL
SLOBODNI CBLFREE CBL
KOMPLEKS CBL-HCCBL-HC COMPLEXPROTEAZE (gu{tera~a)
PROTEASES (pancreas)
IF (parijetalne stanice)IF (parietal cells)
SLOBODNI CBLFREE CBL
PROTEOLIZAPROTEOLYSIS
TRANSKOBALAMINHAPTOKORINTRANSCOBALAMINHAPTOCORIN
KOMPLEKS CBL-HC(hepatociti)CBL-HC COMPLEX(hepatocytes)
tanko crijevosmall intestine
enterocitienterocytes
SLOBODNI CBLFREE CBL
HAPTOKORIN (`lijezde slinovnice)HAPTOCORIN (salivary glands)
5-metil-THF5-methyl-THF
homocisteinhomocysteine
mutazamutase
mitohondrijmitochondrion
citoplazmacytoplasm
lizosomlysosome
RECEPTOR CBL-TCII
CBL-TCII RECEPTOR
endo
citoz
a
endo
cyto
sis
sukc
inil-
CoA
succ
inyl
-CoA
met
ilmal
onil-
CoA
met
hylm
alon
yl-C
oA
ADENOZILKOBALAMINADENOSYLCOBALAMIN
METIL--KOBALAMINMETHYL--COBALAMIN
THFmetioninmethionine
MS
cblF
cblC
cblD
cblA
cblB
cblE
cblG
cblD CBL2+
CBL2+
CBL1+
OHCBL3+
CBL2+
RECEPTOR CUBILIN-AMNIONLESSCUBILIN-AMNIONLESS RECEPTOR

42
K. Juras i sur. Manjak vitamina B12 u djece Lije~ Vjesn 2011; godi{te 133
nalazi se u obliku adenozilkobalamina, ne{to manje u obliku hidroksokobalamina, a najmanje u obliku metilkobalami-na.6 Nasljedne bolesti zbog poreme}ene unutarstani~ne sin-teze kofaktora – metilkobalamina i adenozilkobalamina obu-hva}aju sedam razli~itih poreme}aja (cblA, cblB, cblC, cblD ili cblH, cblE, cblF i cblG). Mogu biti uzrokovane ne-dostatkom obaju kofaktora ili izoliranim manjkom jednoga od njih. Posljedi~no nalazimo povi{ene vrijednosti homoci-steina i/ili metilmalonske kiseline. Homocistein bude povi-{en kada postoji manjak metilkobalamina koji je kofaktor metionin sintaze, pa je ometena remetilacija homocisteina u metionin, a metilmalonska kiselina bude povi{ena kad po-stoji manjak adenozilkobalamina koji je kofaktor metilma-lonilkoenzim A mutaze, enzima koji metilmalonilkoenzim A pretvara u sukcinilkoenzim A. Bolesti cblF, cblC i neki oblici cblD-a o~ituju se kombiniranom homocistinurijom i metilmalonskom acidurijom, bolesti cblE, cblG i neki oblici cblD-a izoliranom homocistinurijom, a bolesti cblA, cblB i neki oblici cblD-a (cblH) izoliranom metilmalonskom aci-durijom.
U lizosomima se kobalamin osloba|a od transkobalami-na procesom proteolize i otpu{ta u citoplazmu u slobodnom obliku (trovalentni kobalamin – Cbl3+). Ako taj korak nije mogu}, nastaje vrlo rijetka bolest cblF, koja se klini~ki o~i-tuje te{ko}ama u hranjenju, osipom, hipotonijom i zaostat-kom u razvoju. Karakteristi~no se u fibroblastima nalazi povi{ena unutarstani~na koncentracija kobalamina.26
Pretpostavlja se da se u citoplazmi zbiva redukcija koba-lamina. Poreme}aji na ovoj razini uzrokuju bolest cblC koja je naj~e{}i nasljedni poreme}aj u metabolizmu kobalamina s do sada u svijetu opisanih oko 400 bolesnika. To~an poreme}aj koji uzrokuju mutacije odgovaraju}ega gena od-govorne za ovu bolest jo{ je nepoznat. Biokemijski se o~i-tuje metilmalonskom acidurijom i homocistinurijom, a kli-ni~ki naj~e{}e ve} u prvoj godini `ivota te{ko}ama u hra-njenju, letargijom, progresivnim neurolo{kim smetnjama, nekontroliranim pokretima tijela, konvulzijama i komom. Mo`e postojati te{ka pancitopenija ili anemija s megalobla-stima u ko{tanoj sr`i te retinopatija. Lije~i se metioninom, hidroksokobalaminom, betainom, L-karnitinom te prehra-nom s ograni~enom koli~inom bjelan~evina u razli~itim kombinacijama, ovisno o fazi bolesti, stanju bolesnika i la-boratorijskim nalazima.26,46
Bolest cblD nastaje ako postoji manjak kobalamin reduk-taze. Postoji vi{e varijanta, pa se mo`e o~itovati sa sva tri navedena biokemijska fenotipa. Klini~ki se o~ituje ili simp-tomima metilmalonske acidurije i/ili homocistinurije, odno-sno razli~itim razvojnim, hematolo{kim, neurolo{kim i me-taboli~kim simptomima, kao i akutnom metaboli~kom kri-zom.48
Dalje se u citoplazmi kobalamin redukcijskom metila-cijom s pomo}u reduktaze metionin sintaze (manjak tog enzima uzrokuje bolest cblE) pretvara u metilkobalamin, jedan od aktivnih oblika vitamina B12, koji je kofaktor me-tionin sintaze (manjak tog enzima uzrokuje bolest cblG).7,26 5-metil-tetrahidrofolat predaje metilnu skupinu kobalaminu te nastaje metilkobalamin, a 5-metil-tetrahidrofolat prelazi u tetrahidrofolat (THF). Metilkobalamin prenosi metilnu skupinu na homocistein. Iz homocisteina s pomo}u metio-nin sintaze nastaje metionin. Metilkobalamin u toj reakciji slu`i kao nosa~ metilne skupine i kao kofaktor metionin sin-tazi.49 Metionin se dalje pretvara u S-adenozilmetionin koji je najve}i donor metilnih skupina u organizmu (npr. za sin-tezu mijelina, DNA, RNA, bjelan~evina, fosfatidiletanola-mina, gvanidinoacetata, mioinozitola itd.). Omogu}uju}i metilaciju, tako|er utje~e na sintezu serotonina, noradrena-
lina i dopamina.7,31,50 THF sudjeluje u sintezi purina, odno-sno DNA. Poreme}aji cblG i cblE o~ituju se izoliranom homocistinurijom (bez metilmalonske acidurije). U klini~koj slici ve} u prvim mjesecima `ivota dominiraju megalo-blasti~na anemija s te{kim zaostatkom u razvoju, ataksija, atrofija mozga, konvulzije, nistagmus i sljepo}a. Koncentra-cija homocisteina u krvi je povi{ena, a koncentracija metio-nina normalna ili smanjena. Lije~e se hidroksokobalami-nom, folatima, betainom i L-metioninom.26,46
Jedan dio kobalamina ulazi u mitohondrij (aktivnom i pa-sivnom difuzijom preko odre|enih prijenosnika na vanjskoj i unutarnjoj membrani mitohondrija), gdje se prvo doga|a redukcija kobalamina s pomo}u mitohondrijske kobalamin reduktaze. Manjak tog enzima dovodi do bolesti cblA. Za-tim se kobalamin s pomo}u kobalamin adenoziltransferaze pretvara u adenozilkobalamin (tako|er aktivni oblik vitami-na B12), koji je kofaktor metilmalonil koenzim A mutaze. Manjak kobalamin adenoziltransferaze uzrokuje bolest cblB. Tim se procesom omogu}uje pretvaranje metilmalo-nil-CoA u sukcinil-CoA koji je sastavni dio Krebsova ciklu-sa potrebnog za stvaranje energije.7 Poreme}aji cblA i cblB o~ituju se izoliranom metilmalonskom acidurijom (tj. bez povi{enja homocisteina) naj~e{}e ve} u dojena~koj dobi. Dolazi do te{kih metaboli~kih kriza (vidi opise bolesnika). Krize se o~ituju povra}anjem, dehidracijom, tahipnejom, progresivnim poreme}ajem svijesti, hipotonijom i drugim neurolo{kim simptomima. Kasno prepoznate i/ili neade-kvatno lije~ene mogu zavr{iti smrtno. U laboratorijskim na-lazima obi~no se vide ketoacidoza, pancitopenija, hipera-moniemija, hiperglicinemija i ketonurija. Povi{ena je kon-centracija metilmalonske kiseline u krvi i urinu. Lije~e se ograni~enim unosom bjelan~evina te primjenom hidrokso-kobalamina i/ili adenozilkobalamina, L-karnitina, a po po-trebi i uno{enjem posebnih mje{avina aminokiselina bez onih iz kojih nastaje metilmalonska kiselina.26,46
Prikazi bolesnika s nasljednim poreme}ajimasinteze kobalamina
Bolesnik 1
Obiteljska anamneza, trudno}a i poro|aj bili su uredni. U dobi od {est dana djevoj~ica postaje uspavana, roditelji je ne uspijevaju probuditi za obrok. Pri primitku u `upanijsku bolnicu bila je somnolentna, tahidispnoi~na, tahikardna i mlohava. U laboratorijskim je nalazima prisutna te{ka me-taboli~ka acidoza (pH 7,07, pCO2 1,8 kPa, BE –26,6). Usprkos terapiji potpornim mjerama do{lo je do pogor{anja op}eg stanja i laboratorijskih nalaza, pa je djevoj~ica slje-de}eg dana premje{tena u Kliniku za pedijatriju Klini~koga bolni~kog centra u Zagrebu. Pri primitku je duboko sopo-rozna, tahidispnoi~na, generalizirano hipotoni~na, primitiv-ni i tetivni refleksi nisu se mogli izazvati. Laboratorijskim pretragama na{li smo pH 7,27, BE –7,6, amonijak 650 µmol/L (normalno <110), ketone u urinu (+), ukupni karni-tin 12,51 µmol/L (normalno 17,4–40,6), slobodni karnitin 1,0 µmol/L (normalno 10,1–21,0), izrazito povi{enu metil-malonsku kiselinu u urinu (2208 mmol/mol kreatinina; nor-malno 0–5) i serumu (22,5 µmol/L; normalno 0,08–0,57) i uredan ukupni homocistein. Zbog izrazito visokog amo-nijaka nakon primitka u~injena je eksangvinotransfuzija te je ordiniran natrijev benzoat. Zbog sumnje na metaboli~ku bolest obustavljeno je hranjenje i dijete je stavljeno na infu-ziju 10%-tne glukoze s elektrolitima. Dijagnoza metilma-lonske acidurije postavljena je na temelju hitne analize or-ganskih kiselina u urinu ve} prvog dana, pa su u terapiju

43
Lije~ Vjesn 2011; godi{te 133 K. Juras i sur. Manjak vitamina B12 u djece
uvedeni L-karnitin (za bolje izlu~ivanje toksi~nih metaboli-ta) i cijanokobalamin (0,5 mg intramuskularno na dan). Nakon brzog pobolj{anja op}eg stanja zapo~elo se hraniti dijete uravnote`enom kombinacijom ograni~ene koli~ine pripravka adaptiranoga dojena~kog mlijeka, posebnog bes-proteinskog pripravka koji je nadomjestak za maj~ino mlijeko i mje{avine aminokiselina bez onih koje djevoj~ica ne mo`e razgraditi (IMTV-AM2® – bez izoleucina, metioni-na, treonina i valina). Tre}eg su dana uo~ene blaga leukope-nija i trombocitopenija. U suradnom inozemnom laborato-riju uo~ena je analizom enzimske aktivnosti – mjerenjem ugradnje propionata u fibroblaste – zna~ajno sni`ena ugrad-nja propionata bez vitamina B12, koja se normalizirala nakon davanja hidroksokobalamina. Aktivnost holomutaze (bez adenozilkobalamina) bila je sni`ena (25 pmol/min/mg pro-teina, normala 1354 pmol/min/mg proteina), a aktivnost ukupne mutaze (s adenozilkobalaminom) bila je urednih vrijednosti. Takav nalaz karakteristi~an je za poreme}aj sin-teze adenozilkobalamina, bolest cblA ili cblB. Djevoj~ica je danas u dobi od tri i pol godine, neupadljiva statusa i nor-malna pona{anja. Prima na dan peroralno oko 0,7 g/kg tje-lesne mase prirodnih bjelan~evina, 0,6 g/kg IMTV-AM2-a, L-karnitin 4×100 mg, 1 mg adenozilkobalamina 3× na tje-dan i intramuskularno 0,5 mg cijanokobalamina 1× na tje-dan. Uz to se izlu~ivanje metilmalonske kiseline u urinu kre}e u prihvatljivim okvirima, ispod 300 mmol/mol kreati-nina. Nema sistemske acidoze ni drugih biokemijskih ab-normalnosti.
Bolesnik 2
Djevoj~ica je ro|ena iz trudno}e komplicirane gestacij-skim dijabetesom. Poro|aj je protekao uredno. Roditelji su u krvnom srodstvu. U obiteljskoj anamnezi zna se za tri slu~aja iznenadne smrti u obitelji. Novoro|ena~ka dob pro-tekla je uredno, a u dojena~koj je dobi bolesnica ~esto povra}ala iz nepoznatih razloga. U dobi od tri godine prim-ljena je u nadle`nu bolnicu zbog vru}ice, povra}anja i akut-nog poreme}aja svijesti. Na|ene su metaboli~ka acidoza (pH 7,22, pCO2 1,4 kPa, bikarbonati 10 mmol/L, BE –24) i blaga hiperamoniemija (83,3 µmol/L). Unato~ terapiji uobi-~ajenim mjerama dolazi do pogor{anja djetetovog stanja, pa je sljede}eg dana premje{tena u Kliniku za pedijatriju Kli-ni~koga bolni~kog centra u Zagrebu. Pri prijmu je soporoz-
na, tahidispnoi~na i tahikardna. Laboratorijskim pretragama nalazimo pH 7,32, BE –16,8, amonijak 106,3 µmol/L (nor-malno <80), ketone u urinu (+++), ukupni karnitin 30,35 µmol/L (34,6–83,6), slobodni karnitin 1,69 µmol/L (nor-malno 24,3–62,5), masivno poja~ano izlu~ivanje metilma-lonske kiseline u urinu 26805 mmol/mol kreatinina (nor-malno 0), povi{enu metilmalonsku kiselina u serumu 41,83 µmol/L, metionin u serumu 7 µmol/L (normalno 15–45), vitamin B12 133 pmol/L (normalno 145–637, preciznije nor-malne vrijednosti vidi u raspravi) i ukupni homocistein 38,9 µmol/L (normalno <8,3–10,7). Dijagnoza metilmalonske acidurije postavljena je drugog dana boravka nakon hitne analize organskih kiselina u urinu. Tada je zapo~eta terapija L-karnitinom i vitaminom B12 (0,5 mg intramuskularno na dan) uz pove}an unos kalorija i poja~anu hidraciju otopi-nom 10%-tne glukoze s elektrolitima uz daljnju korekciju acidoze. Djevoj~ica se brzo oporavila na primijenjenu tera-piju. Pet dana nakon primitka smanjeno je izlu~ivanje metil-malonske kiseline u urinu na prihvatljiva 342 mmol/mol kreatinina. Zapo~inje se enteralnom prehranom s ograni-~enim unosom prirodnih bjelan~evina. U suradnom ino-zemnom laboratoriju uo~ena je analizom enzimske aktivno-sti – mjerenjem ugradnje propionata u fibroblaste – zna~ajno sni`ena ugradnja propionata bez vitamina B12 (1,09, nor-malno 3,5–24,4), koja se normalizirala nakon davanja hidro-ksokobalamina. Aktivnost holomutaze (bez adenozilkobala-mina) bila je sni`ena (185 pmol/min/mg proteina, normalno 906 pmol/min/mg proteina), a aktivnost ukupne mutaze (s adenozilkobalaminom) je bila urednih vrijednosti. Takav je nalaz upu}ivao na poreme}aje sinteze adenozilkobalamina cblA i cbl B. Definitivna dijagnoza poreme}aja cblA po-tvr|ena je genskom analizom. Na|eno je da je djevoj~ica homozigot za mutaciju c.592_595delACTG MMAA-gena. Danas je djevoj~ica u dobi od ~etiri i pol godine, sasvim uredna pona{anja i statusa. Prima na dan 0,75 g/kg tjelesne mase prirodnih bjelan~evina, L-karnitin 1,5 g (62,5 mg/kg tjelesne mase) i intramuskularno 0,5 mg cijanokobalamina 2× na tjedan.
Bolesnik 3
Obiteljska anamneza, trudno}a i poro|aj bili su uredni. Do dobi od pet i pol mjeseci dje~ak, ameri~kog dr`avljanstva, nije bolovao i normalno se razvijao. Tada je iz punog zdrav-
Slika 2. Kromatografija organskih kiselinau urinu u djeteta koje boluje od metilmalonske
acidemije (bolesnik 3 u tekstu). Valja uo~iti karakteristi~ni visoki i {iroki {iljak
metilmalonske kiseline ozna~en s MMA. Ostali ozna~eni {iljci tako|er su karakteristi~ni za
metaboli~ku krizu u metilmalonskoj acidemijiFigure 2. Chromatography of urine organic
acids in a child with methylmalonic acidemia (patient 3 in the text). Note typical high and
large peak of methylmalonic acid marked by MMA. Other marked peaks are also characteristic for metabolic crisis in
methylmalonic acidemia
Kratice/Abbrevations:(MeCit – metilcitrat/methylcitrate, ProGy – propionilglicin/propionylglicine, 3-OHPA – 3-hidroksipro-pionska kiselina/3-hydroxipropionic acid) udru`enu s ketoacidozom/associated with ketoacidosis (AcAc – acetoacetat/acetoacetate, 3-OHBA – 3-hidroksibutirat/3-hydroxibutyra te, 3-HIVA – 3-hidro-ksiizovalerijanska kiselina/3-hydroxiisovaleric acid) i laktacidozom/and lactacidosis (lac – laktat/lactate). IS1, IS2 – interni standardi/internal standards

44
K. Juras i sur. Manjak vitamina B12 u djece Lije~ Vjesn 2011; godi{te 133
lja, nakon prvog obroka sojina mlijeka, ~etiri puta obilno povratio. Postao je pospan i klonuo te je primljen u nadle`nu bolnicu u stanju te{ke dehidracije i nedijabeti~ke ketoacido-ze. Nakon tri dana hospitalizacije postavljena je sumnja na metaboli~ku bolest zbog te{ke ketoacidoze (pH 7,0, pCO2 1,98 kPa, BE –25, ketoni u urinu ++++) koja se nije oporav-ljala na uobi~ajeno lije~enje. Amonijak je bio 93,1 µmol/L (normalno <80), ukupni karnitin 24,29 µmol/L (normalno 34,6–83,6), slobodni karnitin 4,89 µmol/L (normalno 32,6–40,6). Do{lo je do pojave konvulzija koje su bile pra}ene apnoi~kim napadajima. Dje~ak je intubiran i premje{ten u Kliniku za pedijatriju Klini~koga bolni~kog centra u Zagre-bu. Pri primitku je reagirao samo na jake podra`aje, bio je hipotoni~an i mirisao je na aceton. Tada se u laboratorijskim nalazima izdvaja pH 7,4, BE –5,4, hemoglobin 96 g/L, u urinu jaka ketoza (++++) uz masivno poja~ano izlu~ivanje metilmalonske kiseline, amonijak 90 µmol/L te ukupni ho-mocistein 5,4 µmol/L. Hitna analiza organskih kiselina u urinu otkrila je da dijete boluje od metilmalonske acidurije (vidi sliku 2). Lije~enje je zapo~eto obustavljanjem bje-lan~evina u prehrani, hiperhidracijom (radi boljeg izlu~iva-nja {tetnih metabolita), visokim dozama cijanokobalamina (3× 0,5 mg intramuskularno), L-karnitinom i metronidazo-lom. Pove}ao se, ugljikohidratima i lipidima u koli~ini od 1,5 g/kg, unos kalorija na oko 100 kcal/kg na dan. Ubrzo se dje~akovo stanje pobolj{alo, nije vi{e imao apneja niti kon-vulzije, te je ekstubiran. Po~eo je tolerirati hranu na usta te je na `elju roditelja prevezen na daljnje lije~enje u inozem-stvo. U Sjedinjenim Ameri~kim Dr`avama postavljena je analizom fibroblasta kona~na dijagnoza nasljednog pore-me}aja sinteze adenozilkobalamina cblA. Danas je dje~ak u dobi od deset godina, potpuno uredna statusa. Prima na dan 1 mg hidroksokobalamina u mi{i} i na dijeti je s blagim ograni~enjem unosa bjelan~evina.
O nutritivnom manjkukao naj~e{}em uzroku nedostatka vitamina B12
u dje~joj dobi
Manjak aktivnih oblika vitamina B12 mo`e nastati zbog nedovoljnog uno{enja kobalamina hranom, u stanjima pove-}anih potreba za kobalaminom, zbog poreme}aja apsorpcije kobalamina, poreme}aja prijenosa kobalamina i poreme}aja njegova unutarstani~nog metabolizma.
Smanjen unos vitamina B12 hranom (nutritivni manjak vitamina B12) naj~e{}i je uzrok manjka kobalamina u djece, mla|ih odraslih i siroma{nih ljudi.8 Kod djece ga naj~e{}e vi|amo u dojen~adi koja je hranjena isklju~ivo maj~inim mlijekom. Posljednjih se godina sve vi{e isti~e va`nost pre-poznavanja manjka kobalamina u dojene djece zbog mo-gu}ih trajnih neurolo{kih posljedica koje mo`e izazvati.20–22 Koncentracija kobalamina u djeteta u dobi od 6 tjedana iz-ravno je ovisna o koncentraciji kobalamina u majke tijekom trudno}e.12 U istra`ivanjima se pokazalo da ~ak 20% trudni-ca ima niske koncentracije kobalamina u plazmi.11–16 U jed-noj studiji uo~eno je da koncentracija kobalamina ni`a od 185 pmol/L tijekom trudno}e pove}ava rizik od razvoja poreme}aja neuralne cijevi u djeteta.13 U na{oj populaciji je Slobodan Gali} u svome magistarskom radu pokazao da je manjak vitamina B12 u majki koje su rodile djecu s rascje-pom neuralne cijevi rizi~ni ~imbenik za ra|anje djece s tom anomalijom.51 Zbog navedenih razloga postoje preporuke da se majkama izmjeri koncentracija vitamina B12 prije pla-niranja trudno}e i da se poku{a koncentracija prije za~e}a dr`ati iznad 221 pmol/L.13 Visoka u~estalost manjka kobala-
mina u trudnica vi|a se u majki koje su vegetarijanke, a mo`e biti uzrokovana i malapsorpcijom, kao i pernicioznom anemijom u majki.52 Trudno}a i dojenje su stanja pove}anih metaboli~kih potreba, pa bi u tim stanjima trebalo unositi i ve}e koli~ine vitamina B12 od uobi~ajenih. Prema ameri~kim preporukama odrasli ljudi trebaju unositi na dan 2,4 µg ko-balamina, a trudnice ~ak do 6 µg na dan.53 U~estalost manjka vitamina B12 u djece ~e{}a je i zbog toga {to se u svijetu majke sve vi{e poti~u na dojenje, a ono dodatno pove}ava potrebe majki za kobalaminom.54,55
Vitamin B12 je nu`dan tijekom cijelog `ivota, no njegova dovoljna koli~ina posebno je va`na tijekom fetalnog `ivota i dojena~kog doba u kojima je nu`dan za normalan rast i razvoj djeteta, kao i za normalan razvoj sredi{njega ̀ iv~anog sustava.21 Klini~ka slika katkad mo`e biti izra`ena ve} u novoro|en~eta u dobi od tri tjedna, ali je naj~e{}e ne pre-poznamo zbog vrlo nespecifi~nih simptoma.12 Simptomi i laboratorijski znakovi koji upu}uju na manjak vitamina B12 u djeteta su razdra`ljivost, zaostatak u razvoju, konvulzije, nenapredovanje, hipotonija, mikrocefalija,56 pospanost, le-targija, odbijanje hrane, makrocitna anemija, trombocitope-nija, katkad i pancitopenija te druge progresivne ili trajne neurolo{ke smetnje.7,12,26 Magnetska rezonancija mozga dje-teta mo`e pokazati atrofiju razli~itog stupnja i zakasnjelu mijelinizaciju (slika 3).57 Posljedice koje izaziva manjak ko-balamina ne ovise samo o te`ini njegova manjka, ve} isto tako i o duljini izlo`enosti njegovu manjku, odnosno na{oj brzini u dijagnosticiranju.2–5 ^ak i kada uspje{no lije~imo manjak vitamina B12 i kada se povuku sve abnormalnosti vidljive slikovnim pretragama mozga, katkad u djeteta os-taju trajne neurolo{ke posljedice.4
Prema literaturi postoji nekoliko definicija prema koji-ma se na temelju laboratorijskih nalaza i/ili klini~ke slike postavlja dijagnoza manjka vitamina B12, te jo{ uvijek ne
Slika 3. Magnetska rezonancija mozga djeteta koje boluje od nutritivnog manjka vitamina B12. Zna~ajna kortikalna atrofija u bolesnika 3, iz tab-
lice 1.Figure 3. Brain magnetic resonance in a child with nutritional vitamin
B12 deficiency. Remarked cortical atrophy in patient 3, from table 1.

45
Lije~ Vjesn 2011; godi{te 133 K. Juras i sur. Manjak vitamina B12 u djece
postoji »zlatni standard« za dijagnozu manjka kobalami-na.58–60 Naj~e{}e se definira koncentracijom kobalamina u plazmi < 150 pmol/L (< 200 pg/ml), homocisteina > 13 µmol/L i metilmalonske kiseline u plazmi > 0,4 µmol/L. Koncentracija kobalamina u krvi manja od 125 pmol/L zna-~i siguran manjak, a koncentracija 125–250 pmol/L vjeroja-tan manjak kobalamina.61 Te vrijednosti ve}inom odgova-raju vrijednostima za odrasle, dok su referentne vrijednosti u djece ne{to druk~ije (vidi raspravu). Za prepoznavanje aktualnog manjka aktivnih oblika kobalamina najpouzdaniji je nalaz povi{ene koncentracije ukupnog homocisteina i povi{ene koncentracije metilmalonske kiseline u plazmi i urinu.62–64 Iako je manjak kobalamina ~est razlog povi{ene koncentracije metilmalonske kiseline i/ili homocisteina, niti povi{enje metilmalonske kiseline, a jo{ manje homocisteina nema kao jedini mogu}i uzrok manjak kobalamina. Za di-jagnozu manjka zaliha vitamina B12 u budu}nosti }e vjero-jatno koncentracija holotranskobalamina zamijeniti dana{-nje testove i postati standard. U tom smislu zna~ajnom se smatra koncentracija holotranskobalamina u serumu < 35 pmol/L.65–67
Pri sumnji na manjak kobalamina djetetu treba izmjeriti koncentraciju vitamina B12, ukupnog homocisteina i metil-malonske kiseline u plazmi te analizirati organske kiseline u urinu (da vidimo postoji li povi{eno izlu~ivanje metilmalon-ske kiseline). Tako|er treba analizirati cijelu krvnu sliku, jer se mogu na}i makrocitna anemija, trombocitopenija, a kat-kad i pancitopenija. Katkad treba analizirati koncentraciju metionina i cistationina u krvi.68 Ako je rije~ o dojen~etu u kojeg sumnjamo na nutritivni manjak kobalamina, koncen-traciju vitamina B12 i kompletnu krvnu sliku, a katkad i kon-centracije ukupnog homocisteina i metilmalonske kiseline u plazmi (ili urinu) treba analizirati i majci. Temelj lije~enja nutritivnog manjka kobalamina jest primjena intramusku-larnih injekcija hidroksokobalamina (ako ga imamo) ili ci-janokobalamina ~im dijagnoza postane vjerojatna. Dijete naru~ujemo na kontrolni pregled obi~no za 3 do 4 tjedna s nalazima koncentracije kobalamina, ukupnog homocisteina i metilmalonske kiseline u krvi ili urinu te kompletne krve slike. U nas se metilmalonska kiselina u krvi rijetko mjeri, a u urinu se analizira u okviru analize organskih kiselina. U svim iole dvojbenim slu~ajevima preporu~ljivo je konzulti-rati se sa specijalistima koji se bave metaboli~kim bolesti-ma. Gdje za to postoje uvjeti, u svrhu procjene popunjenosti zaliha kobalamina mjere se vrijednosti holotranskobalami-na u krvi. U nas to nije slu~aj, pa o tome treba suditi na te-melju drugih spomenutih pretraga, pra}enja i procjene uzro-ka koji su doveli do manjka kobalamina. Djeca ve}inom pokazuju dobar odgovor na primijenjenu terapiju.
Na tablici 1. prikazana su djeca u koje je dijagnosticiran nutritivni manjak vitamina B12. Sva su djeca bila isklju~ivo na maj~inim prsima do trenutka postavljanja dijagnoze. Prete`ito su sva djeca prilikom postavljanja dijagnoze imala koncentracije vitamina B12 u krvi ni`e od 150 pmol/L, kao i povi{ene koncentracije ukupnog homocisteina u krvi i po-ja~ano izlu~ivanje metilmalonske kiseline u urinu. Sva su djeca pokazala dobar klini~ki i laboratorijski odgovor nakon primjene intramuskularnih injekcija vitamina B12. Kriteriji za postavljanje dijagnoze manjka vitamina B12 bili su: simp-tomi i znakovi bolesti koji se mogu pripisati manjku kobala-mina, nepostojanje drugih jasnih uzroka bolesti, bar dva patolo{ki promijenjena od tri glavna laboratorijska pokaza-telja manjka kobalamina (koncentracija kobalamina u krvi, ukupni homocistein u krvi i metilmalonska kiselina u urinu) te pozitivan odgovor na terapiju.
Rasprava
Iz navedenih literaturnih podataka i vlastitog iskustva, dijelom prikazanog opisom nekoliko bolesnika, mo`e se zaklju~iti da se poreme}ajima vezanima uz manjak vitami-na B12, posebno nutritivnim, u Republici Hrvatskoj pridaje premalo pozornosti. Naime, bez obzira na literaturne poka-zatelje koji upu}uju na zna~ajnu u~estalost manjka vitamina B12 u djece prikazani bolesnici gotovo su svi ~iji se opis u doma}oj literaturi mo`e na}i. Uglavnom su bili prepoznati u populaciji koja gravitira Klini~komu bolni~kom centru u Zagrebu, a valja vjerovati da ih mora biti i drugdje, posebno onih s nutritivnim manjkom. Suo~eni s ~injenicom koja go-vori o visokoj u~estalosti ni`ih koncentracija kobalamina u trudnica i ishodu njihove trudno}e,11,13–19 kao i ~esto}i po-reme}aja vezanih uz nutritivni manjak kobalamina u dojene djece,20–22 morali bismo vi{e pa`nje usmjeriti na mogu}nost postojanja tog poreme}aja u djece, posebno jer se radi o jed-nostavno lje~ivom stanju.
Osim vrlo nespecifi~ne klini~ke slike koja nas mo`e na-vesti na pogre{an put k dijagnozi, drugi va`an razlog za ne-prepoznavanje nutritivnog manjka kobalamina jesu referent-ne vrijednosti za koje se u na{oj sredini ~esto ili zabo ravlja da se u djece razlikuju od onih u odraslih ili su ne od go-varaju}e postavljene. To se odnosi ponajprije na koncentra-ciju ukupnog homocisteina u plazmi, koncentraciju kobala-mina u krvi i srednji volumen eritrocita. U djece je gornja granica normalnog raspona ukupnog homocisteina izme|u 8,3 i 10,7 µmol/L,69–71 a normalni raspon u odraslih do 5,4–13,9 µmol/L.48,72 U Hrvatskoj se vrijednosti do 15 µmol/L smatraju normalnima i za djecu i odrasle. Koncentracija ko-balamina u krvi manja od 125 pmol/L zna~i siguran manjak, a koncentracija 125–250 pmol/L vjerojatan manjak kobala-mina.61 U na{oj zemlji referentne vrijednosti za kobalamin u krvi uglavnom su od 145 do 637 pmol/L, {to bi zna~ilo da pojedince koji imaju vrijednosti izme|u 145 do 250 pmol/L progla{avamo zdravima, a mo`da nisu. U jednom na{em la-boratoriju, u kojem je na tablici 1. prvonavedenom djetetu mjeren vitamin B12 referentni raspon je jo{ i ni`i od 103 do 571 pmol/L. Normalne vrijednosti srednjeg volumena eri-trocita (MCV prema engl. mean corpuscular cell volume) tako|er su ovisne o dobi djeteta. U ro|enoga djeteta kre}u se u rasponu od 100 do 125 fL, u dobi od 2 tjedna 88–110 fL, u dobi od 2 mjeseca 84–98 fL, u dobi od 6 mjeseci 73–84 fL, u dobi od godine dana 70–82 fL, u dobi od 2 do 6 godina 72–87 fL, u dobi od 6 do 12 godina 76–90 fL te u dobi od 12 do 18 godina u djevojaka 77–94 fL, a u dje~aka 77–92 fL.73 Na sve te podatke moramo misliti pri interpreti-ranju rezultata, da ne bismo previdjeli patolo{ko stanje koje mo`e biti obilje`eno trajnim posljedicama za zdravlje djete-ta.24 U bolesnika prikazanih na tablici 1. ima vi{e primjera kako su ove va`ne razlike zanemarene i rezultati pretraga nepravilno interpretirani. To je sigurno i jedan od razloga za zna~ajan vremenski odmak u nekih bolesnika izme|u po-~etka simptoma i trenutka prepoznavanja uzroka bolesti. [to se metilmalonske kiseline kao pokazatelja manjka ko-balamina ti~e, smatra se da njezina koncentracija u plazmi iznad 0,4 µmol/L, mo`e upu}ivati na manjak kobalami-na.60,61 Podaci iz jedinoga metaboli~kog laboratorija u Hr-vatskoj u kojem se mjeri metilmalonska kiselina pokazuju da se njezino mjerenje iz krvi tra`i vrlo rijetko, i to u svrhu pra}enja bolesnika s nasljednim oblicima metilmalonske acidurije, a nikad u svrhu otkrivanja manjka vitamina B12. Referentne vrijednosti za metilmalonsku kiselinu u plazmi u nas su 0,08 do 0,57 µmol/L, {to ostavlja mogu}nost da

Tabl
ica
1. P
rim
jeri
dje
ce s
nut
ritiv
nim
man
jkom
vita
min
a B
12.
Tabl
e 1.
Exa
mpl
es o
f chi
ldre
n w
ith d
ieta
ry v
itam
in B
12 d
efic
ienc
y.
Dob
po~
etka
si
mpt
oma/
dob
pri
post
avlja
nju
dija
gnoz
eA
ge a
t the
on
set o
f sy
mpt
oms/
age
at th
etim
e of
di
agno
sis
Klin
i~ka
slik
apr
ije p
o~et
ka li
je~e
nja
Pres
enta
tion
befo
reth
e tre
atm
ent
Vita
min
B12
u kr
vi(1
45–6
37
pmol
/l)*
Seru
mvi
tam
in B
12
conc
entra
tion
(145
–637
pm
ol/l)
*
Uku
pni
hom
ocis
tein
u kr
vi(<
8.3–
10.7
µm
ol/l)
Tota
l ser
um
hom
ocys
tein
co
ncen
tratio
n(<
8.3–
10.7
µm
ol/l)
Met
ilmal
onsk
a ki
selin
a u
urin
u (m
mol
/mol
kr
eatin
ina)
0–4
mj.
(<5)
>4 m
j. (0
)U
rine
met
hyl-
mal
onic
aci
d(m
mol
/mol
crea
tinin
)0–
4 m
o. (<
5)>4
mo.
(0)
Sred
nji v
olum
en e
ritro
cita
Mea
n er
ythr
ocyt
eco
rpus
cula
r vol
ume
(Ovi
sno
o do
bi/A
ge d
epen
dent
: Pri
ro|e
nju
/At b
irth
– 10
0–12
5 fL
;2
tj./w
. – 8
8–11
0 fL
; 2 m
j./m
o. –
84–
98 fL
; 6 m
j./m
o.–
73–8
4 fL
; 1 g
./a. –
70–
82,1
fL
; 2–6
g./a
. – 7
2–87
fL;
6–12
g./a
. – 7
6–90
fL;
12–1
8 g.
/a. –
77–
94 fL
)
Met
ioni
nu
krvi
(15–
45µm
ol/l)
Seru
m
met
hion
ine
conc
entra
tion
(15–
45µm
ol/l)
Preh
rana
maj
keM
ater
nal n
utrit
ion
Preh
rana
dje
teta
do p
osta
vlja
nja
dija
gnoz
eC
hild
’s n
utrit
ion
befo
re d
iagn
osis
Vita
min
B12
u kr
vi m
ajke
(145
–637
pm
ol/L
)***
Mat
erna
lse
rum
vita
min
B12
co
ncen
tratio
n(1
45–6
37
pmol
/l)**
*
Odg
ovor
na
tera
piju
Res
pons
e to
trea
tmen
t
Bol
esni
k 1
– `e
nsko
do
jen~
ePa
tient
1–
fem
ale
infa
nt
2 m
jese
ca/
10,5
mje
seci
2.5
mon
ths/
10.5
mon
ths
blag
o za
osta
janj
eu
tjele
snom
razv
oju,
atop
ijski
der
mat
itis
mild
failu
re to
thriv
e,at
opic
der
mat
itis
162↓
11,4
↑66
↓tij
ekom
trud
no}e
nije
jela
m
eso,
nak
on p
oro|
aja
prvi
h6
mje
seci
nije
jela
mes
o,rib
u, ja
ja, m
lije~
ne p
roiz
vode
durin
g th
e pr
egna
ncy
did
not
eat m
eat,
afte
r birt
h du
ring
the
first
6 m
onth
s di
d no
t eat
mea
t, fis
h, e
ggs
and
dairy
pro
duct
s
iskl
ju~i
vona
prs
ima
excl
usiv
ely
brea
stfe
d
269N
Pozi
tivan
– b
rz o
pora
vak
nako
n uv
o|en
ja d
odat
ne
preh
rane
Posi
tive
– fa
st re
cove
ryaf
ter s
tarti
ng a
dditi
onal
food
Bol
esni
k 2
– m
u{ko
do
jen~
ePa
tient
2–
mal
ein
fant
7,5
mje
seci
/9,
5 m
jese
ci7.
5 m
onth
s/9.
5 m
onth
s
konv
ulzi
je u
afe
briln
om
stan
ju, v
i{ak
spo
ntan
e m
otor
ike
non-
febr
ile s
eizu
res,
ab
unda
nt s
pont
aneo
us
mov
emen
ts
142↓
20,9
↑je
de m
eso
i mlij
e~ne
proi
zvod
eea
ts m
eat a
nd d
airy
prod
ucts
iskl
ju~i
vona
prs
ima
excl
usiv
ely
brea
stfe
d
Pozi
tivan
– n
ema
vi{e
vi{
ak
pokr
eta
Posi
tive
– no
mor
e ex
cess
ive
mov
emen
ts
Bol
esni
k 3
– m
u{ko
do
jen~
ePa
tient
3–
mal
ein
fant
3 m
jese
ca/
4 m
jese
ca3
mon
ths/
4 m
onth
s
te`a
psi
hom
otor
i~ka
re
tard
acija
, mik
roce
falij
ase
vere
psy
chom
otor
re
tard
atio
n, m
icro
ceph
aly
238*
*(n
akon
tera
pije
/af
ter t
he
treat
men
t >2
000)
75↑
(nak
onte
rapi
jeur
edne
vr
ijedn
osti/
norm
aliz
ed
afte
r the
tre
atm
ent)
555
↑(n
akon
tera
pije
/afte
r the
trea
tmen
t 2,
8 N
)
94↑
(nak
on te
rapi
je/a
fter t
he tr
eatm
ent
78N
)
sni`
en(n
akon
tera
pije
ured
ne
vrije
dnos
ti)de
crea
sed
(nor
mal
ized
af
ter t
he
treat
men
t)
rijet
ko je
de m
eso
i mlij
eko
rare
eat
s m
eat a
nd m
ilkin
take
iskl
ju~i
vona
prs
ima
excl
usiv
ely
brea
stfe
d
refe
rent
ne
vrije
dnos
ti/re
fere
ntva
lues
(211
–911
)21
3↓
Pozi
tivan
– `
ivlji
, bol
jepr
ati p
ogle
dom
Dug
oro~
no –
nije
sas
vim
ur
edno
g po
na{a
nja
kao
vr{n
jaci
Posi
tive
– m
ore
vivi
d, b
ette
r ga
ze fo
llow
ing
Long
term
– n
ot c
ompl
etel
y re
gula
r beh
avio
r com
parin
g w
ith p
eers
Bol
esni
k 4
– `e
nsko
do
jen~
ePa
tient
4–
fem
ale
infa
nt
4 m
jese
ca/
6 m
jese
ci4
mon
ths/
6 m
onth
s
konv
ulzi
je u
afe
briln
om
stan
ju, g
ranu
loci
tope
nija
, su
ha k
o`a,
poj
a~an
oga
mi{
i}no
g to
nusa
non-
febr
ile s
eizu
res,
gr
anul
ocyt
open
ia,
dry
skin
, inc
reas
edm
uscl
e to
ne
113↓
(nak
on te
rapi
je/
afte
r the
tre
atm
ent
1110
↑)
17,8
↑(n
akon
tera
pije
/afte
r th
e tre
atm
ent
10N
)
bla`
e po
ja~a
no
izlu
~iva
nje
mild
ly in
crea
sed
excr
etio
n
83,2
N
jede
mes
o i m
lije~
nepr
oizv
ode
eats
mea
t and
dai
rypr
oduc
ts
iskl
ju~i
vona
prs
ima
excl
usiv
ely
brea
stfe
d
302
Pozi
tivan
– p
ostu
pno
ured
nog
psih
omot
orno
g ra
zvoj
aPo
sitiv
e –
grad
ually
nor
mal
ized
ps
ychm
otor
dev
elop
men
t
Bol
esni
k 5
– `e
nsko
do
jen~
ePa
tient
5–
fem
ale
infa
nt
2 m
jese
ca/
9,5
mje
seci
2 m
onth
s/9,
5 m
onth
s
hipe
rtonu
s m
i{i}
a, s
labi
ja
kont
rola
gla
ve i
trupa
mus
cle
hype
rtoni
a, w
eake
r he
ad a
nd tr
unca
l con
trol
107↓
(nak
on te
rapi
je/
afte
r the
tre
atm
ent
496N
)
10,8
↑(n
akon
tera
pije
/afte
r th
e tre
atm
ent
4.1N
)
63↑
(nak
on te
rapi
jeur
edan
nal
az/
norm
aliz
ed a
fter
the
treat
men
t)
u pr
vom
e tro
mje
se~j
utru
dno}
e ni
je je
la m
eso,
ina~
e ne
pije
mlij
eko
i ne
jede
mlij
e~ne
pro
izvo
dedu
ring
the
first
trim
este
r of
preg
nanc
y di
d no
t eat
mea
t, el
se p
oor i
ntak
e of
milk
and
da
iry p
rodu
cts
5. m
j. is
klju
~ivo
na p
rsim
a, z
atim
prsa
i na
dohr
ana,
sa
da je
de s
vu h
ranu
5 m
onth
sex
clus
ivel
ybr
east
fed,
now
eat
s al
l kin
dsof
food
297N
Pozi
tivan
– n
orm
alno
g po
na{a
nja,
suh
e ko
`e, b
la`e
hi
potro
fi~na
i hi
poto
ni~n
a,
`ivn
ula
jePo
sitiv
e –
norm
al b
ehav
iour
, dr
y sk
in, m
ildly
hyp
otro
phic
an
d hy
poto
nic,
bec
ame
vivi
d

Dob
po~
etka
si
mpt
oma/
dob
pri
post
avlja
nju
dija
gnoz
eA
ge a
t the
on
set o
f sy
mpt
oms/
age
at th
etim
e of
di
agno
sis
Klin
i~ka
slik
apr
ije p
o~et
ka li
je~e
nja
Pres
enta
tion
befo
reth
e tre
atm
ent
Vita
min
B12
u kr
vi(1
45–6
37
pmol
/l)*
Seru
mvi
tam
in B
12
conc
entra
tion
(145
–637
pm
ol/l)
*
Uku
pni
hom
ocis
tein
u kr
vi(<
8.3–
10.7
µm
ol/l)
Tota
l ser
um
hom
ocys
tein
co
ncen
tratio
n(<
8.3–
10.7
µm
ol/l)
Met
ilmal
onsk
a ki
selin
a u
urin
u (m
mol
/mol
kr
eatin
ina)
0–4
mj.
(<5)
>4 m
j. (0
)U
rine
met
hyl-
mal
onic
aci
d(m
mol
/mol
crea
tinin
)0–
4 m
o. (<
5)>4
mo.
(0)
Sred
nji v
olum
en e
ritro
cita
Mea
n er
ythr
ocyt
eco
rpus
cula
r vol
ume
(Ovi
sno
o do
bi/A
ge d
epen
dent
: Pri
ro|e
nju
/At b
irth
– 10
0–12
5 fL
;2
tj./w
. – 8
8–11
0 fL
; 2 m
j./m
o. –
84–
98 fL
; 6 m
j./m
o.–
73–8
4 fL
; 1 g
./a. –
70–
82,1
fL
; 2–6
g./a
. – 7
2–87
fL;
6–12
g./a
. – 7
6–90
fL;
12–1
8 g.
/a. –
77–
94 fL
)
Met
ioni
nu
krvi
(15–
45µm
ol/l)
Seru
m
met
hion
ine
conc
entra
tion
(15–
45µm
ol/l)
Preh
rana
maj
keM
ater
nal n
utrit
ion
Preh
rana
dje
teta
do p
osta
vlja
nja
dija
gnoz
eC
hild
’s n
utrit
ion
befo
re d
iagn
osis
Vita
min
B12
u kr
vi m
ajke
(145
–637
pm
ol/L
)***
Mat
erna
lse
rum
vita
min
B12
co
ncen
tratio
n(1
45–6
37
pmol
/l)**
*
Odg
ovor
na
tera
piju
Res
pons
e to
trea
tmen
t
Bol
esni
k 6
– m
u{ko
do
jen~
ePa
tient
6–
mal
ein
fant
4 m
jese
ca/
6 m
jese
ci4
mon
ths/
6 m
onth
s
bla`
a hi
poto
nija
, dis
toni
~ni
sind
rom
, UZ
moz
ga
(atro
fi~ne
pro
mje
ne)
/mild
hyp
oton
ia,d
ysto
nic
synd
rom
e, b
rain
atro
phy
on u
ltras
ound
158↓
7,36
Nbl
a`e
poja
~ano
iz
lu~i
vanj
e(n
akon
tera
pije
u no
rmal
izac
iji)
mild
ly in
crea
sed
excr
etio
n(n
orm
aliz
ed a
fter
the
treat
men
t)
ured
anno
rmal
13↓
slab
o je
de m
eso
poor
mea
t int
ake
iskl
ju~i
vo n
a pr
sim
aex
clus
ivel
y br
east
fed
249
Pozi
tivan
– p
ostu
pno
napr
eduj
e, o
pora
vio
se, u
dob
i od
15
mje
seci
MR
moz
ga
ured
anPo
sitiv
e –
grad
ual f
ailu
re to
th
rive
reco
vere
d, b
rain
MR
I no
rmal
at a
ge o
f 15
mon
ths
Bol
esni
k 7
– `e
nsko
do
jen~
ePa
tient
7–
mal
ein
fant
2,5
mje
seci
/4
mje
seca
2.5
mon
ths/
4 m
onth
s
konv
ulzi
je, h
iper
kine
za,
povi
{en
tonu
s m
usku
latu
re,
plaz
i jez
ik, s
pont
ane
mot
orik
e, `
ivah
ni re
fleks
i/s
eizu
res,
hyp
erki
nesi
s,
incr
ease
d m
uscl
e to
ne,
prot
rude
d to
ngue
,ab
unda
nt s
pont
aneo
usm
otor
act
ivity
, enh
ance
d re
flexe
s
132↓
(nak
on te
rapi
je/
afte
r the
tre
atm
ent
356N
)
15,6
↑(n
akon
tera
pije
/afte
r th
e tre
atm
ent
5,1N
)
ured
an n
alaz
norm
al fi
ndin
g81
.6N
(nak
on te
rapi
je/a
fter t
he tr
eatm
ent
79,0
N)
jede
mes
o i m
lije~
ne p
roiz
vode
eats
mea
t and
dai
ry p
rodu
cts
iskl
ju~i
vo n
a pr
sim
aex
clus
ivel
y br
east
fed
ref.
vr./r
ef.
valu
e(2
08–9
63)
243
Pozi
tivan
– d
obro
g op
}eg
stan
ja, b
ez v
i{ka
pok
reta
, te`
e ot
vara
{ak
e, p
oja~
an to
nus
mi{
i}a,
sla
bije
odi
`e g
lavi
cu,
ali p
ostu
pno
napr
eduj
ePo
sitiv
e –
over
all g
ood
cond
ition
, no
exce
ssiv
e m
ovem
ents
, inc
ompl
ete
fist o
peni
ng, i
ncre
ased
mus
cle
tone
, but
impr
ovin
g gr
adua
lly, w
eake
r hea
dco
ntro
l
Bol
esni
k 8
– `e
nsko
do
jen~
ePa
tient
8–
fem
ale
infa
nt
u pr
vim
m
jese
cim
a/5,
5 m
jese
cidu
ring
the
first
mon
ths/
5.5
mon
ths
konv
ulzi
je, n
enap
redo
vanj
e na
tjel
esno
j te`
ini
seiz
ures
, fai
lure
to th
rive
122↓
(nak
on te
rapi
je/
afte
r the
tre
atm
ent
240N
)
32,4
↑(n
akon
tera
pije
/afte
r the
tre
atm
ent
9,2N
)
ured
an n
alaz
norm
al fi
ndin
g80
,3N
jede
mes
o i m
lije~
ne p
roiz
vode
eats
mea
t and
dai
ry p
rodu
cts
iskl
ju~i
vo n
a pr
sim
aex
clus
ivel
y br
east
fed
Pozi
tivan
– u
redn
og s
tatu
sai d
obro
g op
}eg
stan
ja, n
ije v
i{e
imal
a ko
nvul
zije
Posi
tive
– no
rmal
phy
sica
l fin
ding
, ove
rall
good
con
ditio
n,
no m
ore
seiz
ures
Bol
esni
k 9
– `e
nsko
do
jen~
ePa
tient
9–
fem
ale
infa
nt
10 m
jese
ci/
11 m
jese
ci10
mon
ths/
11 m
onth
s
te`e
gut
a uz
nag
on n
a po
vra}
anje
, usp
avan
a,
gene
raliz
irano
hip
oton
i~na
, za
osta
je u
psi
hom
otor
nom
ra
zvoj
usw
allo
win
g di
ffic
ultie
s,
leth
argy
, gen
eral
ized
hy
poto
nia,
psy
chom
otor
de
velo
pmen
t del
ay
76,3
↓(n
akon
tera
pije
/af
ter t
he
treat
men
t 14
76↑)
113,
3↑(n
akon
tera
pije
/afte
r th
e tre
atm
ent
12,9
↑)
izra
zito
poj
a~an
o iz
lu~i
vanj
e(n
akon
tera
pije
ur
edan
nal
az)
extre
mel
yin
crea
sed
excr
etio
n(n
orm
aliz
ed a
fter
the
treat
men
t)
106↑
(nak
on te
rapi
je/a
fter t
he tr
eatm
ent
81N
)
slab
o je
de m
eso
i mlij
e~ne
pr
oizv
ode
poor
inta
ke o
f mea
t and
dai
ry
prod
ucts
iskl
ju~i
vo n
a pr
sim
aex
clus
ivel
y br
east
fed
136,
6↓Po
zitiv
an –
ure
dan
psih
omot
orni
razv
oj, p
otpu
no
ured
nog
stat
usa
Posi
tive
– no
rmal
psy
chom
otor
de
velo
pmen
t, ph
ysic
ally
co
mpl
etel
y no
rmal
Bro
jevi
u z
agra
dam
a pr
vog
retk
a pr
edst
avlja
ju je
dini
ce i
rasp
one
norm
alni
h vr
ijedn
osti
u st
ru~n
oj li
tera
turi
. N –
nor
mal
na v
rije
dnos
t, ↑
– po
vi{e
na v
rije
dnos
t, ↓
– sn
i`en
a vr
ijedn
ost.
Num
bers
in b
rack
ets
in th
e fi
rst r
ow p
rese
nt u
nits
and
rang
es o
f nor
mal
val
ues
as w
ritte
n in
pro
fess
iona
l lite
ratu
re. N
– n
orm
al v
alue
, ↑ –
hig
h va
lue,
↓ –
low
val
ue.
*
Za
B12
dan
je ra
spon
nor
mal
nih
vrije
dnos
ti ko
ji je
pri
hva}
en u
ve}
ini n
a{ih
labo
rato
rija
; u li
tera
turi
se
navo
di d
a vr
ijedn
osti
ispo
d 12
5 pm
ol/L
zna
~e s
igur
an, a
izm
e|u
125
i 250
pm
ol/L
vje
roja
tan
man
jak
koba
lam
ina
/Ref
eren
t ran
ges
for v
itam
in B
12 w
hich
are
acc
epte
d in
the
maj
ority
of o
ur la
bora
tori
es; l
itera
ture
con
side
rs v
alue
s be
low
125
pm
ol/L
as
cert
ain,
and
bet
wee
n 12
5 an
d 25
0 pm
ol/L
as
poss
ible
cob
alam
in d
efic
ienc
y. *
* U
ovo
g je
dje
teta
kob
alam
in m
jere
n na
kon
{to
je o
no je
dno
vrije
me
tijek
om b
olni
~ke
obra
de je
lo n
orm
alnu
hra
nu. S
ve g
ovor
i u p
rilo
g to
mu
da je
ta v
rije
dnos
t bila
zna
~ajn
o ni
`a k
ada
je d
ijete
pri
mlje
no u
bol
nicu
./I
n th
is c
hild
cob
alam
in w
as m
easu
red
follo
win
g no
rmal
nut
ritio
n du
ring
a h
ospi
tal e
labo
ratio
n. P
resu
mab
ly th
at v
alue
was
sig
nifi
cant
ly lo
wer
by
the
time
the
child
was
adm
itted
into
the
hosp
ital.
***
Maj
kam
a je
kon
cent
raci
ja v
itam
ina
B12
izm
jere
na n
akon
{to
su
se s
impt
omi u
dje
teta
ve}
pov
ukli.
/ In
mot
hers
cob
alam
in c
once
ntra
tion
was
mea
sure
d af
ter r
esol
utio
n of
sym
ptom
s in
chi
ld.
Nas
tava
k ta
blic
e 1.
/ Ta
ble
1 (c
ont.)

48
K. Juras i sur. Manjak vitamina B12 u djece Lije~ Vjesn 2011; godi{te 133
katkad previdimo povi{ene koncentracije. Vjerojatno je i tolerancija prema odre|enomu manjem nedostatku kobala-mina u neke dojen~adi za koji se ra~una da }e spontano ne-stati uz normalnu prehranu dojen~eta razlog da se prihvatlji-vim dr`i izlu~ivanje metilmalonske kiseline u urinu u dobi do 4 mjeseca do 5 mmol/mol kreatinina. Nakon te dobi me-tilmalonska kiselina u urinu smije biti prisutna tek u tragu. Svako odstupanje od toga razlog je za bri`ljivu, specifi~nu i {to skoriju dijagnosti~ku obradu. U spomenutome se me-taboli~kom laboratoriju analizom organskih kiselina indici-ranom iz razli~itih razloga nerijetko u urinu dojen~adi na|e blago povi{eno izlu~ivanje metilmalonske kiseline. Iako po{iljatelj uzorka bude obavije{ten da je mogu}e da se radi i o manjku kobalamina, ne sje}amo se povratne informacije da je obrada krenula u tom smislu i {to je donijela, {to tako|er sugerira da se problemu manjka kobalamina ne pri-stupa dovoljno temeljito.
Ako prihvatimo sve navedene pokazatelje koji upozora-vaju da je u nas nutritivni manjak kobalamina problem koji postoji i koji se zanemaruje sa {tetnim posljedicama za zdravlje nero|ene i ro|ene djece, nedvojbeno bi trebalo oblikovati preporuke za njegovo suzbijanje. One bi o~ito tre-bale biti dane za nekoliko razina odnosno razdoblja pro-vo|enja. Preventivne mjere obuhva}ale bi zdravu prehranu `ena generativne dobi kako bi trudnice prije za~e}a imale po`eljne koli~ine vitamina B12 koje odr`avaju koncentracije kobalamina u krvi na vi{e od 221 pmol/L. To bi najjedno-stavnije bilo posti}i s dovoljno namirnica `ivotinjskog po-drijetla, ponajprije mesa i mlijeka. Druga mjera bila bi pro-vjera koncentracije kobalamina u krvi kao jedna od mjera priprema za trudno}u i na~in da se prepozna manjak koba-lamina i u onih `ena koje unose dovoljno kobalamina, ali imaju problem resorpcije. Jo{ bi pouzdanije za procjenu koli~ine kobalamina u tijelu bilo mjerenje holotranskobala-mina, no {iroka dostupnost te pretrage u nas zasad ne izgle-da realna. Preporuke bi obuhva}ale spomenutu zdravu pre-hranu tijekom cijele trudno}e i parenteralno davanje kobala-mina onim trudnicama u kojih preporu~ena prehrana iz raz-li~itih razloga ne mo`e biti provedena (alergije na mlijeko, u~estalo intenzivno povra}anje itd.). Jedna od sve ra{irenijih metoda rane detekcije manjka kobalamina nakon ro|enja je tzv. pro{ireni novoro|ena~ki skrining koji se zadnjih dese-tak godina sve vi{e primjenjuje u razvijenom svijetu radi ranog otkrivanja brojnih nasljednih metaboli~kih bolesti metodom tandemske spektrometrije masa. U okviru takvog skrininga s namjerom ranog prepoznavanja propionske i metilmalonske kiseline mjeri se i propionilkarnitin, metabo-lit koji bude povi{en i kod manjka kobalamina u djeteta kao posljedica maj~ina nedostatka vitamina B12. U nas su u tije-ku pripreme za takvo pro{irenje novoro|ena~kog skrininga. Za razdoblje nakon toga preporuke za otkrivanje manjka ko-balamina uklju~ivale bi mjerenje bar kobalamina, MCV-a i homocisteina u svakog djeteta koje ima nejasne simptome koji se mogu pripisati nedostatku kobalamina, a nemaju drugo obja{njenje. Sretna je okolnost da je uz mjerenje ko-balamina i mjerenje ukupnog homocisteina u nas dostupnije u sve ve}em broju zdravstvenih ustanova. U iole nejasnim slu~ajevima treba izmjeriti i metilmalonsku kiselinu, za {to je potrebno uzorak uputiti u Metaboli~ki laboratorij Kli-ni~koga bolni~kog centra u Zagrebu, a konzultacija sa spe-cijaliziranim centrom za metaboli~ke bolesti uvijek je do-brodo{la.
Iako priro|eni poreme}aji apsorpcije, transporta i unu-tarstani~nog metabolizma kobalamina nisu ni izbliza tako ~esti kao ste~eni manjak, njihovo zna~enje nipo{to nije ma-leno. S obzirom na to da se radi o skupini od bar desetak
bolesti, njihova zajedni~ka incidencija nije zanemariva. Tu tvrdnju ilustrira i opis na{ih triju bolesnika sa samo jednim od tih poreme}aja (poreme}aj cblA odnosno cblA/cblB). Klini~ki tijek tih bolesnika zorno pokazuje koliko je va`no da svatko tko lije~i djecu bude svjestan postojanja ove sku-pine bolesti i na vrijeme poduzme prikladne dijagnosti~ke i terapijske postupke. Dok se poreme}aji apsorpcije i tran-sporta kobalamina, pa donekle i unutarstani~ni poreme}aji koji zahva}aju samo sintezu metilkobalamina, obi~no o~i-tuju kroni~nim tijekom u kojem ipak ima vremena za ne{to dulja diferencijalnodijagnosti~ka razmi{ljanja, poreme}aji koji zahva}aju sintezu adenozilkobalamina, posebno njezi-ne zadnje stepenice (cblA i cblB) manifestiraju se naj~e{}e akutnim, za `ivot opasnim metaboli~kim krizama pra}enim metaboli~kom acidozom zbog nakupljanja velikih koli~ina metilmalonske kiseline. Na{a bolesnica pod brojem 1 ve} je u dobi od 7 dana bila u dubokom soporu, a drugih dvoje je u sli~no te{ko stanje do{lo samo 2 do 3 dana nakon prvih simptoma krize. Njihove pri~e pokazuju kako razlozi za pogor{anje mogu biti kataboli~ko stanje neposredno nakon ro|enja, povra}anje kao reakcija na novu hranu ili naizgled bezazlena interkurentna infekcija – sve podra`aji kakve dje-ca bez priro|enih metaboli~kih poreme}aja lako prevladaju. U takvim situacijama treba se prisjetiti »abecede« nasljed-nih metaboli~kih bolesti, pa u ugro`enog bolesnika ~iji se simptomi ne mogu valjano objasniti ste~enim uzrocima po-sumnjati na nasljedni metaboli~ki poreme}aj i hitno podu-zeti odgovaraju}e mjere – prekid unosa hrane (time i bje-lan~evina koje ovi bolesnici ne mogu sasvim razgraditi), zaustaviti katabolizam izda{nim parenteralnim unosom glukoze s elektrolitima te uz ostale simptomatske mjere svakako dati »koktel« kofaktora koji mogu pokrenuti enzim-ske reakcije koje ne funkcioniraju. Tom »koktelu« kojemu se dodaje karnitin obi~no pripadaju vitamini B1, B2, H (bio-tin) i, u ovom slu~aju spasonosni, B12. Daju se u visokim, tzv. farmakolo{kim dozama, a za bolesnike kao {to su ovdje opisani ka`e se jo{ da boluju od vitaminskih ovisnosti. Iz prikazanog je jasno da propu{teno ili zakasnjelo davanje ovih vitamina mo`e bolesnika stajati `ivota ili biti uzrok trajnih posljedica za zdravlje i da bi ih svaka bolnica morala imati na raspolaganju za hitne bolesnike kao {to su ovi. Kad je ve} rije~ o kobalaminu, {teta je {to je Hrvatskoj na ras-polaganju samo cijanokobalamin umjesto u~inkovitijeg hi-droksokobalamina, kako zbog opisanih bolesnika koji redo-vito parenteralno moraju primati kobalamin tako i zbog onih koje }emo tek u nekim sli~nim krizama otkriti. Iako bi terapijski postupak za sve bolesnike u ovakvim situacijama trebao biti sli~an, valja ipak naglasiti da je hitna analiza or-ganskih kiselina u svih troje bolesnika omogu}ila posta-vljanje to~ne dijagnoze metilmalonske acidurije i nastavak ciljanog lije~enja u roku od 24 sata nakon dolaska u Refe-rentni centar u Klini~kome bolni~kom centru u Zagrebu. To pokazuje koliko je va`no da u ovakvim zgodama specifi~ne pretrage postaju hitne i budu 24 sata na raspolaganju.
Zaklju~no se mo`e re}i da manjak vitamina B12 sa svojim vrlo {irokim spektrom klini~kih manifestacija i zapravo vi-sokom pojavno{}u neosporno mora biti predmet interesa svakog tko se bavi djecom po~ev{i ve} prije trenutka njiho-va za~e}a. Jednostavno lije~enje i mogu}e te{ke i trajne po-sljedice razlog su da i zajednica u~ini sve {to mo`e kako bismo smanjili {tetan u~inak manjka kobalamina za `ivot i zdravlje djece. Promicanje pravilne prehrane, organizirana skrb o `enama prije trudno}e i trudnicama, pro{irenje pro-grama novoro|ena~kog skrininga, dobra i {iroka raspolo-`ivost specifi~nih pretraga i kobalamina (po mogu}nosti u obliku hidroksokobalamina), odabir realnih referentnih ra-

49
Lije~ Vjesn 2011; godi{te 133 K. Juras i sur. Manjak vitamina B12 u djece
spona u laboratorijskim nalazima i trajna edukacija zdrav-stvenog osoblja u prepoznavanju i lije~enju brojnih pore-me}aja koji rezultiraju manjkom aktivnih oblika kobalami-na mjere su na kojima bi trebalo ustrajati. Vjerujemo da }e napretku u tom smislu i ovaj ~lanak biti doprinos.
Zahvala
Zahvaljujemo dr. Brianu Fowleru, Universitäts Kinder-spital Basel, na mjerenjima enzimske aktivnosti u prikaza-nih bolesnica s poreme}ajem unutarstani~nog metabolizma kobalamina.
Ovaj rad poduprlo je Ministarstvo znanosti, obrazova-nja i {porta Republike Hrvatske u okviru projekta 0108--1081870-1885.
L I T E R A T U R A
1. Herrmann W, Obeid R. Causes and Early Diagnosis of Vitamin B12 De-ficiency. Dtsch Ärztebl Int 2008;105:680–5.
2. Grattan-Smith PJ, Wilcken B, Procopis PG, Wise GA. The neurological syndrome of infantile cobalamin deficiency: developmental regression and involuntary movements. Mov Disord 1997;12:39–46.
3. Graham SM, Arvela OM, Wise GA. Long-term neurologic consequenc-es of nutritional vitamin B12 deficiency in infants. J Pediatr 1992;121: 710–4.
4. von Schenck U, Bender-Gotze C, Koletzko B. Persistence of neurologi-cal damage induced by dietary vitamin B-12 deficiency in infancy. Arch Dis Child 1997;77:137–9.
5. Louwman MW, van Dusseldorp M, van de Vijver FJ i sur. Signs of im-paired cognitive function in adolescents with marginal cobalamin sta-tus. Am J Clin Nutr 2000;72:762–9.
6. Quadros EV. Advances in the Understanding of Cobalamin Assimila-tion and Metabolism. Br J Haematol 2010;148:195–204.
7. Coelho D, Suormala T, Stucki M i sur. Gene identification for the cblD defect of vitamin B12 metabolism. N Engl J Med 2008;358:1454–64.
8. Allen LH. How common is vitamin B-12 deficiency? Am J Clin Nutr 2009;89:693–6.
9. Dali-Youcef N, Andres E. An update on cobalamin deficiency in adults. Q J Med 2009;102:17–28.
10. Wolters M, Ströhle A, Hahn A. Age-associated changes in the metabo-lism of vitamin B(12) and folic acid: prevalence, aetiopathogenesis and pathophysiological consequences. Z Geront Geriatr 2004;37:109–35.
11. Lowenstein L, Lalonde M, Deschenes EB, Shapiro L. Vitamin B12 in pregnancy and the puerperium. Am J Clin Nutr 1960;8:265–75.
12. Bjørke-Monsen AL i sur. Common metabolic profile in infants indicat-ing impaired cobalamin status responds to cobalamin supplementation. Pediatrics 2008;122:83–91.
13. Molloy AM i sur. Maternal vitamin B12 status and risk of neural tube defects in a population with high neural tube defect prevalence and no folic Acid fortification. Pediatrics 2009;123:917–23.
14. Kirke PN, Molloy AM, Daly SE, Burke H, Weir DG, Scott JM. Maternal plasma folate and vitamin B12 are independent risk factors for neural tube defects. Q J Med 1993;86:703–8.
15. Suarez L, Hendricks K, Felkner M, Gunter E. Maternal serum B12 levels and risk for neural tube defects in a Texas-Mexico border population. Ann Epidemiol 2003;13:81–8.
16. Groenen PM, van Rooij IA, Peer PG, Gooskens RH, Zielhuis GA, Stee-gers-Theunissen RP. Marginal maternal vitamin B12 status increases the risk of offspring with spina bifida. Am J Obstet Gynecol 2004;191:11–7.
17. Ronnenberg AG, Goldman MB, Chen D i sur. Preconception homocys-teine in Chinese women. Am J Clin Nutr 2002;76:1385–91.
18. Lindblad B, Zaman S, Malik A i sur. Folate, vitamin B12 and homocys-teine levels in South Asian women with growth-retarded fetuses. Acta Obstet Gynecol Scand 2005;84:1055–61.
19. Muthayya S, Kurpad AV, Duggan CP i sur. Low maternal vitamin B12 status is associated with intrauterine growth retardation in urban South Indians. Eur J Clin Nutr 2006;60:791–801.
20. Allen LH. Vitamin B12 metabolism and status during pregnancy, lacta-tion and infancy. Adv Exp Med Biol 1994;352:173–86.
21. Rosenblatt DS, Whitehead VM. Cobalamin and folate deficiency: ac-quired and hereditary disorders in children. Semin Hematol 1999;36:19–34.
22. Ueland PM, Bjørke-Monsen AL. Total homocysteine is making its way into pediatric laboratory diagnostics. Eur J Clin Invest 2001;31:928–30.
23. Campbell CD, Ganesh J, Ficicioglu. Two newborns with nutritional vitamin B12 deficiency: Challenges in newborn screening for vitamin B12 deficiency. Haematologica 2005;90:119–21.
24. Von Schenck U, Bender-Götze C, Koletzko B. Persistence of neurologi-cal damage induced by dietary Vitamin B-12 deficiency in infancy. Arch Dis Child 1997;77:137–9.
25. Johnston J, Bollekens J, Allen RH, Berliner N. Structure of the cDNA encoding transcobalamin I, a neutrophil granule protein. J Biol Chem 1989;264:15754–7.
26. Whitehead VM. Acquired and inherited disorders of cobalamin and fo-late in children. Br J Haematol 2006;134:125–36.
27. Yang YM, Ducos R, Rosenberg AJ i sur. Cobalamin malabsorption in three siblings due to an abnormal intrinsic factor that is markedly sus-ceptible to acid and proteolysis. J Clin Invest 1985;76(6):2057–65.
28. Katz M, Mehlman CS, Allen RH. Isolation and characterization of an abnormal human intrinsic factor. J Clin Invest 1974;53(5):1274–83.
29. Rothenberg SP, Quadros EV, Straus EW, Kapelner S. An abnormal in-trinsic factor (IF) molecule: A new cause of »pernicious anemia« (PA). Blood 1984;103:1515–1517
30. Chanarin I. The Megaloblastic Anaemias, 3. izd. London: Blackwell Scientific Publications; 1990.
31. http://emedicine.medscape.com/article/1152670-overview32. Kristiansen M, Kozyraki R, Jacobsen C, Nexo E, Verroust PJ, Moestrup
SK. Molecular dissection of the intrinsic factor – vitamin B12 receptor, cubilin, discloses regions important for membrane association and li-gand binding. J Biol Chem 1999;274:20540–4.
33. He Q, Madsen M, Kilkenney A i sur. Amnionless function is required for cubilin brush-border expression and intrinsic factor – cobalamin (vitamin B12) absorption in vivo. Blood 2005;106:1447–53.
34. Birn H, Willnow TE, Nielsen R i sur. Megalin is essential for renal pro-ximal tubule reabsorption and accumulation of transcobalamin – B(12). Am J Physiol – Ren Physiol 2002;282:408–16.
35. Ahuja R, Yammani R, Bauer JA, Kalra S, Seetharam S, Seetharam B. Interactions of cubilin with megalin and the product of the amnionless gene (AMN): effect on its stability. Biochem J 2008;410:301–8.
36. Orlando RA, Exner M, Czekay RP i sur. Identification of the second cluster ligand-binding repeats in megalin as a site for receptor-ligand interactions. Proc Natl Acad Sci USA 1997;94:2368–73.
37. Moestrup SK, Birn H, Fischer PB i sur. Megalin-mediated endocytosis of transcobalamin-vitamin-B12 complexes suggests a role of the re-ceptor in vitamin-B12 homeostasis. Proc Natl Acad Sci USA 1996;93: 8612–7.
38. Christensen EI, Gliemann J, Moestup SK. Renal tubule gp330 is a cal-cium binding receptor for endocytic uptake of protein. J Histochem Cytochem 1992;40:1481:90.
39. Birn H, Verroust PJ, Nexo E i sur. Characterization of an epithelial ap-proximately 470-kDa protein that facilitates endocytosis of intrinsic factor-vitamin B12 and binds receptor-associated protein. J Biol Chem 1997;272:26497–504.
40. Christensen EI, Birn H. Megalin and cubilin: synergistic endocytic re-ceptor sin renal proximal tubule. Am J Physiol Renal Physiol 2001; 280:62–73.
41. Madhavan S i sur. Imerslund-Gräsbeck syndrome: association with dia-betes mellitus. Indian Pediatrics 2009;46:251–3.
42. Najman E, Brausil B. Megaloblastische Anämie mit Relapsen ohne Ac-hylia gastrica im Kindesalter. Annales paediatrici 1952;178(1):47–59.
43. Adkins Y, Lonnerdal B. Mechanisms of vitamin B(12) absorption in breast-fed infants. J Pediatr Gastroenterol Nutr 2002;35:192–8.
44. Quadros EV, Rothenberg SP, Pan YC, Stein S. Purification and molecu-lar characterization of human transcobalamin II. Am J Physiol 1989; 256:296–303.
45. Frisbie SM, Chance MR. Human cobalophilin: the structure of bound methylcobalamin and a functional role in protecting methylcobalamin from photolysis. Biochemistry 1993;32(50):13886–92.
46. Rosenblatt DS, Fowler B. Disorders of Cobalamin and Folate Transport and Metabolism. U: Fernandes J, Saudubray JM, van den Berghe G, Walter JH, ur. Inborn Metabolic Diseases, 4. izd. Heidelberg: Springer; 2006, str. 341–51.
47. Yammani RR, Seetharam S, Dahms NM, Seetharam B. Transcobalamin II receptor interacts with megalin in the renal apical brush border mem-brane. J Membr Biol 2003;193:57–66.
48. Coelho D, Suormala T, Stucki M i sur. Gene identification for the Cbld defect of vitamin B12 metabolism. N Engl J Med 2008;358(14):1454–64.
49. Banerjee R. The Ying-Yang of cobalamin biochemistry. Chem Biol 1997;4:175–186.
50. Bari} I, Fumi} K, Glenn B i sur. S-adenosylhomocisteine hydrolase deficiency in a human: a genetic disorder of methionine metabolism. Proc Nat Acad Sci USA 2004;101:4234–9.
51. Gali} S. Zna~enje polimorfizma C677T gena za 5,10-metilentetra-hidrofolat reduktazu u patogenezi poreme}aja razvoja neuralne cijeviu populaciji Hrvatske (magistarski rad). Zagreb: Medicinski fakultet Sveu~ili{ta u Zagrebu; 2005, str. 146.
52. Rasmussen SA, Fernhoff PM, Scanlon KS. Vitamin B12 deficiency in children and adolescents. J Pediatr 2001;138:10–17.

50
K. Juras i sur. Manjak vitamina B12 u djece Lije~ Vjesn 2011; godi{te 133
VERTEBROBAZILARNA INSUFICIJENCIJAI OPSTRUKCIJSKA APNEJA TIJEKOM SPAVANJA
VERTEBROBASILAR INSUFFICIENCY AND OBSTRUCTIVE SLEEP APNEA
VJEKOSLAV GRGI]*
Deskriptori: Opstrukcijska apneja tijekom spavanja – etiologija; Vertebrobazilarna insuficijencija – komplikacije; Medula oblongata – patofiziologija; Anoksija – patofiziologija
Sa`etak. Cilj je ovoga ~lanka upozoriti na me|usobnu povezanost vertebrobazilarne insuficijencije (VBI) i opstrukcijske apneje tijekom spavanja (engl. obstructive sleep apnea; OSA) {to do sada nije dovoljno primije}eno. Naime, u opse`noj literaturi o poreme}ajima disanja tijekom spavanja VBI se navodi samo kao jedan od mogu}ih uzroka sredi{nje i mije{ane apneje tijekom spavanja. Me|utim, prema na{im klini~kim zapa`anjima, VBI bi moglo biti jedan od najva`nijih ~imbenika u etiopatogenezi OSE. Rezultati nedavnog istra`ivanja, koji potvr|uju uzro~no-posljedi~nu vezu izme|u VBI i OSE, idu u prilog na{oj hipotezi. Visoka prevalencija i patogeneza OSE u bolesnika s VBI-jem mogu se objasniti hipoksijom produ`ene mo`dine tijekom spavanja (spavanje+polo`ajni VBI→hipoksija produ`ene mo`dine→hipoksija respiracijskog centra koji regulira funkciju disanja+hipoksija motornih jezgara IX, X. i XII. kranijalnog `ivca ~iji neuroni reguliraju tonus mi{i}a gornjega di{nog puta (IX, X) i jezika (XII)→OSA). Razvoj OSE u odre|enih bolesnika s VBI-jem vjerojatno je u uskoj uzajamnoj vezi sa stupnjem hipoksije produ`ene mo`dine tijekom spavanja (umjereni VBI→OSA; te{ki VBI→sredi{nja ili mije{ana apneja tijekom spavanja). S obzirom na ~injenicu da VBI vaskularne i/ili kompresivne etiologije mo`e biti prima-ran uzrok OSE, doplersonografski pregled VB slijeva (VBS) s polo`ajnim funkcionalnim testovima trebalo bi uklju~iti u dijagnosti~ki algoritam za OSU. Budu}i da funkcionalni i organski poreme}aji vratne kralje`nice mogu uzrokovati cirku-lacijske smetnje u VBS-u ili pogor{avati oslabljenu cirkulaciju, osobito tijekom spavanja u odre|enim polo`ajima glave i vrata, detaljan pregled vratne kralje`nice koji uklju~uje fizijatrijski pregled, manualni funkcionalni pregled i radiolo{ki pregled, trebao bi postati dio rutinskog pregleda u bolesnika sa suspektnom ili potvr|enom OSOM. Odgovaraju}om terapi-jom vaskularnih poreme}aja (primjerice, ugradnja stenta u vertebralnu arteriju) mo`e se pobolj{ati ili normalizirati cirku-lacija u VBS-u, a odgovaraju}om terapijom poreme}aja vratne kralje`nice (primjerice, manualna terapija, fizikalna terapija, kineziterapija, operacija i dr.) mo`e se smanjiti ili ukloniti kompresivni u~inak poreme}aja vratne kralje`nice na cirkulaci-
* Privatna lije~ni~ka ordinacija (Vjekoslav Grgi}, dr. med.) Adresa za dopisivanje: Dr. V. Grgi}, Bosanska 10, 10 000 Zagreb, e-mail: vjekoslav.grgicºzg.t-com.hrPrimljeno 21. rujna 2009., prihva}eno 27. velja~e 2010.
53. Institute of Medicine. Dietary reference intakes for thiamin, riboflavin, niacin, vitamin B6, folate, vitamin B12, pantothenic acid, biotin, and choline. Washington: Nat Acad Press 2000;50–95.
54. Habicht JP. Expert consultation on the optimal duration of exclusive breastfeeding: the process, recommendations, and challenges for the future. Adv Exp Med Biol 2004;554:79–87.
55. Kontic-Vucinic O, Sulovic N, Radunovic N. Micronutritiens in women’s reproductive health, part I: vitamins. Int J Fertil Womens Med 2006; 51:106–115.
56. Honzik T, Adamovicova M, Smolka V, Magner M, Hruba E, Zeman J. Clinical presentation and metabolic consequences in 40 breastfed in-fants with nutritional vitamin B(12) deficiency – What have we learned? Eur J Pediatr Neurol 2010; in print.
57. Lövblad K, Ramelli G, Remonda L, Nirkko AC, Ozdoba C, Schroth G. Retardation of myelination due to dietary vitamin B12 deficiency: cra-nial MRI findings. Pediatric Radiol 1997;27:155–158.
58. Snow CF. Laboratory diagnosis of vitamin B12 and folate deficiency:a guide for the primary care physician. Arch Intern Med 1999;159:1289–98.
59. Zittoun J, Zittoun R. Modern clinical testing strategies in cobalamin and folate deficiency. Semin Hematol 1999;36:35–46.
60. Carmel R. Current concepts in cobalamin deficiency. Annu Rev Med 2000;51:357–75.
61. Hvas AM, Nexo E. Diagnosis and treatment of vitamin B12 deficiency. An update. Haematologica 2006;91:1506–12.
62. Monsen AL i sur. Cobalamin status and its biochemical markers me-thylmalonic acid and homocysteine in different age groups from 4 days to 19 years. Clin Chem 2003;49:2067–75.
63. Bjorke Monsen AL i sur. Determinants of cobalamin status in newborns. Pediatrics 2001;108:624–30.
64. Lindenbaum J, Healton EB, Savage DG i sur. Neuropsychiatric disor-ders caused by cobalamin deficiency in the absence of anemia or mac-rocytosis. N Engl J Med 1988;318:1720–1728.
65. Klee GG. Cobalamin and folate evaluation: measurement of methylma-lonic acid and homocysteine vs vitamin B(12) and folate. Clin Chem 2000;46:1277–83.
66. Andres E, Perrin AE, Kraemer JP i sur. Anemia caused by vitamin B12 deficiency in subjects aged over 75 years: new hypotheses. A study of 20 cases. Rev Med Interne 2000;21:946–54.
67. Markle HV. Cobalamin. Crit Rev Clin Lab Sci 1996;33:247–356.68. Stabler SP, Lindenbaum J, Savage DG, Allen RH. Elevation of serum
cystathionine levels in patients with cobalamin and folate deficiency. Blood 1993;81:3404–3413.
69. Vilaseca MA, Moyano D, Ferrer I, Artuch R. Total Homocysteine in Pediatric Patients. Clin Chem 1997;43:690–2.
70. Delvin EE, Rozen R, Merouani A, Genest J, Lambert M. Influence of methylenetetrahydrofolate reductase genotype, age, vitamin B-12, and folate status on plasma homocysteine in children. Am J Clin Nutr 2000;72:1469–1473.
71. Reddy MN. Reference ranges for total homocysteine in children. Clin Chim Acta 1997;262:153–155.
72. Ueland PM, Refsum H, Stabler SP, Malinow MR, Andersson A, Allen RH. Total homocysteine in plasma or serum: methods and clinical ap-plications. Clin Chem 1993;39:1764–1779.
73. Arceci RJ, Hann IM, Smith OP. Pediatric Hematology, 3. izd. Baltimo-re: Maryland: Blackwell Publishing; 2006, str. 793.