BAB II TINJAUAN PUSTAKA 2.1 Ginjal 2.1.1 Struktur dan ...
Transcript of BAB II TINJAUAN PUSTAKA 2.1 Ginjal 2.1.1 Struktur dan ...

6
BAB II
TINJAUAN PUSTAKA
2.1 Ginjal
2.1.1 Struktur dan Anatomi Ginjal
Ginjal merupakan sepasang organ dari sistem urinaria yang berwarna coklat
kemerahan yang terletak dirongga retroperitoneal bagian atas pada dinding abdomen
di kanan dan kiri columna vertebralis setinggi vertebra T12 hingga L3 dan sebagian
besar tertutup oleh arcus costalis. Ginjal kanan terletak sedikit lebih rendah dari pada
ginjal kiri karena besarnya lobus hepatis dekstra (Guyton dan Hall, 2014). Pada orang
dewasa, berat ginjal kira kira 140 gram dengan panjang 6-7,5 cm dan tebal 1,5-2,5 cm
dan bentuknya menyerupai seperti biji kacang dan sisi dalamnya atau hilum
menghadap ke tulang punggung sedangkan sisi luarnya cembung (Pearce, 2016).
Setiap ginjal diselubungi oleh tiga lapisan jaringan ikat yaitu kapsula fibrosa,
Lemak Perirenal, dan fasia renal. Lapisan pertama yang paling dekat dengan struktur
ginjal adalah kapsula fibrosa yang berfungsi untuk mencegah penjalaran infeksi dari
regio sekitar ke ginjal. Lapisan kedua merupakan lemak perirenal, yang melindungi
ginjal dari benturan dan Lapisan terluar adalah fasia renal yang merupakan jaringan
ikat fibrosa yang padat dan berfungsi untuk memisahkan ginjal dan kelenjar adrenal
dari struktur sekitar (Marieb & Hoehn, 2015).
Pada potongan sagital ginjal terdapat 2 bagian, yaitu bagian tepi luar ginjal yang
disebut cortex renalis yang berwarna coklat gelap dan bagian dalam ginjal yang
berbentuk segitiga disebut piramid ginjal atau bagian medula renalis yang berwarna
coklat terang (Guyton dan Hall, 2014). Bagian medula renalis ini tersusun atas 15-16
massa berbentuk piramida. Puncaknya langsung mengarah ke hilum dan berakhir di
kalises. Kalises ini menghubungkannya dengan pelvis ginjal (Pearce, 2015). Bagian
medula yang berbentuk kerucut disebut pelvis renalis, yang akan terhubung dengan
ureter sehingga urin yang terbentuk dapat lewat menuju vesika urinaria (Verdiansyah,
2016).

7
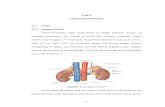
Gambar 2.1 Penampang posisi ginjal pada tubuh (Shier, 2012)
Unit anatomik fungsi ginjal adalah nefron. Nefron merupakan struktur kapiler
berkelompok dengan fungsi yang sama, terdiri dari glomerulus dan tubulus renalis
yang dilingkupi oleh kapsula Bowman. Glomerulus merupakan tempat dimana fungsi
filtrasi darah berlangsung, sedangkan tubulus renalis merupakan tempat untuk
reabsorpsi air dan garam yang masih diperlukan oleh tubuh. (Maulidah, 2015). Setiap
satu ginjal manusia memiliki sekitar satu juta nefron yang merupakan unit pembentuk
urin (Perlman et al., 2014).
Glomerulus berdiameter kira-kira 200 μm dan terdiri dari arteriol aferen dan
sekelompok kapiler yang dibatasi oleh sel endotel dan dilapisi oleh sel epitel yang
membentuk lapisan kapsula Bowman dan tubulus renalis (Maulidah, 2015). Arteriol
aferen bekerja membawa darah masuk ke glomerulus dan arteriol eferen bekerja
membawa darah keluar dari glomerulus. Arteriol eferen bercabang menjadi kapiler
peritubulus yang memperdarahi tubulus (Verdiansyah, 2016). Tubulus renalis terdiri
dari tubulus kontortus proksimal, lengkung henle, dan tubulus kontortus distal. Pada
daerah tubulus kontortus proksimal, air dan elektrolit direabsorpsi dalam jumlah ±
80%. Pada daerah ansa henle terjadi pemekatan urin dan pada daerah tubulus kontortus
distal berperan untuk mengatur keseimbangan air dan elektrolit yang diubah
berdasarkan kontrol hormonal (Maulidah, 2015).

8
Gambar 2.2 Penampang melintang ginjal (a), piramida ginjal (b), dan nefron (c)
(Shier, 2012)
2.1.2 Fisiologi Ginjal
Alatas et al (2011) menjelaskan bahwa fungsi ginjal adalah sebagai organ
ekskresi. Ginjal memiliki fungsi utama dalam menjaga keseimbangan internal dengan
menjaga komposisi cairan ekstraselular. Untuk melaksakan hal tersebut sejumlah
cairan yang hampir bebas protein difiltrasi dari kapiler glomerulus ke kapsula
Bowman. Kebanyakan zat dalam plasma, kecuali protein, di filtrasi secara bebas,
sehingga konsentrasi pada filtrat glomerulus dalam kapsula bowman hampir sama
dengan plasma. Awalnya zat akan difiltrasi secara bebas oleh kapiler glomerulus tetapi
tidak difiltrasi, kemudian direabsopsi (Sherwood, 2014). Tingkat reabsorpsi bervariasi
menurut substansi dan lokasi anatomis di tubulus, sehingga memungkinkan untuk
pengaturan regulasi komponen penyusun yang berbeda. Sebagian besar 60-70% Na+
yang disaring dan hampir semua K+ dan glukosa secara aktif diserap dari cairan tubular
melalui mekanisme co-transpor di tubulus proksimal dan air diserap secara pasif
disepanjang gradien osmotik yang dibentuk oleh reabsorpsi Na+. Selain penyerapan,
sejumlah zat disekresikan ke dalam cairan tubular melalui transporter di sepanjang

9
tubulus ginjal (Perlman et al., 2014). Filtrat glomerular yang memasuki tubulus ginjal
akan mengalir secara berurutan melalui tubulus proksimal, lengkung henle, tubulus
distal dan collecting duct sebelum dikeluarkan sebagai urin (Guyton dan Hall, 2011).
Dalam keadaan normal, tidak lebih dari 5-10 mL/menit filtrat glomerular dikirim ke
collecting duct (Perlman et al., 2014). Peran penting dari collecting duct dalam
pengaturan fungsi ginjal bergantung pada dua hal yaitu sebagai kontrol hormonal, dan
merupakan daerah terakhir dari tubulus ginjal yang dilalui sebelum 1-2 ml/min sisa
dari filtrat glomerulus keluar ke ureter sebagai urin (Perlman et al., 2014). Setelah
ureter, urin akan ditampung terlebih dahulu di kandung kemih. Bila orang tersebut
merasakan keinginan berkemih dan keadaan memungkinkan, maka urin yang
ditampung dikandung kemih akan di keluarkan lewat uretra (Sherwood, 2014).
Ginjal memiliki fungsi utama yaitu sebagai fungsi ekskresi dan non-ekskresi.
Fungsi ekskresi pada ginjal antara lain ekskresi produk sisa metabolisme dan bahan
kimia asing, pengaturan keseimbangan air dan elektrolit, pengaturan keseimbangan
asam dan basa, pengaturan osmolaritas cairan tubuh ,sekresi dan ekskresi hormon dan
glukoneogenesis (Guyton & Hall, 2014).
a) Ekskresi produk sisa metabolik, bahan kimia asing, obat dan metabolik hormon.
Ginjal merupakan organ utama yang berfungsi untuk membuang produk sisa
metabolisme yang tidak diperlukan lagi oleh tubuh. Produk-produk ini meliputi urea
(dari sisa metabolisme asam amino), kreatin asam urat (dari asam nukleat), produk
akhir dari pemecahan hemoglobin (bilirubin), metabolik hormon, garam anorganik,
bakteri dan juga obat-obatan. Jika zat-zat ini tidak diekskresikan oleh ginjal, maka
tubuh akan diracuni oleh kotoran yang dihasilkan oleh tubuhnya sendiri (Prabowo dan
Pranata, 2014). Setiap harinya kedua ginjal pada orang dewasa mengeluarkan 1,5 – 2,5
liter urin. Ginjal juga tersusun dari beberapa juta unit fungsional (nefron) yang akan
melakukan ultrafiltrasi terkait dengan ekskresi (pembentukan urin) dan reabsorpsi
(Guyton dan Hall, 2014).

10
b) Pengaturan keseimbangan air dan elektrolit
Peran ginjal dalam menjaga keseimbangan air tubuh diregulasi oleh ADH (Anti-
Diuretik Hormon). ADH akan bereaksi pada perubahan osmolalitas dan volume cairan
intravaskuler. Peningkatan osmolalitas plasma atau penurunan volume cairan
intravaskuler menstimulasi sekresi ADH oleh hipotalamus posterior, selanjutnya ADH
akan meningkatkan permeabilitas tubulus kontortus distal dan duktus kolektivus,
sehingga reabsorpsi meningkat dan urin menjadi lebih pekat. Pada keadaan haus, ADH
akan disekresikan untuk meningkatkan reabsorpsi air. Pada keadaan dehidrasi, tubulus
ginjal akan memaksimalkan reabsorpsi air sehingga dihasilkan sedikit urin dengan
osmolalitas mencapai 1200 mOsmol/L. Pada keadaan cairan berlebihan akan
dihasilkan banyak urin dan encer dengan osmolalitas menurun sampai dengan 50
mOsmol/L (Verdiansyah, 2016). Selain itu, ginjal juga dapat mengekskresikan ion
natrium (Na+), kalium (K+), kalsium (Ca2+), magnesium (Mg), sulfat (SO42−) dan
fosfat (PO43−) (Tortora, 2014).
c) Pengaturan tekanan arteri
Peningkatan volume darah akan meningkatkan tekanan darah sedangkan
penurunan volume darah akan menurunkan tekanan darah (Tortora, 2014).
Pemeliharaan natrium dan keseimbangan ginjal akan mencapai regulasi volume darah.
Sehingga, melalui kontrol volume, ginjal ikut serta dalam pengendalian tekanan darah
(Eaton, 2009).
Ginjal memegang peran penting dalam regulasi tekanan darah melalui
pengaturan Natrium dan keseimbangan air. Konsentrasi Na+ di cairan tubulus
proksimal dideteksi di makula densa yaitu di bagian aparatus juxtaglomerulus. Melalui
peran makula densa dan juxtaglomerular terjadi penurunan konsentrasi natrium di
duktus kolektivus dan penurunan tekanan darah yang akan merangsang terbentuknya
renin. Renin merupakan suatu protease yang dibentuk di sel juxtaglomerular yang akan
menguraikan angiotensinogen dalam sirkulasi menjadi angiotensin I, kemudian
angiotensin I diuraikan oleh angiotensin-converting enzyme (ACE) menjadi
angiotensin II. Angiotensin II merupakan salah satu vasokonstriksi kuat yang
menyebabkan terjadinya konstriksi arteriol yang bekerja pada korteks adrenal dalam

11
meningkatkan produksi aldosterone (Barrett et al., 2012). sehingga menyebabkan
retensi natrium dan air oleh ductus collingens serta meningkatkan cairan intravascular
dan peningkatan tekanan darah akibat dari peningkatan renin (Tortora, 2014). Efek dari
Angiotensin II adalah meningkatnya tekanan darah melalui 2 mekanisme tersebut.
Sistem pengaturan tekanan darah ini sering disebut RAAS (Renin Angiotensin
Aldosterone System).
d) Pengaturan asam-basa
Ginjal berperan dalam pengaturan keseimbangan asam-basa bersama dengan
paru dan sistem dapar cairan tubuh dengan cara mengekskresikan asam dan mengatur
penyimpanan dapar cairan tubuh. Ginjal mengatur keseimbangan asam basa dengan
mengekskresikan H+ ketika terjadi asam berlebih atau mengekskresikan HCO3- ketika
terjadi basa berlebih (Rhodes dan Bell, 2009) melalui pengaturan ion bikarbonat
(HCO3-) dan pembuangan sisa metabolisme yang bersifat asam. Ginjal juga berperan
dalam mengendalikan ekskresi ion hidrogen (H+), bikarbonat (HCO3-) dan amonium
(NH4+) serta memproduksi urine asam atau basa, tergantung pada kebutuhan tubuhnya
(Sloane, 2004).
e) Pengaturan osmolaritas cairan tubuh , Ekskresi ginjal
Dengan secara terpisah pengaturan pengeluaran air dan pengeluaran zat terlarut
dalam urin, ginjal mempertahankan osmolaritas darah relatif konstan mendekati 300
mOsm/L (Tortora, 2014). Osmol dengan mengubah ekskresi air, mempertahankan
volume ECF (Extra Cellular Fluid). Ekskresi ginjal meliputi sisa metabolisme protein
(ureum, kalium, fosfat, sulfur anorganik dan asam urat).
f) Gluconeogenesis.
Saat asupan karbohidrat dihentikan lebih dari setengah hari, tubuh kita akan
mengaktifkan glukoneogenesis dari sumber non karbohidrat (asam amino dari 11
protein dan gliserol dari trigliserida). Sebagian besar glukoneogenesis terjadi di hati,
namun bisa juga di ginjal, terutama selama puasa yang berkepanjangan (Eaton, 2009).
Ginjal dapat menggunkan asam amino glutamin untuk glukoneogenesis. Mereka
kemudian dapat melepaskan glukosa ke dalam darah untuk membantu menjaga kadar
gula darah normal (Tortora, 2014).

12
g) Pengaturan pH Darah
Ginjal mengekskresikan sejumlah ion hidrogen H+ ke dalam urin dan
mempertahankan ion karbonat (HCO3+), yang merupakan dapar penting dalam darah.
Kedua mekanisme ini menmbantu mengatur pH darah (Tortora, 2014). untuk
mempertahankan derajat keasaman/pH plasma sekitar 7,4 dengan mengeluarkan
kelebihan hidrogen dan membentuk kembali karbonat.
Fungsi non-ekskresi dari ginjal meliputi sintesis dan aktifasi hormon, mensekresi
renin yang memilliki peran penting dalam pengaturan tekanan darah, menghasilkan
eritropoetin yang berperan dalam merangsang produksi sel darah merah oleh
hematopoetik sumsum tulang. Salah satu rangsangan yang penting untuk sekresi
eritropoietin oleh ginjal adalah hipoksia. Pada manusia normal, ginjal menghasilkan
hampir semua eritropoietin yang disekresi ke dalam sirkulasi. Pada orang dengan
penyakit ginjal berat atau yang ginjalnya telah diangkat dan digantikan dengan
hemodialisis, timbul anemia berat sebagai hasil dari penurunan produksi eritropoietin.
(Guyton dan Hall, 2011). Mensekresi prostaglandin, yang berperan sebagai vasodilator
dan bekerja secara lokal serta melindungi dari kerusakan iskemik ginjal. Serta 1,25
dihidroksi vitamin D3 yang merubah vitamin D menjadi metabolit aktif yang
membantu penyerapan kalsium Sebagai fungsi organ non-ekskresi, ginjal juga
mendegradasi hormon polipeptida, insulin, glukagon, parathormon, prolaktin, hormon
pertumbuhan, ADH dan hormon gastrointestinal. (Price & Wilson, 2012).
2.2 Penyakit Ginjal Kronik (PGK)
2.2.1 Definisi Penyakit Ginjal Kronik
PGK didefinisikan sebagai kelainan pada struktur atau fungsi ginjal yang terjadi
selama 3 bulan atau lebih, dan berdampak bagi kesehatan. Kelainan skturktural
termasuk albuminuria lebih dari 30 mg/hari, hematuria atau sel darah merah pada urin,
elektrolit dan kelainan lain karena ganguan tubular (Wells et al., 2015). Penyakit ginjal
kronik merupakan suatu proses patofisiologi dengan etiologi yang beragam, dapat
mengakibatkan penurunan fungsi ginjal yang progresif, dan pada umumnya berakhir
dengan gagal ginjal (Suwitra, 2014)

13
Berdasarkan KDIGO Clinical Practice Guideline for the Evaluation and
Management of Chronic Kidney Disease (2013), definisi Penyakit Ginjal Kronik
terbagi menjadi 2 kriteria yaitu :
(1) Penyakit ginjal kronik didefinisikan sebagai kerusakan pada struktur atau fungsi
ginjal selama 3 bulan atau lebih dan ditetapkan dengan adanya abnormalitas
struktur dan fungsi ginjal, dengan atau tanpa adanya penurunan GFR. Dengan
manifestasi klinis berupa:
Abnormalitas patologi
Pertanda adanya kerusakan ginjal, termasuk abnormalitas pada komposisi darah
atau urin, atau abnormalitas dari gambaran tes (imaging test).
(2) Penyakit ginjal kronik merupakan suatu keadaan yang ditandai dengan Glomerular
Filtration Rate kurang dari 60mL/menit/1,73m2 selama 3 bulan atau lebih, dengan
atau tanpa adanya kerusakan ginjal.
Chronic Kidney Disease stage 5, disebut juga sebagai End Stage Renal Disease
(ESRD) atau penyakit ginjal stadium akhir dan terjadi kerusakan ginjal yang ditandai
dengan penurunan GFR di bawah 15mL/menit/1,73m2 atau pada pasien yang
menerima terapi penggantian ginjal dan dialisis jangka panjang (Dipiro et al., 2015).
Penyakit ginjal kronik merupakan salah satu penyakit yang menjadi masalah
kesehatan global yang menyebabkan fungsi organ ginjal mengalami penurunan hingga
akhirnya tidak mampu melakukan fungsinya dengan baik dalam hal penyaringan
pembuangan elektrolit tubuh, menjaga keseimbangan cairan dan zat kimia tubuh
seperti sodium dan kalium didalam darah atau produksi urin (NKF, 2016). Kerusakan
ginjal ini mengakibatkan kemampuan aktivitas kerja tubuh menjadi terganggu sehingga
kualitas hidup pasien juga menurun (Ali, 2017).
2.2.2 Klasifikasi Penyakit Ginjal Kronik
Berdasarkan KDIGO Clinical Practice Guideline for the Evaluation and
Management of Chronic Kidney Disease (2018), penyakit ginjal kronik dapat
diklasifikasikan berdasarkan penyebab, kategori GFR (G1-G5) dan kategori
albuminuria (A1-A3). Derajat PGK dan resiko progresivitasnya diklasifikasikan
sebagai berikut :

14
Tabel II.1 Kategori GFR pada penyakit ginjal kronik (KDIGO, 2012)
Kategori GFR GFR (ml/menit/1,73 m2) Keterangan Stadium
G1 ≥ 90 Normal atau tinggi Stadium 1
G2 60 – 89 Sedikit menurun* Stadium 2
G3a 45 – 59 Sedikit menurun
sampai cukup
menurun
Stadium 3
G3b 30 – 44 Cukup menurun
sampai sangat
menurun
Stadium 3
G4 15 – 29 Sangat menurun Stadium 4
G5 < 15 Gagal ginjal Stadium 5
Keterangan:
CKD (Chronic Kidney Disease)
GFR (Glomerular Filtration Rate)
*pada tingkat dewasa muda jika tidak adanya bukti kerusakan ginjal, baik kategori GFR G1 maupun G2
tidak memenuhi kriteria CKD.
Menurut Henry Ford Health Systems (2011) untuk perhitungan laju filtrasi
glomerulus dapat dihitung berdasarkan rumus Modification of Diet in Renal Disease
(MDRD) sebagai berikut:
eGFR (ml/menit/1,73m2) = 186 𝑥 (Serum Kreatinin)−1,154 x 𝑢𝑚𝑢𝑟−0,203 x (0,742
jika perempuan) x (1,212 jika African American)
Atau menggunakan rumus Cockroft-Gault sebagai berikut (Ahmed dan lowder, 2012):
GFR = (140−umur)x BB (Kg)x (0,85 jika perempuan)
72 x serum kreatinin
Dalam praktis klinis, GFR biasanya diperkirakan dengan menggunakan
konsentrasi serum kreatinin. Kreatinin merupakan produk yang dihasilkan
metabolisme otot, yang disaring secara bebas di glomerulus dan tidak dapat diserap
kembali ke dalam tubulus ginjal. Pada dasarnya semua kreatinin yang disaring dalam
glomerulus diekskresikan bersama urin daripada diserap kembali ke dalam darah. Oleh
karena itu, serum kreatinin dapat digunkaan untuk menilai GFR dan tingkat kerusakan
ginjal yang terjadi pada CKD (Porth, 2015)

15
Tabel II.2 Kategori albuminuria pada penyakit ginjal kronik (KDIGO, 2012)
Kategori AER
(mg/24 jam)
ACR
(mg/mmol)
Keterangan
A1 < 30 < 3 < 30 Normal
sampai sedikit
meningkat
A2 30 – 300 3 – 30 30 – 300 Cukup
meningkat*
A3 > 300 > 30 > 300 Sangat
meningkat**
Keterangan: AER: Albumin Excretion Rate; ACR: Albumin to Creatine Ratio
*Relatif terhadap tingkat dewasa muda
**Termasuk sindrom nefrotik (ekskresi albumin biasanya >2200mg/24jam [ACR >2220mg/g; >220 mg/mmol]
a. Penyakit Ginjal Kronik Stadium 1
Berdasarkan data National Health and Nutrition Examination Survey
(NHANES) di Amerika Serikat pada tahun 1999-2004 mengestimasi prevalensi CKD
pada stadium 1 sebesar 5,7% (Arora, 2016). Selama stadium ini ginjal masih berfungsi
secara normal tetapi ditemukan abnormalitas yang menunjukkan terjadinya gangguan
ginjal (KDOQI, 2012). Biasanya tidak terdapat gejala yang timbul tetapi terjadi
peningkatan tekanan darah bila dibandingkan dengan pasien yang bukan menderita
CKD. Pada pasien juga terjadi albuminuria (AIHW, 2014).
b. Penyakit Ginjal Kronik Stadium 2
Berdasarkan data National Health and Nutrition Examination Survey
(NHANES) di Amerika Serikat pada tahun 1999-2004 mengestimasi prevalensi CKD
pada stadium 2 sebesar 5,4% (Arora, 2016). Pada stadium ini, terjadi penurunan fungsi
ginjal dengan GFR sebesar 60-89 ml/menit/1,73 m2 (KDOQI, 2012). Terjadi
peningkatan tekanan darah pada stadium 2 (Suwitra, 2014). Kebanyakan pasien tidak
mengalami gejala tetapi, terjadi peningkatan tekanan darah dan pasien juga terjadi
albuminuria (AIHW, 2014).
(mg/g)

16
c. Penyakit Ginjal Kronik Stadium 3
Menurut survei yang dilakukan oleh National Health and Nutrition Examination
Survey (NHANES) prevalensi CKD stadium 3 terjadi peningkatan dari tahun 1988-
1994 sebanyak 18,8% menjadi 24,5% pada tahun 2003-2006 pada pasien dengan usia
lebih dari 70 tahun. Pada periode yang sama, prevalensi CKD pada usia 20-39 tahun
relatif sama yaitu dibawah 0,5%. Biasanya tidak terdapat gejala yang timbul atau
biasanya terjadi peningkatan frekuensi buang air kecil pada malam hari (nokturia) dan
kehilangan nafsu makan (AIHW, 2014). Pada stadium 3 terjadi komplikasi diantaranya
adalah hiperfosfatemia, hipokalsemia, anemia, hipertensi dan hiperparatiroid (Suwitra,
2014).
d. Penyakit Ginjal Kronik Stadium 4
Berdasarkan data National Health and Nutrition Examination Survey
(NHANES) di Amerika Serikat pada tahun 1999-2004 mengestimasi prevalensi PGK
pada stadium 4 sebesar 0,4% (Arora, 2016). Pada stadium 4 terjadi beberapa
komplikasi yaitu diantaranya malnutrisi, asidosis metabolik, hiperkalemia dan
dislipidemia (Suwitra, 2014) dan juga terjadi gejala seperti pada stadium 3 disertai
mual, kulit gatal, dan sesak nafas (AIHW, 2014).
e. Penyakit Ginjal Kronik Stadium 5
Berdasarkan data National Health and Nutrition Examination Survey
(NHANES) di Amerika Serikat pada tahun 1999-2004 mengestimasi prevalensi PGK
pada stadium 5 sebesar 0,4% (Arora, 2016). Pada stadium 5 terjadi penurunan GFR
>15 ml/menit/1,73 m2 (KDOQI, 2012). Gejala yang timbul seperti yang terjadi pada
stadium 5, tetapi terjadi komplikasi tambahan seperti peradangan lapisan jaringan pada
jantung, perdarahan pada saluran pencernaan, perubahan fungsi dan struktur otak,
gangguan atau perubahan struktural atau fungsional pada sistem saraf perifer (AIHW,
2014). CKD stadium 5 menyebabkan komplikasi gagal jantung dan uremia (Suwitra,
2014).

17
2.2.3 Epidemiologi Penyakit Ginjal Kronik
PGK merupakan salah satu masalah kesehatan dunia yang secara global
memilliki prevalensi dan insiden yang tinggi juga tingkat morbiditas dan mortalitasnya.
Menurut data WHO, penyakit ginjal kronik telah menyebabkan kematian pada 850.000
orang setiap tahunnya. Angka tersebut menunjukkan bahwa penyakit ginjal kronik
menduduki peringkat ke-12 tertinggi sebagai penyebab angka kematian dunia.
Berdasarkan Data The United State Renal Data System (2018), prevalensi terjadinya
PGK di Amerika kurang dari 15% atau sebesar lebih dari 30 juta orang. Pada tahun
2016, sekitar 124.675 dilaporkan kasus baru terkait dengan gagal ginjal stadium akhir.
Menurut Hill et al (2016) prevalensi global PGK sebesar 13,4% dengan 48% di
antaranya mengalami penurunan fungsi ginjal dan tidak menjalani dialisis dan
sebanyak 96% pasien dengan kerusakan ginjal atau fungsi ginjal yang berkurang, tidak
sadar bahwa mereka memiliki PGK. Penyakit ginjal kronik umumnya dialami individu
yang berusia lebih dari 60 tahun dan juga memiliki resiko tinggi terkena hipertensi,
diabetes mellitus serta penyakit kardiovaskular lainnya (Hudson & Wazny., 2014).
Berdasarkan dari data hasil Riset Kesehatan Dasar (2018), menunjukkan bahwa
prevalensi yang menderita penyakit ginjal kronik di Indonesia sebesar 3,8%. Jika
ditinjau berdasarkan tempat tinggal, masyarakat yang tinggal di perkotaan (3,85%)
lebih tinggi prevalensinya dibandingkan di perdesaan (3,84%). Provinsi dengan
prevalensi PGK tertinggi terdapat di provinsi Kalimantan Utara sebesar (6,4%), diikuti
oleh Maluku Utara, Sulawesi Utara , Gorontalo, hingga prevalensi PGK terendah
terdapat pada Sulawesi Barat sebesar (1,8%)
Gambar 2.3 Prevalensi PGK menurut karakteristik di Indonesia (Riskesdas,2018)

18
Jika ditinjau berdasarkan karakteristik jenis kelamin, prevalensi PGK pada laki-
laki (4,17%) lebih tinggi dibandingkan dengan perempuan (3,52%). Hal ini
dimungkinkan karena perempuan lebih memperhatikan kesehatan dan menjaga pola
hidup sehat dibandingkan dengan laki-laki, sehingga laki-laki lebih mudah terkena
penyakit ginjal kronik dibandingkan dengan perempuan (Arifa, 2017).
Berdasarkan karakteristik usia, prevalensi tertinggi pada kategori usia di atas 75
tahun (7,48%) dan terjadi peningkatan tajam pada kelompok usia 35-44 tahun.
Pertambahan usia juga akan mempengaruhi anatomi, fisiologi dan sitologi ginjal. Pada
usia 35-75 tahun, laju filtrasi glomelurus akan menurun secara progresif hingga 50%
dari keadaan normal sehingga terjadi penurunan kemampuan tubulus ginjal untuk
mereabsorpsi dan terjadi pemekatan urin. Selain itu, terjadi penurunan kemampuan
pengosongan kandung kemih. Sehingga, dapat meningkatkan resiko infeksi dan
obstruksi serta penurunan intake cairan yang merupakan faktor resiko terjadinya
kerusakan ginjal (Ali, 2017).
Berdasarkan strata pendidikan, prevalensi PGK tertinggi pada masyarakat yang
tidak atau belum pernah sekolah (5,73%). Semakin tinggi pendidikan seseorang maka
akan semakin cepat memahami tentang kondisi penyakit yang dialami. Kurangnya
pengetahuan dan kesadaran masyarakat untuk deteksi dini dalam memeriksakan
dirinya ke pusat pelayanan kesehatan menjadi penyebab meningkatnya pasien PGK
dikarenakan pada PGK stadium awal belum memperlihatkan gejala dan keluhan yang
spesifik. Kebanyakan pasien datang dengan keluhan yang sudah berat dan pada saat
dilakukan pemeriksaan lanjutan sudah berada pada stadium terminal (stadium 5)
(Arifa, 2017).
Berdasarkan pekerjaan, prevalensi tertinggi terjadi pada kelompok masyarakat
yang tidak bekerja (4,76%) dan diikuti oleh profesi lain seperti buruh/nelayan/petani
(4,64%), PNS/TNI/Polri/BUMN/BUMD (4,59%). Tanpa disadari pekerjaan dapat
menyebabkan penyakit ginjal kronik seperti pekerja kantoran yang duduk terus
menerus sehingga menyebabkan terhimpitnya saluran ureter pada ginjal. Selain itu,
intensitas aktivitas sehari-hari seperti orang yang bekerja di panasan dan pekerja berat

19
yang banyak mengeluarkan keringat lebih mudah terserang dehidrasi. Akibat dehidrasi,
urin menjadi lebih pekat sehingga bisa menyebabkan terjadinya PGK (Arifa, 2017).
Berdasarkan data yang diperoleh dari Indonesia Renal Registry (2016), sebanyak
98% penderita PGK menjalani terapi hemodialisis (HD) dan 2% menjalani terapi
peritoneal dialisis (PD). Pasien baru PGK terus mengalami peningkatan dari tahun ke
tahun. Penderita PGK yang mejalani hemodialisis di Indonesia pada tahun 2007-2015
tercatat sebanyak 30.554 pasien aktif, dan 21.050 merupakan pasien baru.
(Data diatas tahun diambil dari 249 unit)
Gambar 2.4 Prevalensi pasien baru dan pasien aktif PGK yang menjalani HD dari
tahun ke tahun (IRR, 2015)
Jumlah pasien baru terus meningkat dari tahun ke tahun , pasien baru adalah
pasien yang pertama kali menjalani dialisis pada tahun 2015 sedangkan pasien aktif
adalah seluruh pasien baik pasien baru tahun 2015 maupun pasien lama dari tahun
sebelumnya yang masih menjalani terapi hemodialisis rutin dan masih bertahan hidup
sampai dengan tanggal 31 Desember 2015. Pada diagram ini terlihat suatu perbedaan
dibandingkan tahun-tahun sebelumnya, pada tahun 2015 pasien aktif lebih banyak jika
dibandingkan dengan jumlah pasien baru , hal ini menunjukkan lebih banyak pasien
yang dapat menjalani hemodialisis lebih lama, dikarenakan adanya faktor jaminan
kesehatan national (JKN) yang berperan penting dalam menjaga kelangsungan terapi
pasien. .Jumlah pasien ini belum menunjukkan data seluruh pasien di Indonesia, akan

20
tetapi dapat dijadikan representasi dari kondisi saat ini (Data diatas tahun diambil dari
249 Unit).
2.2.4 Etiologi dan Faktor Resiko Penyakit Ginjal Kronik
PGK merupakan hasil dari proses patofisiologi yang beragam terkait dengan
kerusakan fungsi nefron yang diakibatkan dari adanya gangguan primer (penyakit
ginjal) maupun komplikasi sekunder dari penyakit tertentu misalnya hipertensi dan
diabetes mellitus yang akhirnya mengakibatkan kerusakan ginjal secara ireversibel
(Alldredge et al., 2013). Menurunnya fungsi ginjal sejalan dengan bertambahnya usia,
pada pasien lanjut usia yang mempunyai nilai GFR di bawah 50 mL/min disebabkan
oleh berkurangnya massa otot yang tidak memperlihatkan kenaikan dari serum
kreatinin (BPOM RI, 2015). PGK dapat disebabkan oleh 3 jenis faktor diantaranya
adalah faktor kerentanan, faktor inisiasi dan faktor progresi. Faktor kerentanan
merupakan faktor yang dapat meningkatkan resiko penyakit ginjal namun tidak secara
langsung menyebabkan kerusakan pada ginjal diantaranya adalah faktor usia lanjut,
berkurangnya massa ginjal, berat lahir rendah, riwayat keluarga, peradangan sistemik
dan dislipidemia. Faktor inisiasi dapat menyebabkan kerusakan ginjal secara langsung
dan dapat dimodifikasi dengan terapi farmakologis, diantaranya adalah diabetes
melitus, hipertensi, glomerulonefritis, penyakit ginjal polikistik, dan HIV nefropati.
Sedangkan faktor progresi merupakan faktor yang dapat mempercepat penurunan
fungsi ginjal setelah inisiasi dari kerusakan ginjal, termasuk faktor glikemia pada
penderita diabetes, hipertensi, proteinuria, dan hiperlipidemia (Dipiro et al., 2015).
Berdasarkan data Indonesia Renal Registry (2015), angka kejadian PGK
terbanyak di Indonesia disebabkan oleh faktor nefrosklerosis hipertensi yang
meningkat menjadi 43% dari tahun-tahun sebelumnya, diikuti oleh nefropati diabetika
sebesar 22%, glomerulopati primer 8%, pielonefritis kronik 7%, nefropati obstruksi
5%, nefropati asam urat 2%, nefropati lupus dan ginjal polikistik 1% dan lain-lain
sebanyak 8%.

21
Gambar 2.5 Diagram etiologi PGK di Indonesia tahun 2015 (IRR, 2015)
Hipertensi dan diabetes merupakan faktor risiko PGK yang paling banyak terjadi.
Secara keseluruhan, diabetes dan hipertensi menyumbang 72% penyebab ESRD.
Diketahui juga bahwa resistensi insulin, obesitas, riwayat keluarga, obstruksi saluran
kemih, berkurangnya massa ginjal, obat nefrotoksik (analgesik, aminoglikosida), berat
badan lahir rendah, preeklamsia, sosiodemografi (usia >55 tahun, jenis kelamin,
kurangnya akses ke pelayanan kesehatan), merokok, tingkat pendapatan/pendidikan
rendah, paparan bahan kimia berbahaya dan sindrom metabolik juga terlibat sebagai
faktor resiko PGK (Ford, 2011).
2.2.4.1 Hipertensi
Hipertensi dan PGK saling mempengaruhi. Hipertensi dapat menyebabkan PGK,
begitupun sebaliknya penyakit ginjal kronik dapat menyebabkan hipertensi. Hipertensi
yang berlangsung lama dapat mengakibatkan perubahan struktur pada arteriol di
seluruh tubuh, ditandai dengan adanya fibrosis dan hialinisasi dinding pembuluh darah.
Organ sasaran utamanya adalah jantung, otak, mata, dan ginjal. Pada ginjal,
arteriosklerosis akibat hipertensi lama menyebabkan nefrosklerosis. Gangguan ini
merupakan akibat langsung iskemia karena penyempitan lumen pembuluh darah
intrarenal. Penyumbatan arteri dan arteriol akan menyebabkan kerusakan glomerulus

22
dan atrofi tubulus, sehingga seluruh nefron rusak, yang menyebabkan terjadinya
penyakit ginjal kronik (Ekantari, 2012). Sekitar 90% hipertensi bergantung pada
volume dan berkaitan dengan retensi air dan natrium, sementara kurang dari 10%
bergantung pada renin. Renin disekresikan oleh ginjal sebagai respon terhadap
penurunan volume darah dan perfusi ginjal. Renin mengubah angiotensinogen
membentuk angiotensin I yang kemudian oleh ACE diubah menjadi angiotensin II
dimana angiotensin II merupakan vasokonstriktor yang kuat. Angiotensin II
menyebabkan sekresi aldosteron dan reabsorpsi natrium, sehingga menyebabkan
peningkatan tekanan darah (Hsueh dan Wyne, 2011). Secara klinik, pasien dengan
riwayat penyakit hipertensi mempunyai risiko mengalami PGK 3,2 kali lebih besar
daripada pasien tanpa riwayat penyakit dan faktor resiko hipertensi (Pranandari, 2012)
2.2.4.2 Diabetes
Diabetes merupakan faktor komorbiditas PGK yang tinggi dan sebesar 65%
pasien PGK yang menjalani hemodialisis dan meninggal memiliki riwayat penyakit
diabetes. Kadar gula dalam darah yang tinggi akan mempengaruhi struktur ginjal,
merusak pembuluh darah halus di ginjal (glomerulosklerosis noduler dan difus).
Kerusakan pembuluh darah menimbulkan kerusakan glomerulus yang berfungsi
sebagai penyaring darah. Dalam keadaan normal protein tidak melewati glomerulus
karena ukuran protein yang besar tidak dapat melewati lubang-lubang glomerulus yang
kecil. Namun karena kerusakan glomerulus, protein (albumin) dapat melewati
glomerulus sehingga dapat ditemukan dalam urin yang disebut dengan
mikroalbuminuria. Apabila jumlah atau dalam fungsi insulin mengalami defisiensi
(kekurangan) insulin, maka akan terjadi hiperglikemia. Hiperglikemia dapat
meningkatkan aktivasi RAAS (Hsueh dan Wyne, 2011) dan mengganggu autoregulasi
dalam glomerulus dengan mengaktifkan lokal intrarenal RAAS (Kanwar et al., 2011).
Faktor hemodinamik menyebabkan terganggunya Renin Angiotensin Aldosterone
System yang menimbulkan kelainan pada sel endotel pembuluh darah yang
mengaktivasi peningkatan hormon vasoaktif seperti angiotensin II (Sunaryanto, 2010).
Hal ini dapat meningkatkan tekanan kapiler glomerulus dan peregangan pada sel
mesangial dan kemudian mengaktifkan molekul sinyal seperti ROS (Reactive Oxygen

23
Species) dan menyebabkan disfungsi endotel (Kanwar et al., 2011). Disfungsi endotel
dan hilangnya kapiler glomerulus dan tubulointerstisial menyebabkan kerusakan epitel
dan menyebabkan progresivitas Diabetes Kidney Disease (DKD) (Reidy et al., 2014).
Apabila kondisi ini tidak dapat diatasi dan berlangsung terus menerus maka dapat
menyebabkan kematian (Arifa, 2017).
Komplikasi yang terjadi pada diabetes mellitus salah satunya adalah
makrovaskuler dan mikrovaskuler. Komplikasi makrovaskuler merupakan penyakit
yang timbul akibat diabetes yang menjadi penyebab utama kematian pada pasien
diabetes tipe 2 dan terjadi pada pembuluh darah besar yang terdapat di seluruh bagian
tubuh. Komplikasi yang sering dijumpai adalah penyakit jantung koroner (PJK), stroke,
trombosit otak (pembekuan darah pada sebagian otak), gagal jantung kongestif,
penyakit pembuluh darah perifer dan nefro-sklerosis (Effendi et al., 2015) . Sedangkan,
Komplikasi mikrovaskuler terjadi pada pasien dengan komplikasi yang diderita yaitu
nefropati diabetik yang merupakan penyebab kedua tersering penyakit ginjal stadium
akhir, diabetik retinopati (kebutaan), neuropati dan amputasi akibat luka diabetes yang
tidak terawat dengan baik akhirnya mengalami infeksi yang parah (PERKENI, 2015)
Secara klinik, riwayat penyakit diabetes melitus mempunyai pengaruh terhadap
kejadian PGK 4,1 kali lebih besar dibandingkan dengan pasien tanpa riwayat penyakit
dan faktor resiko diabetes melitus (Pranandari, 2012).
2.2.4.3 Glomerulonefritis
Glomerulonefritis merupakan penyakit peradangan ginjal. Peradangan dimulai
dalam glomerulus dan bermanifestasi sebagai proteinuria dan/atau hematuria.
Proteinuria merupakan indikasi dari hipertensi intraglomerular dan abnormalitas
permeabilitas glomerular. Keadaan ini biasanya dinterpretasikan sebagai pertanda
mulai terjadinya nefropati. Jumlah protein dalam urin mungkin bisa sangat banyak,
khususnya dalam nefrosis. Hal ini dapat menyebabkan hipoproteinemia yang dapat
menurunkan tekanan onkotik yang bisa menyebabkan edema karena akumulasi cairan
di jaringan (Barrett et al., 2012). Meskipun lesi terutama ditemukan pada glomerulus,
tetapi seluruh nefron pada akhirnya akan mengalami kerusakan, sehingga
mengakibatkan terjadinya CKD. Kematian yang diakibatkan oleh PGK umumnya

24
disebabkan oleh glomerulonefritis kronik yang merupakan kerusakan glomerulus
secara progresif lambat akibat glomerulonefritis yang sudah berlangsung lama (Price
et al., 2006). Glomerulonefritis ditandai dengan gomerular dan tubulointerstisial
fibrosis yang irreversibel dan progresif, akhirnya menyebabkan penurunan GFR dan
retensi racun uremik (Salifu et al., 2017). Glomerulonefritis dibagi menjadi 2 yaitu
glomerulonefritis akut, dan glomerulonefritis kronik. Glomerulonefritis akut dialami
sekitar 1-3 minggu setelah terinfeksi bakteri yang cukup parah seperti adanya
peradangan pada tenggorokan yang akan mereda setelah beberapa hari sedangkan
glomerulonefritis kronik terjadi dalam jangka waktu yang panjang dan bersifat
progresif dengan membrane filtrasi akan menebal dan akhirnya digantikan dengan
jaringan ikat, sehingga ginjal tidak dapat berfungsi dengan normal (Regan et al., 2016)
2.2.4.4 Obstruksi Saluran Kemih
Obstruksi yang diakibatkan oleh batu saluran kemih dapat menyebabkan
peningkatan tekanan intratubular yang diikuti oleh vasokonstriksi pembuluh darah
hingga mengakibatkan iskemik pada ginjal. Iskemik pada waktu yang lama dapat
menyebabkan glomeruloskerosis, atrofi tubulus dan fibrosis intertisial. Obstruksi
komplit pada ginjal selama 24 jam akan mengakibatkan kehilangan fungsi nefron
secara permanen sebanyak 15% (Arifa, 2017).
2.2.4.5 Pielonefritis
Pielonefritis adalah inflamasi atau infeksi akut pada pelvis renalis, tubula dan
jaringan interstisial. Penyakit ini terjadi akibat infeksi oleh bakteri enterit (paling
umum adalah Escherichia coli) yang telah menyebar dari kandung kemih ke ureter dan
ginjal akibat refluks vesikouretral. Infeksi ini akan merusak nefron, sel darah, dan
lengkung henle, sehingga mengakibatkan berkurangnya fungsi ginjal untuk mengatur
konsentrasi urin. Pielonefritis kronis dapat merusak jaringan ginjal secara permanen
akibat inflamasi yang berulang kali dan dapat menyebabkan terjadinya PGK. Proses
perkembangan kegagalan ginjal kronis dari infeksi ginjal yang berulang-ulang
berlangsung beberapa tahun atau setelah infeksi yang gawat.

25
2.2.4.6 Nefropati analgetik
Nefropati analgetik merupakan kerusakan nefron akibat penggunaan analgetik
dan OAINS yang berfungsi untuk menghilangkan rasa nyeri dan menekan radang
dengan mekanisme kerja menekan sintesis prostaglandin. Akibat penghambatan
sintesis prostaglandin, menyebabkan terjadinya vasokonstriksi renal, menurunkan
aliran darah ke ginjal dan berpotensi menimbulkan iskemia glomerular. Obat analgetik
dan OAINS juga menginduksi terjadinya nefritis interstisial yang selalu diikuti dengan
kerusakan ringan glomerulus dan nefropati yang akan mempercepat progresifitas
kerusakan ginjal, nekrosis papilla, dan PGK.
2.2.5 Patofisiologi Penyakit Ginjal Kronik
Gambar 2.6 Progresi Gagal Ginjal (Dipiro et al., 2015)
Pada awalnya patofisiologi PGK tergantung pada etiologi yang mendasarinya.
PGK dimulai ketika terjadinya pengurangan pada massa ginjal yang mengakibatkan
hipertrofi struktural. Fungsional nefron yang masih tersisa (surviving nephrons)
sebagai upaya kompensasi, yang diperantarai oleh molekul vasoaktif seperti sitokin
dan growth factors seperti transforming growth factor β (TGF- β). Hal ini
mengakibatkan terjadinya hiperfiltrasi, yang diikuti dengan terjadinya peningkatan

26
tekanan kapiler dan aliran darah glomerolus. Proses adaptasi ini berlangsung singkat,
namun pada akhirnya diikuti oleh proses maladaptasi berupa sklerosis ginjal yang
masih tersisa. Adanya peningkatan aktivitas renin-angiotensin-aldosteron intrarenal
juga ikut memberikan kontribusi terhadap terjadinya hiperfiltasi dan sklerosis ginjal
yang menyebabkan kerusakan perifer yang berlangsung secara progresif kronik
(Hudson, 2014). Bila terjadi penurunan fungsi ginjal secara progresif, maka akan
menyebabkan terjadinya penurunan GFR yang ditandai dengan peningkatan kadar urea
dan serum kreatinin sehingga berdampak pada terjadinya penyakit ginjal kronik
(Kovesdy, 2014). Beberapa hal juga dianggap berperan terhadap terjadinya
progresivitas PGK antara lain albuminuria, hipertensi, hiperglikemia, dan dislipidemia
(Hudson, 2014).
2.2.6 Manifestasi Klinik Penyakit Ginjal Kronik
Pada PGK stadium awal, terjadi kehilangan daya cadang ginjal (renal reserve)
serta keadaan LFG masih normal. Kemudian akan terjadi penurunan fungsi nefron
secara perlahan, ditandai dengan terjadinya peningkatan kadar ureum dan serum
kreatinin. Ketika LFG pasien berkisar antara 60-89%, pasien belum merasakan adanya
keluhan (asimtomatik) namun sudah terjadi peningkatan kadar ureum dan serum
kreatinin. Pasien mulai mengalami keluhan seperti nokturia, badan lemas, mual, nafsu
makan berkurang, dan penurunan berat badan ketika LFG pasien sebesar 30-59%.
Sampai pada kondisi LFG sebesar 15-29%, pasien menunjukkan gejala dan tanda
uremia seperti anemia, peningkatan tekanan darah, gangguan metabolisme fosfor dan
kalsium, pruritus, dan muntah. Selain itu, pasien juga mudah terkena infeksi (misalnya
infeksi saluran kemih, infeksi saluran nafas, maupun infeksi saluran cerna) serta terjadi
ketidakseimbangan air seperti hipovolemia atau hipervolemia dan ketidakseimbangan
elektrolit terutama pada natrium dan kalium. Pada saat LFG pasien PGK <15% maka
pasien akan menunjukkan gejala serta komplikasi yang lebih serius dan pasien
memerlukan terapi pengganti ginjal (kidney replacement) antara lain dialisis atau
transplantasi ginjal. Pada keadaan ini pasien sudah dikatakan masuk pada kategori
penyakit ginjal kronik stadium 5 (ESRD) (Hudson, 2014).

27
2.2.7 Komplikasi Penyakit Ginjal Kronik
2.2.7.1 Asidosis Metabolik
Pengaturan asam-basa dengan cara mengatur ekskresi ion-ion hidrogen dalam
tubuh merupakan salah satu peran penting dari ginjal. Akibat hilangnya kemampuan
ginjal untuk mengeluarkan asam dan memproduksi basa menyebabkan terjadinya
asidosis metabolik. Selain itu, akumulasi dari fosfat, sulfat, dan anionanion lain yang
tidak terekskresi dengan baik oleh ginjal juga dapat menyebabkan terjadinya anion gap
yang memicu terjadinya asidosis metabolik (Perlman et al., 2014).
Pada pasien PGK, semua ion bikarbonat (HCO3-) yang difiltrasi akan
direabsorpsi, namun kemampuan ginjal untuk mensistesis ammonia (𝑁𝐻4 +)
terganggu dan dapat berkembang menjadi asidosis metabolik. Asidosis metabolik
ditandai dengan penurunan tingkat serum bikarbonat (HCO3-) sejumlah 15-20 mEq/L
dan pH plasma. Umumnya kondisi ini terlihat pada pasien PGK dengan GFRnya
menurun < 20-30 mL/menit (Hudson, 2014). Konsekuensi klinis asidosis metabolik
dari CKD termasuk osteopenia, potensi memperburuk hiperparatiroidisme sekunder,
mengurangi cadangan pernafasan dan melemahkan sistem buffer tubuh, dan penurunan
aktivitas Na+ , K+-ATPase pada sel darah merah dan sel-sel miokard, yang dapat
menyebabkan penurunan kontraktilitas miokard dan gagal jantung kongestif (Kovesdy,
2012). Terjadinya asidosis metabolik terutama disebabkan hilangnya massa ginjal.
Kegagalan fungsi ekskresi ginjal yang menyebabkan pengumpulan asam di dalam
darah (tubuh menghasilkan asam yang berlebih) sehingga menyebabkan terjadinya
asidosis metabolik.
Ginjal berperan dalam pengaturan kesimbangan asam basa. Seiring dengan
penurunan fungsi ginjal, reabsorpsi bikarbonat dipertahankan, namun eksresi 18
hidrogen berkurang karena kemampuan ginjal menghasilkan amonia terganggu,
sehingga terjadi akumulasi ion hidrogen. Gangguan keseimbangan H+ menyebabkan
asidosis metabolik, yang ditandai dengan tingkat bikarbonat serum 15 sampai 20
mEq/L, dan peningkatan anion lebih besar dari 17 mEq/L, meghasilkan pH kurang dari
7,35. Asidosis metabolik umumnya muncul saat GFR menurun di bawah 25
mL/menit/1,73 m2 (Schonder et al., 2016).

28
2.2.7.2 Anemia
Anemia merupakan komplikasi yang biasa terjadi pada pasien penyakit ginjal
kronik (Wagner, Tata dan Fink, 2016). Menurut KDIGO (2018), anemia adalah kondisi
kadar hemoglobin (Hb) pasien <13 g/dL untuk laki-laki dewasa dan <12 g/dL untuk
perempuan dewasa. Anemia pada pasien PGK biasanya dimulai saat stadium 3 yaitu
ketika GFR 30-59 mL/menit/1,73 m2. Pasien PGK yang mengalami anemia pada
stadium 3 sebanyak 42%; pada stadium 4 sebanyak 54% dan pada stadium 5 sebanyak
76% (Henry Ford, 2011).
Pada pasien PGK, penyebab utama anemia adalah terjadi penurunan produksi
eritropoietin oleh ginjal sehingga menyebabkan stimulasi eritropoiesis menjadi
menurun. Peningkatan besi dibutuhkan ketika produksi sel darah merah dirangsang
oleh suatu Erythropoietin Stimulating Agent (ESA) seperti epoetin alfa. Namun
umumnya defisiensi besi terjadi pada pasien PGK dan merupakan penyebab utama
resistensi terhadap ESA. Untuk mencegah dan memperbaiki defisiensi besi tersebut,
maka sering dibutuhkan suplementasi zat besi. Faktor lain yang dapat menyebabkan
anemia pada PGK adalah berkurangnya umur sel darah merah. Secara normal, umur
sel darah merah adalah 120 hari, namun pada pasien PGK (terutama stadium 5) terjadi
penurunan menjadi 60 hari. Selain itu juga terjadi kekurangan vitamin B12 dan asam
folat, kehilangan darah akibat pengujian laboratorium dan hemodialisis (Hudson, 2014;
McPhee, 2006).
Anemia kronik ditandai dengan adanya rasa lelah, gangguan kardiovaskular dan
fungsi kognitif, gangguan tidur, dan peningkatan kebutuhan trasnfusi sel darah merah
(Hermanson et al., 2016). Hal-hal lain yang ikut berperan dalam terjadinya anemia
adalah defisiensi besi kehilangan darah misalnya terjadi pada pendarahan saluran cerna
serta hematuria, masa hidup eritrosit yang pendek akibat hemolisis, defisiensi asam
folat, penekanan sumsum tulang oleh substansi uremik proses inflamasi akut masupun
kronik (Suwitra, 2014).

29
2.2.7.3 Ketidakseimbangan Natrium-Air
Ginjal berperan penting dalam menjaga keseimbangan natrium dan air. Kadar
Na+ normal di dalam tubuh adalah 130-147 mEq/L (Henry Ford, 2011). Karena pada
pasien PGK fungsi ginjal terganggu dan menyebabkan terjadinya ketidakseimbangan
elektrolit, maka pasien PGK umumnya mengalami kelebihan Na+ dan air yang
disebabkan karena hilangnya rute ekskresi garam dan air melalui ginjal. Kondisi Na+
dan air yang berlebih dapat terjadi tanpa menunjukkan tanda-tanda. Namun apabila
kelebihan Na+ berlangsung secara terus menerus, maka dapat menyebabkan terjadinya
gagal jantung, hipertensi dan edema perifer. Sementara itu kelebihan air dapat
menyebabkan terjadinya hiponatremia (Perlman et al., 2014), sedangkan hipernatremia
merupakan peningkatan konsentrasi natrium lebih dari 145 mmol/L yang disebabkan
karena kelebihan aldosterone sehingga menyebabkan retensi natrium belebih.
2.2.7.4 Uremia
Uremia merupakan salah satu komplikasi yang disebabkan karena PGK.
Umumnya uremia terjadi karena beberapa faktor yaitu 1) retensi senyawa-senyawa
yang pada keadaan normal dieksresi oleh ginjal, misalnya sisa metabolime protein yang
mengandung senyawa nitrogen, 2) peningkatan hormon tertentu, dan 3) berkurangnya
produksi hormon oleh ginjal, misalnya eritropoietin (Perlman et al., 2014).
Gejala uremia ditandai dengan kelelahan, lemah, sesak napas, mual, muntah.
Umumnya tidak muncul pada PGK stadium 1 dan 2, dan akan terjadi pada pasien PGK
stadium 5 dengan tanda dan gejala uremia didasarkan pada keputusan untuk
menerapkan RRT (Renal Replacement Therapy) (DiPiro et al., 2015).
2.2.7.5 Mineral and Bone Disorder dan Osteodistrofi Ginjal
Pada pasien PGK, umum terjadi gangguan metabolisme mineral dan tulang serta
kelainan pada hormon paratiroid, kalsium, fosfor dan vitamin D. Digambarkan sebagai
karakteristik statik hiperparatiroidisme sekunder dan osteodistrofi ginjal. Evaluasi awal
terhadap kondisi Mineral and Bone Disorder pada pasien PGK adalah menilai dan
menetapkan tingkat dasar Ca2+, P, PTH, vitamin D, alkalin fosfatase dan serum HCO3
(Ford, 2011).

30
Ketika terjadi penurunan fungsi ginjal maka akan terjadi penurunan ekskresi
fosfor yang mengakibatkan hiperfosfatemia di dalam tubuh dan disertai dengan
penurunan konsentrasi serum kalsium secara timbal balik. Sebagai respon terhadap
peningkatan kadar fosfat dan penurunan konsentrasi kalsium maka kelenjar paratiroid
akan mengeluarkan hormon paratiroid. Peningkatan hormon paratiroid dapat
menyebabkan deplesi kalsium tulang dan berakibat timbulnya osteomalasia dan
osteoporosis. Selain itu, ketika PGK berkembang, proses aktivasi vitamin D menjadi
terganggu dan menyebabkan berkurangnya penyerapan kalsium dalam usus serta
memburuknya hiperparatiroidisme. Jumlah vitamin D dan reseptor penginduksi
kalsium yang lebih sedikit menyebabkan perkembangan osteodistrofi ginjal (Hudson,
2014).
Pada fungsi ginjal yang normal, 90% fosfat plasma difiltrasi dan diekskresi. Pada
CKD terjadi CKD-MBD disorder (termasuk hiperparatiroidisme sekunder,
hiperfosfatemia, penurunan absorpsi kalsium dan kelainan metabolisme vitamin D)
(Carla, 2016). Progresivitas CKD menyebabkan perubahan metabolisme mineral
tulang. Serum paratiroid hormon (PTH) sebagai indikator penyakit tulang pada CKD,
dapat dimulai dengan GFR turun dibawah 70 ml/menit/1,73 m2 (Chauhan, 2012).
Paratiroid hormon (PTH) diatur dengan negative feedback dengan serum kalsium.
Serum kalsium yang rendah menstimulasi kelenjar paratiroid untuk mensekresi PTH,
sebaliknya peningkatan serum kalsium dapat menghambat sekresi PTH. Namun pada
pasien CKD, osteosit dan osteoblas mensekresikan peningkatan fibroblast growth
factor 23 (FGF23). FGF23 mempertahankan kadar serum fosfat normal dengan
mengurangi absorpsi fosfat pada usus kecil dengan menurunkan produksi vitamin D
(kalsitriol). Mekanisme ini mempertahankan serum kalsium dan fosfor normal pada
awal CKD hingga GFR turun dibawah 50 ml/min/1,73 m2 . Saat terjadi penurunan
GFR hingga stadium 3,60% pasien terjadi peningkatan PTH. Hal ini merangsang
nefron untuk mengeskresi fosfor dan merangsang tulang untuk melepaskan kalsium.
PTH juga merangsang tubulus proksimal pada ginjal untuk menghasilkan kalsitriol
untuk meningkatkan kadar kalsium dan melawan FGF23. Namun meskipun
meningkatnya kadar PTH, kemampuan ginjal untuk mengaktifkan vitamin D

31
berkurang karena hilangnya fungsi nefron. Bila GFR terus menurun maka mekanisme
adaptif tidak mampu lagi mempertahankan homeostasis kalsium-fosfor dan akhirnya
terjadi hiperfosfatemia dan hiperparatiroid sekunder (Carla, 2016)
2.2.7.6 Hipoalbuminemia
Hipoalbuminemia merupakan kondisi dimana terjadi penurunan serum albumin
hingga dibawah 3,5 g/dl, namun signifikai secara klinis nampak ketika kadar serum
albumin dibawah 2,5 g/dL (Gatta et al., 2012). Hipoalbuminemia dapat disebabkan
oleh penurunan sintesis, yaitu pada keadaan malnutrisi dan penyakit hati, proses
degradasi yang berlebihan pada kondisi nefrosis dan gastrointestinal, atau peningkatan
kehilangan albumin dari vaskular pada keadaan syok dan edema. Kadar albumin
plasma < 2 g/dl sering dijumpai pada sindroma nefrotik, gastroenteropati dan sepsis,
sedangkan kadar 2-2,3 g/dl sering didapatkan pada pasien sirosis hati dan
glomerulonefritis, dan kadar 2,3-3 g/dl dijumpai pada reaksi fase akut, hepatitis virus,
malnutrisi, carcinoma, arthritis rematik, dan infeksi berat (Susetyowati et al., 2017).
2.2.7.7 Hiperkalemia
Hiperkalemia merupakan komplikasi umum yang sering terjadi pada pasien
ESRD dan berpotensi mengancam jiwa dikarenakan terjadi penurunan ekskresi kalium
(K+) di ginjal (Apel et al., 2014). Bila kadar K+ serum mencapai sekitar 7 mEq/L,
maka dapat menyebabkan terjadinya disaritmia yang serius bahkan henti jantung
(McPhee, 2006). Pada Pasien PGK terjadi penurunan GFR akibat dari kemampuan
ginjal yang tidak mampu mempertahankan kadar serum kalium (Kovesdy, 2014). Pada
tubulus ginjal kalium dapat direabsorbsi namun tidak mampu untuk diekskresi
sehingga terjadi penumpukan kalium di dalam darah. kelainan distribusi kalium terlihat
selama asidosis metabolik, defisiensi insulin, defisiensi aldosteron, antagonis
adrenergik, dan kerusakan jaringan. Selama mengalami asidosis metabolik maka akan
terjadi pergeseran kalium dari intraseluler menuju ke ekstraseluler sehingga terjadi
ketidakseimbangan antara keduanya dan menyebabkan hiperkalemia pada pasien
(Mushiyakh, 2011)

32
2.2.7.8 Hipokalemia
Management of Hypokalaemia Clinical Guideline, 2019 mendefinisikan
hipokalemia sebagai konsentrasi serum kalium <3,5 mmol / L sedangkan jika
konsentrasi kalium <2,5 mmol / L maka disebut dengan hipokalemia berat.
Hipokalemia dapat disebabkan oleh Asupan kalium makanan yang kurang, terjadi
gastrointestinal dan penurunan fungsi ginjal, serta obat-obatan yang dapat
menyebabkan hipokalemia misalnya diuretik tiazid (Bendroflumethiazide) dan loop
diuretik (furosemide).
Manifestasi klinik yang dialami oleh pasien hipokalemia tergantung pada tingkat
keparahan pengurangan kalium. Pasien dengan kadar kalium 3.0 - 3.5 mmol / L
biasanya tidak mengalami gejala yang tampak jelas, tetapi gejalanya mungkin termasuk
aritmia, kelemahan, konstipasi, mual, kram otot dan kelelahan, perubahan EKG dapat
mencakup gelombang T datar atau terbalik, depresi segmen ST dan gelombang U yang
menonjol, sedangkan kadar kalium 2.5 - < 3.0 mmol / L mengalami gejala yang tampak
lebih jelas, juga terjadi nekrosis otot dan aritmia pada pasien dengan masalah jantung,
sedangkan jika kadar kalium < 2.5 mmol / L tampak jelas terjadi aritmia jantung,
kelumpuhan kaki dan otot pernapasan, rhabdomiolisis, ileus, mioglobinuria, serta gagal
ginjal akut.
2.2.8 Pemeriksaan Fungsi Ginjal
Pemeriksaan terhadap fungsi ginjal sangat penting dilakukan untuk
mengidentifikasi sedini mungkin adanya penyakit ginjal agar penatalaksanaan dapat
diberikan secara efektif. Pengukuran fungsi ginjal terbaik adalah dengan cara
mengukur laju filtrasi glomerulus (LFG). Pengukuran LFG tidak dapat dilakukan
secara langsung, namun hasil estimasinya dapat dinilai melalui bersihan ginjal dari
suatu penanda filtrasi, salah satunya serum kreatinin. Serum kreatinin tidak dapat
digunakan sebagai satu-satunya faktor dalam memprediksi fungsi ginjal seseorang
karena dapat dipengaruhi oleh banyak hal, diantaranya: ras, diet, umur, jenis kelamin,
konsumsi obat dan lain-lain. Meskipun begitu, pemeriksaan serum kreatinin masih
dilakukan karena relatif mudah dan murah. Pertambahan usia seseorang dapat

33
menurunkan bersihan kadar serum kreatinin yang menggambarkan penurunan pada
fungsi ginjal.
Ada beberapa metode pemeriksaan yang dapat digunakan untuk mengevaluasi
fungsi ginjal. Metode pemeriksaan yang dilakukan adalah denganmengukur zat sisa
metabolisme tubuh yang diekskresikan melalui ginjal seperti ureum dan kreatinin
(Riskesdas, 2013).
2.2.8.1 Pemeriksaan Kadar Ureum
Ureum adalah produk akhir dari katabolisme protein dan asam amino yang
diproduksi oleh hati dan didistribusikan melalui cairan interseluler dan ekstraseluler ke
dalam darah untuk kemudian difiltrasi oleh glomerulus. Pengukuran ureum serum
dapat digunakan untuk mengevaluasi fungsi ginjal, menilai progresivitas penyakit
ginjal, dan menilai hasil hemodialisis. Kadar urea nitrogen dapat dikonversi menjadi
ureum dengan persamaan:
1 mg urea
dL𝑥
1mmol urea
14 mg N𝑥
1 mmol urea
2 mmol N𝑥
60 mg urea
1 mmol urea
= 2,14 𝑚𝑔 𝑢𝑟𝑒𝑎 𝑑𝑙
Ureum dapat diukur dari bahan pemeriksaan plasma, serum, ataupun urin.
Peningkatan ureum dalam darah disebut azetomia. Kondisi gagal ginjal yang ditandai
dengan kadar ureum plasma yang sangat tinggi dikenal dengan istilah uremia.keadaan
ini dapat berbahaya dan memerlukan hemodialisis atau transplantasi ginjal.
Peningkatan kadar urea plasma dapat menunjukkan adanya penurunan fungsi ginjal
karena ekskresi urea dalam urin menurun. (Verdiansah, 2016).
Tabel II.3 Nilai Rujukan Kadar Ureum (Verdiansah, 2016)
Spesimen Nilai Rujukan
Plasma atau Serum 6-20 mg/dl 2,1 – 7,1 mmol urea/hari
Urin 24 jam 12-20 g/hari 0,43 – 0,71 mmol urea/hari

34
2.2.8.2 Pemeriksaan Kadar Kreatinin
Kreatinin adalah hasil pemecahan keratin fosfat otot yang diproduksi oleh tubuh
secara konstan tergantung pada massa otot. Kadar kreatinin relatif stabil karena tidak
dipengaruhi oleh protein dari diet. Ekskresi kreatinin dalam urin dapat diukur dengan
menggunakan bahan urin yang dikumpulkan selama 24 jam. The National Kidney
Disease Education program merekomendasikan penggunaan serum kreatinin untuk
mengukur kemampuan LFG yang bermanfaat untuk memantau perjalanan penyakit
ginjal. Diagnosis PGK dapat ditegakkan ketika nilai serum kreatinin meningkat di atas
nilai rujukan normal. Peningkatan serum kreatinin dalam darah dapat menyebabkan
terjadinya peningkatan filtrasi kreatinin dari darah ke dalam urin. Pada keadaan gagal
ginjal dan uremia, ekskresi kreatinin oleh glomerulus dan tubulus ginjal menurun
(Verdiansah, 2016).
f. Klirens Kreatinin
Klirens zat merupakan volume plasma yang dibersihkan dari zat tersebut dalam waktu
tertentu. Klirens kreatinin merupakan pengukuran GFR yang tidak absolut karena
sebagian kecil kreatinin direabsorpsi oleh tubulus ginjal dan sekitar 10% kreatinin urin
disekresikan oleh tubulus. Namun, pengukuran klirens kreatinin dapat memberikan
informasi mengenai perkiraan nilai GFR (Verdiansah, 2016)
𝐶𝑐𝑟 =𝑈𝑐𝑟 (
𝑚𝑔𝑑𝐿 ) 𝑥𝑉𝑢𝑟(
𝑚𝐿24 𝑗𝑎𝑚)
𝑃𝑐𝑟 (𝑚𝑔𝑑𝐿 ) 𝑥
1440 𝑚𝑒𝑛𝑖𝑡24 𝑗𝑎𝑚
𝑥1,73
𝐴
Keterangan:
Ccr : Klirens kreatinin
Ucr : Kreatinin urin
Vur : Volume urin dalam 24 jam
Pcr : Kadar urin dalam 24 jam
1,73/A : Faktor luas permukaan tubuh
Nilai Rujukan:
Laki-laki : 97 mL/menit - 137 mL/menit per 1,73 m2
Perempuan : 88 mL/menit - 128 mL/menit per 1,73 m2

35
g. Estimated Glomerular Filtration Rate (eGFR)
The National Kidney Foundation merekomendasikan bahwa estimated GFR
dapat diperhitungkan sesuai dengan serum kreatinin, usia, berat badan dan jenis
kelamin (persamaan Cockcroft and Gault) (Verdiansah, 2016).
𝐺𝐹𝑅 𝑚𝑙/ min =(140 − 𝑢𝑠𝑖𝑎)𝑥 𝑊𝑒𝑖𝑔ℎ𝑡 (𝑘𝑔)
72 𝑥 𝑆𝑐𝑟 (𝑚𝑔𝑑𝐿 )
𝑥 (0,45 𝑝𝑎𝑑𝑎 𝑝𝑒𝑟𝑒𝑚𝑝𝑢𝑎𝑛
Tabel II.4 Nilai Rujukan Kadar Kreatinin (Verdiansah, 2016)
Populasi Sampel Metode Jaffe
Metode Enzimatik
Pria Dewasa Plasma atau
serum
0,9-1,3 mg/dL
(80-115μmol/L)
0,6-1,1 mg/dL
(55-96μmol/L)
Wanita Dewasa Plasma atau
serum
0,6-1,1 mg/dL
(53-97μmol/L)
0,5-0,8 mg/dL
(40-66μmol/L)
Anak Plasma atau
serum
0,3-0,7 mg/dL
(27-62μmol/L)
0,0-0,6 mg/dL
(0-52μmol/L)
Pria Dewasa Urin 24 jam 800-2000 mg/hari
(7,1-17,7 mmol/hari)
Wanita Dewasa Urin 24 jam 600-1800 mg/hari
(5,3-15,9 mmol/hari)
2.2.9 Penatalaksanaan Terapi
2.2.9.1 Tahap Pertama (Konservatif)
Terapi tahap pertama (konservatif) pada pasien PGK bertujuan untuk
memperlambat progresivitas gangguan fungsi ginjal (Dipiro et al., 2015). Pada tahap
ini dilakukan observasi untuk menentukan penyebab utama dari PGK dan menyelidiki
setiap faktor yang masih reversibel diantaranya adalah:

36
- Penurunan volume cairan ekstrasel karena penggunaan diuretik yang berlebihan
atau pembatasan garam yang terlalu ketat.
- Obstruksi saluran kemih akibat batu, pembesaran prostat atau fibrosis
retroperitoneal.
- Infeksi, terutama infeksi saluran kemih.
- Obat-obatan yang nefrotoksik, seperti aminoglikosida, obat antitumor, obat
antiinflamasi nonsteroid.
- Hipertensi berat atau maligna
1) Pengaturan Diet Protein
Pengaturan terhadap asupan protein berpengaruh terhadap penurunan
progresivitas PGK. Selain mengurangi kadar Blood Urea Nitrogen (BUN), namun juga
dapat mengurangi asupan kalium, fosfat dan produksi ion hidrogen yang berasal dari
hasil metabolisme protein toksik. Asupan rendah protein juga dapat mengurangi beban
ekskresi terhadap ginjal sehingga dapat menurunkan hiperfiltrasi glomerulus.
Rekomendasi klinis terbaru mengenai jumlah protein yang diperbolehkan untuk pasien
PGK adalah 0,6 g/kg/hari. Dilakukan juga monitoring terhadap status nutrisi pasien
agar dapat memastikan berat badan dan serum albumin tetap stabil (Kandarini, 2018).
2) Pengaturan Diet Kalium
Hiperkalemia merupakan komplikasi umum yang sering terjadi pada kondisi
ESRD. Pengaturan terhadap asupan kalium memiliki peranan penting terkait hal
tersebut. Adapun rekomendasi klinik mengenai jumlah kalium yang diperbolehkan
untuk pasien PGK adalah 40-80 mEq/hari. Tidak memberikan obat-obatan atau
makanan yang mengandung tinggi kalium juga dapat membantu menghindari kondisi
hiperkalemia. Pada pasien yang menerima hemodialisis dan dialisis peritoneal,
konsentrasi kalium juga dapat diatur dalam dialisat untuk mengatasi kondisi
hiperkalemia yang dialami pasien (Hill, 2016).

37
3) Pengaturan Diet Natrium dan Cairan
Pada kondisi PGK umum terjadi ketidakseimbangan elektrolit, salah satunya
adalah peningkatan kadar Na+. Untuk mengatasi hal tersebut, diperlukan adanya suatu
pengaturan diet natrium dan air. Rekomendasi klinik mengenai jumlah natrium yang
diperbolehkan untuk pasien PGK adalah 40-90 mEq/hari (1-2 g natrium), namun
asupan natrium yang optimal tetap harus ditentukan secara individual pada setiap
pasien. Asupan natrium yang berlebih dapat menyebabkan terjadinya retensi cairan,
edema perifer, edema paru, hipertensi dan gagal jantung kongestif (Kandarini, 2018).
Menurut Suwitra (2014), prinsip penatalaksanaan PGK meliputi :
1) Terapi spesifik terhadap penyakit dasarnya
Waktu yang paling tepat untuk terapi penyakit dasarnya adalah sebelum
terjadinya penurunan LFG, sehingga perburukan terhadap fungsi ginjal tidak terjadi.
Ukuran ginjal yang masih normal pada pemeriksaan ultrasonografi, biopsi dan
histopatologi dapat menentukan indikasi yang tepat terhadap terapi spesifik.
Sebaliknya, bila terjadi penurunan LFG hingga 20-30% dari normal, terapi terhadap
penyakit dasar sudah tidak banyak bermanfaat (Suwitra, 2014).
2) Pencegahan dan terapi terhadap kondisi komorbid
Mengikuti dan mencatat kecepatan penurunan LFG pada pasien PGK merupakan
hal yang sangat penting dikarenakan dapat mengetahui kondisi komorbid yang dapat
memperburuk keadaan pasien, diantaranya adalah gangguan keseimbangan cairan,
hipertensi yang tidak terkontrol, infeksi dan obstruksi traktus urinarius, obat-obat
nefrotoksik, atau peningkatan aktivitas penyakit dasarnya (Suwitra, 2014).
3) Menghambat perburukan fungsi ginjal
Hiperfiltrasi glomerulus merupakan faktor utama penyebab perburukan fungsi
ginjal. Pengurangan hiperfiltrasi glomerulus dapat dilakukan dengan cara pengaturan
diet dengan jumlah kalori 30-35 kkal/kgBB/hari, pengaturan asupan karbohidrat 50-
60% dari kalori total dan pengaturan asupan lemak 3040% dari kalori (Suwitra, 2014).

38
4) Pencegahan dan terapi terhadap penyakit kardiovaskular
Dikarenakan 40-45% kematian pada PGK disebabkan oleh penyakit
kardiovaskular, maka pencegahan dan terapi terhadap penyakit kardiovaskular
merupakan hal yang penting. Hal ini dapat dilakukan dengan melakukan pengendalian
diabetes, hipertensi, dislipidemia, anemia, hiperfosfatemia, serta terapi terhadap
kelebihan cairan dan gangguan keseimbangan elektrolit (Suwitra, 2014).
5) Terapi pengganti ginjal (replacement kidney)
Terapi pengganti ginjal dilakukan pada PGK stadium akhi dengan GFR kurang
dari 15 ml/menit. Ada 2 jenis terapi pengganti ginjal yaitu dialisis dan transplantasi.
Untuk dialisis, terdapat 2 metode yaitu hemodialisis dan peritoneal dialisis.
Hemodialisis merupakan suatu cara untuk mengeluarkan produk sisa metabolisme
melalui membran semipermeabel. Sedangkan, peritoneal dialisis merupakan proses
dialisis yang bekerja sebagai tempat menampung cairan dialisis dan peritoneum
sebagai membran semipermeable. Pemilihan metode dialisis tergantung pada kondisi
pasien (Price et al, 2005)
2.2.9.2 Penatalaksanaan Terapi Terhadap Komplikasi
1) Hipertensi
Kontrol tekanan darah secara optimal merupakan tindakan yang dapat dilakukan
untuk menurunkan laju progresivitas PGK. KDIGO (2018) merekomendasikan jika
ekskresi albumin urin setara atau <30 mg/24 jam maka target tekanan darah adalah
140/90 mmHg untuk mengurangi perkembangan PGK dan morbiditas mortalitas
penyakit kardiovaskular. Sedangkan jika ekskresi albumin urin >30 mg/24 jam atau
setara (albuminuria) maka target tekanan darah adalah 130/80 mmHg (Lukela et al.,
2014).
Pada kondisi hipertensi dengan GFR > 20 mL/min/1,73 m2, terapi lini pertama
yang dapat dilakukan yaitu dengan pemberian obat anti hipertensi golongan
Angiotensin Converting Enzim Inhibitor (ACEI) atau Angiotensin II Receptor Blocker
dengan cara memblokade RAAS untuk mencegah dan menurunkan laju progresivitas
PGK ke tahap stadium akhir (ESRD). Terapi kombinasi ACEI dan ARB harus
dipertimbangkan kembali, hanya untuk pasien dengan kondisi albuminuria berat (>1

39
g/hari) (Lukela et al., 2014). Jika diperlukan, ARB atau ACEI dapat dikombinasikan
dengan golongan thiazide untuk mengurangi proteinuria. Selain itu, dapat juga
diberikan obat anti hipertensi golongan Non Dihydropyridine Calcium Channel
Blocker (CCB) yang digunakan sebagai obat antiproteinurik lini kedua. Pengobatan
harus dimulai dengan dosis serendah mungkin kemudian diikuti dengan peningkatan
secara bertahap untuk mencapai target tekanan darah dan untuk meminimalkan
proteinuria (Dipiro et al., 2015). Selain itu, tekanan darah pasien PGK dapat juga
dikontrol dengan hemodialisis (Ali, 2017).
Tabel II.5 Obat anti hipertensi pada terapi PGK (Lukela, 2014)
Nama Obat Generik Rentang Dosis
Angiotensin Converting Enzim Inhibitor (ACEI)
Enalapril 5-40 mg/hari (terbagi 12-24 jam)
Captopril 25-50 mg/hari (terbagi 8-12 jam)
Ramipril 2,5-20 mg/hari (terbagi 12-24 jam)
Lisinopril 10-40 mg/hari (24 jam)
Angiotensin II Receptor Blocker (ARB)
Losartan 50-100 mg/hari (24 jam)
Irbesartan 150-300 mg/hari (24 jam)
Valsartan 80-320 mg/hari (24 jam)
Calcium Channel Blocker (CCB)
Amlodipin 5-10 mg (24 jam)
Verapamil 80-120 mg (8 jam)
Diltiazem 30-90 mg (6 jam)
Nifedipin 10 (8 jam)

40
2) Anemia
Pemberian terapi Erythropoietic-Stimulating Agent (ESA) merupakan terapi
awal yang diterima pasien PGK dengan kadar Hb antara 9-10 g/dL, sehingga perlu
dilakukan koreksi Hb terlebih dahulu sebelum diberikan terapi ESA. Pengobatan
anemia dengan ESA sering mengalami resistensi dikarenakan defisiensi zat besi
sehingga diperlukan suplementasi zat besi untuk memenuhi persediaan zat besi
tersebut. Terapi zat besi secara parenteral dapat meningkatkan respon terhadap terapi
ESA serta dapat mengurangi dosis yang dibutuhkan untuk mencapai dan
mempertahankan indeks target. Sebaliknya, terapi oral dibatasi oleh penyerapan dan
kepatuhan pasien yang buruk karena efek samping yang ditimbulkan. Pemberian
epoetin alfa secara subkutan lebih disukai daripada intravena karena dosis subkutan
15%-30% lebih rendah dari dosis intravena untuk dapat mempertahankan indeks target.
Selain itu, ada darbepoetin alfa yang memiliki waktu paruh lebih lama daripada epoetin
alfa dan aktivitas biologis yang panjang. Efek samping yang paling umum terjadi dari
penggunaan ESA yaitu hipertensi (Dipiro et al., 2015).
Tabel II.6 Obat anemia untuk terapi PGK (Henry Ford, 2011)
Nama Obat Rentang Dosis
Zat Besi
Ferro Sulfat 200 mg/24 jam (alternatif, Ferro Fumarat)
Erythropoietic-Stimulating Agent (ESA)
Epoetin alfa 10-40000 unit, subkutan, 1-4 minggu; terapi dimulai saat Hb
<10 g/dL dengan dosis 100 unit/kg/minggu
Darboetin alfa 40-300 mcg unit, subkutan, 2-4 minggu; terapi dimulai saat
Hb <10 g/dL dengan dosis 0,9 mcg/kg/2 minggu (ekuivalen
dengan 0,45 mcg/kg/minggu)

41
Tindakan lain yang dapat dilakukan untuk meringankan anemia pada pasien PGK
adalah dengan meminimalkan kehilangan darah, memberikan vitamin dan transfusi
darah. Multivitamin dan asam folat biasanya diberikan setiap hari karena dialisis
mengurangi vitamin yang larut dalam air. Transfusi darah Packed Red Cell (PRC)
lazim digunakan untuk mengobati anemia pada pasien PGK tetapi sekarang terbatas
pada pasien dengan kadar hematokrit kurang dari 24% (Price et al., 2005).
3) Asidosis metabolik
Terapi non farmakologi berupa pengaturan asupan protein dapat memperbaiki
keadaan asidosis. Bila kadar serum bikarbonat <15 mEq/L, beberapa ahli nefrologi
memberi rekomendasi klinik untuk memberikan terapi alkali seperti natrium
bikarbonat (NaHCO3) dengan dosis 0,5-2,0 mEq/kg sehari dengan target HCO3 22-26
mEq/L, maupun dengan terapi sitrat pada dosis 1 mEq/kg/hari secara oral.
Asidosis berat dapat timbul bila penderita sebelumnya sudah mengalami asidosis
kronik ringan. Bila pada kondisi asidosis berat akan dikoreksi dengan pemberian
NaHCO3 secara parenteral, maka perlu diperhatikan resiko yang ditimbulkan (Price et
al., 2005) dengan cara dilakukan monitoring terhadap kemungkinan munculnya
hiperkalemia, alkalosis metabolik, hipokalsemia, dan hipokalemia (Henry Ford, 2011).
4) Mineral Bone Disease dan Osteodistrofi ginjal
Salah satu terapi untuk mencegah timbulnya hiperparatiroidisme sekunder adalah
pengaturan diet rendah fosfat dengan melakukan pemberian agen pengikat fosfat dalam
usus. Sebaiknya pengobatan ini dimulai ketika GFR pasien turun hingga sepertiga
normal. Rekomendasi klinik terkait pemberian agen pengikat fosfat yaitu diberikan
pada pasien PGK stadium 3 dan 4 dengan kadar P > 4,6 mg/dL dan Ca < 10.2 mg/dL.
Selama terapi pengikat fosfat, jumlah asupan total Ca harian tidak boleh melebihi 2000
mg setiap hari untuk mencegah Ca yang berlebih.
Selain itu, kondisi hiperfosfatemia dapat dikontrol dengan pemberian aluminium
hidroksida secara oral atau kalsium karbonat, yang mengurangi penyerapan fosfat oleh
gastrointestinal. Kalsium karbonat (CaCO3) harus diminum 1-2 g bersama makanan
untuk memastikan keefektifan maksimum dalam pengikatan fosfat yang kemudian

42
akan mencegah absorpsinya. Terapi ini bertujuan untuk mempertahankan serum fosfat
sekitar 4,5 mg/dL dan Ca2+ sekitar 10 mg/dL (Harrison, 2005).
Vitamin D, ergocalciferol (sumber tanaman) atau cholecalciferol (sumber
hewani) dapat juga digunakan sebagai pengobatan untuk hipovitaminosis D pada setiap
stadium PGK. Namun, mungkin tidak cukup untuk menekan PTH pada stadium 3-5,
meskipun dapat memenuhi kebutuhan vitamin D. Akibatnya diperlukan vitamin aktif
D sterol untuk menekan PTH ke level target.
Tabe lI.7 Obat Mineral Bone Disease dan Osteodistrofi Ginjal pada PGK
(Ford, 2011)
Nama Obat Rentang Dosis
Vitamin D
Ergocalciferol (D2) 50000 IU 4x/1 minggu atau 8x/1 bulan,
kecuali bila Ca > 9,5 g/dL atau P > 4,6 mg/dL
Cholecalciferol (D3) 1750 IU satu kali sehari
Active Vitamin D Sterols
Calcitrol 0,25-0,50 mcg satu kali sehari
Doxercalciferol 1,0 mcg satu kali sehari
Paricalcitol 1,0 mcg satu kali sehari atau 2,0 mcg 3 kali
tiap minggu
Agen Pengikat Fosfat (Phospate Binder)
Kalsium asetat 1,0-1,5 g/hari untuk P >4,6 mg/dL dan Ca
8,8-10,2 mg/dL
Kalsium karbonat 1,0-1,5 g/hari untuk P >4,6 mg/dL dan Ca
8,8-10,2 mg/dL

43
5) Ketidakseimbangan Natrium-Air
Hipernatremia biasanya disebabkan oleh defisiensi air dalam tubuh relatif
terhadap natrium, jika konsentrasi natrium plasma meningkat di atas normal (135-145
mEq/L) (Yaswir dan Ferawati, 2012). Pengobatan yang dilakukan antara lain dengan
mengoreksi defisit air dan mencegah kehilangan lebih lanjut dengan mengoreksi
penyebab yang mendasarinya. Tergantung pada tingkat keparahan, penggantian air
dilakukan dengan asupan air secara oral dan intravena dengan larutan dekstrosa
(glukosa) 5% (dekstrosa dikeluarkan oleh metabolisme). Natrium plasma harus
diperiksa secara teratur untuk memastikan koreksi tidak dilakukan terlalu cepat (target
12 mmol/L per jam) (O’Callaghan, 2009).
2.3 Kondisi Hiperkalemia
2.3.1 Definisi Hiperkalemia
Kalium merupakan ion intraseluler utama dalam tubuh dan berperan penting
dalam menjaga fungsi sel. Kalium ditemukan banyak terdapat pada makanan terutama
buah dan cokelat. Kelebihan kalium biasanya dikeluarkan dari tubuh melalui ginjal.
Namun, pada pasien PGK kadar kalium dalam darah dapat meningkat seiring dengan
terjadinya penurunan GFR. Kondisi ini disebut sebagai hiperkalemia dengan kadar
kalium > 5 meq/L (Hsieh, 2010).
Hiperkalemia merupakan komplikasi umum yang sering terjadi pada pasien
PGK, terutama untuk pasien yang mempunyai nilai LFG <15 mL/menit (stadium
akhir). Ketika terjadi ketidakseimbangan elektrolit berupa peningkatan serum kalium
(K+) diatas kisaran normal (Kovesdy, 2014)., berpotensi mengancam jiwa. Bila kadar
serum kalium mencapai sekitar 7 mEq/L, maka dapat menyebabkan terjadinya
disaritmia yang serius (McPhee, 2006) hingga dapat menyebabkan kelainan konduksi
jantung termasuk fibrilasi ventrikel dan asistol karena peningkatan K+ di ekstrasel
(Apel et al., 2014).

44
Tabel II.8 Klasifikasi Hiperkalemia Berdasarkan Tingkat Keparahan (European
Resuscitation Guidelines, 2015)
Klasifikasi Hiperkalemia GFR (mmol/L)
hiperkalemia ringan 5,5-5,9 mmol/L
hiperkalemia sedang 6,0-6,4 mmol/L
hiperkalemia berat ≥ 6 mmol/L.
Hiperkalemia ringan biasanya berkaitan dengan adanya peningkatan
gelombang T, sedangkan hiperkalemia berat berkaitan dengan peningkatan interval PR
dan perpanjangan interval QRS. Namun hubungan antara kadar kalium dan EKG
tergantung pada beberapa faktor seperti sensitifitas dan kecepatan perkembangan
hiperkalemia. Penyebab terjadinya hiperkalemia yaitu karena adanya pergeseran
kalium ke ekstrasel yang disebabkan akibat penurunan ekskresi kalium ginjal,
redistribusi kalium ke cairan ekstrasel karena asidosis metabolik dan asupan kalium
yang berlebihan (Alldredge, 2013).
Pada pasien harus dipasang monitor jantung. Jika terdapat perubahan EKG
pengobatan harus cepat dilakukan. Awalnya, kalsium diberikan dalam bentuk kalsium
glukonat atau kalsium klorida yang akan melawan (antagonis terhadap) efek kalium
pada potensi aksi jantung, namun tidak bertahan lama. Untuk jangka menengah, kalium
dapat digerakkan masuk ke dalam sel dengan pemberian insulin, dikombinasikan
dengan glukosa, untuk mencegah hipoglikemia. Agonis B2 dapat juga digunakan.
Pemberian natrium bikarbonat menyebabkan alkalosis sementara, yang juga memacu
pergerakan kalium intraseluler. Untuk jangka panjang kelebihan kalium harus
dikeluarkan dari tubuh. Diuretik, seperti furosemid, dikombinasikan dengan hidrasi,
akan meningkatkan ekskresi oleh ginjal. Jika fungsi ginjal sangat terganggu, dialisis
atau hemofiltrasi akan mengeluarkan kalium (O’Callaghan, 2009). Untuk terapi lain
hiperkalemia dilakukan diet rendah kalium dengan tidak mengonsumsi obat-obatan
atau makanan yang mengandung kalium tinggi. Jumlah yang diperbolehkan dalam diet
adalah 40 hingga 80 mEq/ hari. Makanan yang mengandung kalium seperti sup, pisang,
dan jus buah murni. Pemberian kalium yang berlebihan akan menyebabkan
hiperkalemia yang berbahaya (Haryanti dan Nisa, 2015)

45
2.3.2 Mekanisme Terjadinya Hiperkalemia pada Penyakit Ginjal Kronik
Mekanisme utama ketika ginjal mempertahankan homeostasis kalium adalah
terjadi sekresi kalium ke dalam tubulus distal dan terkumpul di duktus proksimal. Jika
LFG mengalami penurunan maka kemampuan ginjal untuk mempertahankan kadar
serum kalium sulit dilakukan dan dapat mengancam kisaran fisiologis normal dari
ginjal (Kovesdy, 2014). Kelainan distribusi kalium terlihat selama asidosis metabolik,
defisiensi insulin, defisiensi aldosteron, antagonis adrenergik, dan kerusakan jaringan.
Selama mengalami asidosis metabolik maka akan terjadi pergeseran kalium intraseluler
menuju ke ekstraseluler yang signifikan dan menyebabkan ketidakseimbangan antara
keduanya dan menjadi hiperkalemia (Mushiyakh, 2011)
Gambar 2.7 Mekanisme terjadinya hiperkalemia pada PGK (Koda-kimble, 2013)
Menurut Clinical Practice Guidelines Treatment Of Acute Hyperkalemi In
Adults, 2014, Hiperkalemia biasanya terjadi pada pasien dengan gangguan ginjal akut
atau kronis. Pada pasien dengan penyakit ginjal kronis (CKD), ada beberapa faktor
yang dapat meningkatkan kerentanan terhadap hiperkalemia termasuk penurunan laju
filtrasi glomerulus (GFR), asidosis metabolik , ion H+ masuk ke sel untuk dibufer dan
ion K+ meninggalkan sel untuk mempertahankan elektronitas., dan asupan kalium
makanan tinggi relatif terhadap fungsi ginjal residual, tubulus distal terus-menerus

46
mensekresikan kalium, terjadi peningkatan aldosteron yang juga mendorong sekresi
kalium dengan menstimulasi pertukaran natrium-kalium di ginjal dan kolon. Selain itu
hiperkalemi dapat disebabkan oleh berkurangnya ekskresi kalium melalui ginjal yang
terjadi pada hiperaldosteronisme, gagal ginjal, pemakaian siklosporin atau akibat
koreksi ion kalium berlebihan dan juga pada kasus yang mendapat terapi angiotensin
converting enzyme inhibitor dan potassium sparing diuretic maka risiko hiperkalemia
akan semakin meningkat. (Sandala G, 2016).
Fisiologi dari kalium sangat membantu ketika mendekati pasien dengan
hiperkalemia. Total simpanan kalium tubuh sekitar 3000 mEq atau lebih (50 hingga 75
mEq / kg berat badan) Kalium merupakan ion utama tubuh, hampir 98% dari kalium
intraseluler. Konsentrasi kalium intraseluler sekitar 140 mEq / L dibandingkan dengan
4 hingga 5 mEq / L dalam cairan ekstraseluler. Perbedaan distribusi kedua kation
tersebut dipertahankan oleh pompa Na-K-ATPase dalam membran sel, yang memompa
natrium keluar dan kalium ke dalam sel dalam perbandingan 3: 2. Rasio konsentrasi
kalium dalam sel dan cairan ekstraseluler adalah penentu utama dari potensial
membran istirahat di seluruh membran sel, yang menetapkan tahap untuk generasi
potensial aksi yang penting untuk fungsi saraf dan otot normal yang mengarah ke
peningkatan depolarisasi jantung, dan rangsangan otot yang dapat menyebabkan
elektrokardiografi (ECG) berubah. Perubahan EKG dengan hiperkalemia tidak secara
konsisten bertahap, polanya tergantung pada dosis yang diberikan. Ketika terjadi
perubahan EKG yang cepat maka akan menyebabkan Risiko aritmia meningkat dengan
nilai K+ > 6,5 mmol / L dan bahkan ketinggian yang kecil di K+ dapat menyebabkan
gelombang T memuncak hingga ke ventrikel fibrilasi atau asistole. Semakin tinggi
kadar kalium pasien, maka semakin besar risiko terjadinya hiperkalemia. sehingga,
baik hiperkalemia dan hipokalemia dapat menyebabkan kelumpuhan otot dan aritmia
jantung yang berpotensi fatal (David, 2019)

47
2.3.3 Penatalaksanaan Hiperkalemia
Gambar 2.8 Penatalaksanaan Hiperkalemia (Clinical Practice Guidelines
Hyperkalemia, 2016)
Hiperkalemia (K+) ≥ 5 mmol/L
Hentikan semua suplemen K, Hentikan pengobatan yang
menyebabkan hiperkalemia, dan Pemantauan jantung
Pengecualian pseudohyyperkalemia
(Periksa kembali dengan menggunakan
sampel vena)
Pasien Asimtomatik
dengan ECG normal,
dan K+ > 6 sampai ≤
7 mmol/L
Pasien yang tidak stabil atau
simtomatik dengan ECG yang
tidak normal dan K+ > 7
mmol/L
Polystyrane sulfonate
(Kalitake)\
Natrium Bikarbonat
jika pasien mengalami
Asidosis Metabolik
Pertimbangkan untuk
pemberian salbutamol
Pasien Asimtomatik,
dengan ECG normal, dan
K+ ≥ 5,5 sampai ≤ 6,0
mmol/L
Kalitake
Natrium Bikarbonat
jika pasien mengalami
Asidosis Metabolik
Salbutamol
Insulin dan glukosa
jika terjadi perfusi
Kalsium glukonas
Insulin dengan glukosa
Salbutamol
Natrium Bikarbonat
jika pasien mengalami
Asidosis Metabolik
Kalitake
Pertimbangan
Dialisis

48
Terapi untuk pasien PGK dengan hiperkalemia dapat diberikan ketika pasien
memiliki EKG yang abnormal terkait dengan hiperkalemia atau serum kalium
≥6 mmol/L. Pada kondisi hiperkalemia ringan (5,5-5,9 mmol/L), awalnya pasien harus
diterapi dengan pengaturan pembatasan asupan kalium. Selanjutnya, pada pasien
hiperkalemia sedang (6,0-6,4 mmol/L) yang secara klinis dan EKG tidak menunjukkan
adanya hiperkalemia, dapat dikendalikan dengan pemberian resin penukar ion (natrium
polistiren sulfonat 15-30 g setiap 3-4 jam). Pada pasien hiperkalemia berat ( >6,5
mmol/L) dan menunjukkan kondisi hiperkalemia dengan adanya abnormalitas EKG
atau gambaran klinis, terapi darurat harus dilakukan yaitu berupa pemberian insulin 10
unit dan 50 ml dektrosa 50% secara intravena yang dapat menimbulkan pergeseran
kalium ke intrasel dalam waktu 30-60 menit. Selain itu, dapat juga dilakukan
pemberian kalsium glukonat 10 mL larutan 10% secara intravena (Brenner, 2014).
Penatalaksanaan dalam mengatasi hiperkalemia memiliki 3 mekanisme tujuan
diantaranya adalah menstabilkan membran jantung terhadap efek hiperkalemia,
meningkatkan uptake kalium ke intrasel serta mendorong ekskresi kalium (Apel et al.,
2014).
1) Menstabilkan membran jantung terhadap efek hiperkalemia
Efek hiperkalemia terhadap konduksi dan repolarisasi otot jantung dapat
dihambat dengan pemberian kalsium glukonat secara intravena. Efek pemberian
kalsium akan dapat dilihat pada EKG dalam 1-3 menit setelah pemberian atau paling
lambat dalam 30-60 menit. Pada kondisi hiperkalemia berat, dapat juga diberikan 10
ml kalsium glukonat 10% iv dalam 2-3 menit dengan disertai monitoring EKG pasien.
Bila masih belum terdapat perubahan EKG maka pemberian kalsium glukonat dapat
diulang setelah 5-10 menit.
2) Meningkatkan uptake kalium ke intrasel
Meningkatkan uptake kalium ke intrasel dapat menurunkan kadar serum kalium
secara cepat di ekstrasel. Yang termasuk dalam kategori ini adalah penggunaan insulin
dan β2-agonis.

49
a. Kombinasi insulin 10-20 unit dan 25-50 gram dekstrosa
Pemberian insulin secara intravena merupakan cara yang cepat untuk
menurunkan kadar serum kalium. Jika efektif, maka kadar kalium akan turun sebesar
0,5-1,5 mmol/L dalam 15-30 menit dan efek paling lama terjadi dalam 30-60 menit.
Insulin memicu pompa ion Na+, K+, ATPase untuk menguptake kalium ke dalam
intrasel. Sedangkan pemberian dekstrosa intravena bertujuan untuk mencegah
hipoglikemia akibat pemberian insulin.
h. Pemberian natrium bikarbonat
Natrium bikarbonat akan meningkatkan pH sistemik. Peningkatan pH tersebut
akan merangsang ion H+ keluar dari dalam sel yang kemudian menyebabkan K+ masuk
ke dalam sel. Dalam keadaan tanpa asidosis metabolik, natrium bikarbonat diberikan
50 mEq IV selama 10 menit. Bila dalam keadaan asidosis metabolik, disesuaikan
dengan keadaan asidosis metabolik yang ada.
c. Pemberian β2-agonis
Secara inhalasi maupun intavena β2-agonis akan merangsang pompa Na+, K+,
ATPase, sehingga kalium masuk ke dalam sel. Contohnya adalah albuterol 10-20 mg
secara inhalasi selama 10 menit, memiliki onset dalam 30 menit dan mampu
menurunkan konsentrasi kalium plasma sebesar 0,5-1,5 mmol/L. Efek terjadi paling
lama dalam 2-4 jam.
3) Mengeluarkan kalium dari dalam tubuh
a. Diuretik
Pada keadaan hiperkalemia kronik, pemberian loop diuretik atau tiazid diuretik
cukup untuk ekskresi kalium. Pemberian diuretik umumnya tidak dapat mengobati
hiperkalemia akut karena kecepatan ekskresi kalium tidak adekuat.
b. Resin penukar ion (kayexalate)
Cara lain untuk mengeliminasi kalium adalah dengan pemberian resin penukar
ion yaitu sodium polystyrene sulfonate (kayexalate). Umumnya akan menurunkan
konsentrasi kalium plasma sebanyak 0,5-1 mmol/L dalam 1-2 jam dan paling lama
dalam 4-6 jam. Resin tersebut dapat diberikan secara oral maupun rektal dengan dosis
25-50 g dicampur dengan 100 mL sorbitol 20%, mempunyai efek untuk mengganti

50
natrium dengan kalium di sistem saluran cerna. 1 gram resin dapat memindahkan 1
mEq kalium dengan 2-3 mEq natrium. Efek puncaknya terlihat dalam 4 jam
dikarenakan kecepatan perpindahan yang relatif lambat.
c. Dialisis
Selain itu, tindakan utama untuk mengeliminasi kalium pada penderita gangguan
fungsi ginjal, hiperkalemia persisten dan hiperkalemia berat dapat dilakukan dengan
cara dialisis (stadium akhir)
Tabel II.9 Penatalaksanaan Hiperkalemia (Mushiyakh, 2011)
Obat Tipe
Respon
Onset Durasi Mekanisme Kerja Penurunan
Kalium
yang
Diharapkan
Kalsium
Glukonat
Cepat 1-2
Menit
30-60
menit
Melindungi
kardiomikosit
0,5-1,5 mEq/L
Glukosa +
Insulin
Menengah 10-20
Menit
5-6
jam
Menarik kalium
ke intraseluler
0,5-1,5 mEq/L
(dosis berbeda)
Beta-
Agonis
Menengah 3-5
Menit
1-4
jam
Menarik kalium
ke intraseluler
-
Sodium
bikarbonat
Menengah 30-60
Menit
2-6
jam
Menarik kalium
ke intraseluler
-
Resin
Pengganti
Lambat 2-6
jam
4-6
jam
Mengeliminasi
kalium dari tubuh
-
Furosemid Lambat 5-30
Menit
2-6
jam
Mengeliminasi
kalium dari tubuh
-
Hemo-
dialisis
Lambat Mene
ngah
Mengel
iminasi
kalium
dari
tubuh
1 mmol/L pada 60
menit pertama dan
2 mmol/L pada
180 menit
kemudian.
-

51
2.4 Insulin
2.4.1 Struktur dan Nama Kimia Insulin
Insulin terdiri dari dua rantai peptida yaitu A dan B dimana masing-masing rantai
peptida terdiri dari 21 dan 30 asam amino yang saling dihubungkan dengan 2 jembatan
disulfida. Dua jembatan disulfida antar rantai tersebut menghubungkan A7 ke B7 dan
A20 ke B19. Selain itu, masih terdapat jembatan disulfide antara asam amino ke-6 dan
ke-11 pada rantai A. Insulin berperan mengatur metabolisme karbohidrat, lemak dan
protein (Katzung, 2010)
Insulin merupakan hormon polipeptida dengan struktur kompleks. Semua
sediaan insulin umumnya imunogenik pada manusia tetapi resistensi imunologis
terhadap kerja insulin tidak lazim terjadi. Insulin dirusak oleh enzim dalam saluran
cerna oleh karena itu harus diberikan melalui injeksi atau inhalasi; rute subkutan
memberi hasil yang baik pada semua kondisi (Tjay, 2015).
Rumus molekul : C256H381N65O76S6
Berat molekul : 5777.603 g/mol
Gambar 2.9 Struktur Kimia Insulin (Mellisa, 2013)
2.4.2 Sifat Fisika Kimia Insulin
a) Pemerian : Bubuk, putih atau hampir putih
b) Kelarutan : Praktis tidak larut dalam air dan alkohol, larut dalam asam
encer, mineral dan alkali.
c) Penyimpanan : Simpan di ruang kedap udara dan yang terlindung dari cahaya.
Simpan pada suhu -20°. Ketika dicairkan, insulin dapat disimpan pada suhu 2°-8°

52
dan digunakan untuk tujuan manufaktur dalam periode waktu yang singkat. Untuk
menghindari penyerapan kelembapan dari udara, maka insulin dapat disimpan pada
suhu kamar (Sweetman, 2009)
2.4.3 Farmakologi Insulin
2.4.3.1 Farmakodinamik Insulin
Insulin menghasilkan efek fisiologi yang bersifat luas dan kompleks. Efek yang
paling banyak ditemukan adalah hipoglikemia, selain itu juga terdapat efek yang lain
yang memiliki kaitan dengan transportasi elektrolit dan asam amino, berbagai enzim
dan pertumbuhan. Penyimpanan karbohidrat, protein dan lemak merupakan efek akhir
dari hormon ini. Berdasarkan hal tersebut, maka insulin dapat dikatakan sebagai
hormone of abundance (Ganong, 2003).
Efek kerja insulin yang sudah sangat dikenal adalah membantu transport glukosa
dari darah ke dalam sel. Kekurangan insulin menyebabkan glukosa darah tidak dapat
atau terhambat masuk ke dalam sel. Akibatnya, glukosa darah akan meningkat, dan
sebaliknya sel-sel tubuh kekurangan bahan sumber energi sehingga tidak dapat
memproduksi energi sebagaimana seharusnya (Dipiro et al., 2015)
2.4.3.2 Farmakokinetika Insulin
Insulin mempunyai peran yang sangat penting dan luas dalam pengendalian
metabolisme. Insulin yang disekresikan oleh sel-sel β pankreas akan langsung
diinfusikan ke dalam hati melalui vena porta, yang kemudian akan didistribusikan ke
seluruh tubuh melalui peredaran darah. Pemberian insulin tidak dapat dilakukan secara
per oral karena dapat mengalami penguraian oleh pepsin lambung. Oleh karena itu,
insulin selalu diberikan melalui injeksi. Insulin dirombak dengan cepat terutama di hati,
ginjal dan otot. t ½ dalam plasma hanya terjadi beberapa menit pada orang sehat namun
pada pasien diabetes dapat diperpanjang sampai 13 jam, hal ini mungkin terjadi akibat
pengikatan pada antibodi (Tjay, 2015). Lispro, insulin aspart dan glulisin merupakan
analog yang lebih cepat diserap, mencapai puncak lebih cepat dan memiliki jangka
waktu yang lebih pendek dari insulin reguler (Dipiro et al., 2015).

53
a) Absorpsi : tingkat keefektifan penyerapan insulin tergantung pada aliran darah
lokal, dengan penyerapan tercepat yaitu pada bagian perut. Selain secara subkutan,
penginjeksian insulin secara intramuskular juga menghasilkan efek terapi yang
cepat. Peningkatan absorbs insulin secara subkutan akan meingkatkan kadar insulin
dalam darah sehingga mengakibatkan peningkatan dari efek insulin yang
memungkinkan terjadinya hipoglikemia.
b) Distribusi : tidak mengikat protein plasma, kecuali antibodi insulin
c) Metabolisme : insulin terdegradasi oleh protease insulin atau enzim pengurai insulin
dan isomerase protein disulfida. Insulin cepat dimetabolisme, terutama di hati.
Insulin akan diserap kembali di tubulus proksimal ginjal dan direabsorpsi ke darah
vena atau dimetabolisme.
d) Eliminasi : waktu paruh ditentukan oleh tingkat penyerapan. Hanya sedikit jumlah
insulin yang diekskresikan dalam urin.
Tabel II.10 Farmakokinetika berbagai variasi insulin (Dipiro, 2015)
Tipe Insulin Onset Puncak
(jam)
Durasi
(jam)
Durasi
maksimum
(jam)
Rapid acting
Aspart 15-30 menit 1-2 3-5 5-6
Lispro 15-30 menit 1-2 3-4 4-6
Glulisin 15-30 menit 1-2 3-4 5-6
Short acting
Regular 30-60 menit 2-3 3-6 6-8
Intermediate
acting
NPH 2-4 jam 4-6 8-12 14-18
Long acting
Detemir 2-4 jam 6-9 14-24 24
Glargin 4-5 jam - 22-24 24

54
2.4.4 Mekanisme Insulin dalam Penatalaksanaan Hiperkalemia
Gambar 2.10 Mekanisme Insulin dalam Pelaksanaan Hiperkalemia
(Williams and Wilkins, 2012)
Karena efek dari uremia, penyerapan glukosa dan insulin menjadi terganggu
namun efek insulin dalam menurunkan serum kalium tidak terganggu. Hal ini
disebabkan karena jalur independen untuk kalium dan transportasi glukosa dalam
melintasi membran sel berbeda. Dalam mengatasi kondisi hiperkalemia, insulin bekerja
menstimulasi uptake K+ oleh otot skelet dan sel hepatik dengan cara memasukkan K+
ke intrasel, disertai dengan terjadinya rangsangan pada membran sel terhadap aktivitas
Na+dan H+. Selanjutnya Na+ dan K+ tersebut akan dimasukkan ke intrasel sehingga
mengakibatkan terjadinya aktivasi Na+ dan K+ tersebut. Terjadi pengikatan terhadap
K+ pada ekstrasel yang kemudian akan dimasukkan ke intrasel, sehingga akan terjadi
penurunan kadar K+ dalam serum (Vijayan, 2014).
2.4.5 Permasalahan pada Penggunaan Terapi Insulin
2.4.5.1 Efek Samping Insulin
Efek samping terpenting dari penggunaan insulin yang dapat terjadi berupa
hipoglikemia, reaksi alergi, resistensi, lipodistrofi dan gangguan penglihatan (Tjay,
2015).

55
a) Hipoglikemia
Biasanya terjadi karena overdosis atau tidak/terlambat makan sesudah injeksi
dikarenakan kerja fisik terlalu berat, atau interaksi dengan obat-obat yang diminum
bersamaan. Sediaan depot lebih berbahaya, karena menimbulkan hipoglikemia secara
berangsur-angsur yang tidak dapat diperkirakan oleh pasien dan kebanyakan terjadi di
tengah malam sewaktu tidur. Hipoglikemia lebih sering terjadi pada insulin human
kemungkinan karena adanya gejala adrenergik seperti rasa lapar, gemetar, berkeringat
dan jantung berdebar, kurang jelas dirasakan berhubung regulasi gula darahnya yang
lebih baik. Semakin baik regulasi gula darah, semakin besar resiko akan timbulnya
hipoglikemia serius.
b) Reaksi alergi
Reaksi alergi di kulit pada tempat injeksi adakalanya terjadi dan kebanyakan
ditimbulkan oleh zat-zat tambahan (protamin, seng, zat-zat pengawet, kotoran). Alergi
untuk insulin jarang terjadi dan umumnya bersifat lokal (eksantema, gatal dan
pengerasan di tempat injeksi, antara lain karena iritasi kulit, teknik injeksi kurang tepat
atau infeksi kuman). Reaksi immunogen sistemik jarang sekali terjadi dan berupa
urtikaria, mual, muntah dan anafilaksis.
c) Lipodystrofia
Lipodystrofia yakni terganggunya pertumbuhan lemak subkutan di tempat
injeksi, jarang terjadi dan bersifat ringan. Misalnya atrofia (penyusutan) dan hipertrofia
(berlebihan) yang hampir selalu disebabkan oleh tidak sering mengganti lokasi injeksi.
d) Resistensi insulin
Terjadi bila kebutuhan insulin melebihi 200 IU/hari. Keadaan ini dapat
disebabkan oleh pembentukan antibodi yang mengikat sebagian insulin. Resistensi
terutama dapat timbul pada pasien dengan overweight, kemungkinan akibat
berkurangnya reseptor insulin atau penurunan kepekaannya.
e) Gangguan akomodasi mata
Dapat terjadi akibat terlalu cepatnya penurunan gula darah, yang dapat
menimbulkan terganggunya keseimbangan osmotik antara lensa dan cairan mata.

56
2.4.5.2 Interaksi Insulin
Menurut (A to Z Drug Facts, 2013) dalam penggunaannya bersamaan dengan
obat lain, diketahui bahwa beberapa obat lain dapat berpotensi menimbulkan interaksi
dengan insulin, seperti:
1. Ethanol : alkohol dapat meningkatkan atau menurunkan efek dari insulin dalam
menurunkan glukosa darah, juga meningkatkan efek hipoglikemia
2. Aspirin : aspirin meningkatkan efek dari insulin, sehingga dilakukan modifikasi
terapi atau monitor
3. Captopril : captopril meningkatkan efek dari insulin. Keduanya menurunkan glukosa
darah. Lakukan monitor glukosa darah
4. Ciprofloxacin : meningkatkan efek dari insulin. Dilaporkan penggunaan quinolon
dan OAT dapat menyebabkan hiperglikemia dan hipoglikemia
5. Prednison : prednison menurunkan efek dari insulin
6. Isoniazid : isoniazid menurunkan efek dari insulin
7. Valsartan : valsartan meningkatkan efek dari insulin. Penggunaan insulin dan ARB
secara bersamaan memerlukan penyesuaian dosis insulin dan peningkatan
pemantauan glukosa
8. Kontrasepsi oral : meningkatkan kebutuhan insulin
9. Obat hipoglikemik oral : menurunkan kebutuhan insulin (A to Z Drug Facts, 2013)
2.4.6 Jenis-Jenis Insulin
Berbagai jenis-jenis insulin diantaranya adalah sebagai berikut (Tjay, 2015):
1) Insulin kerja singkat (Insulin Rapid Acting).
Onset of action dari insulin kerja singkat adalah 30 menit (melalui injeksi
subkutan), waktu untuk mencapai kadar puncak adalah 1-3 jam kemudian dengan
durasinya selama 5-6 jam, dan memiliki variabilitis terendah pada absorbs sekitar 5%
dari semua insulin komersial yang tersedia (Katzung, 2015). Contoh insulin kerja
singkat adalah insulin glulisin, insulin lispro dan insulin aspart. Insulin soluble yang
diberikan secara intravena hanya diberikan pada keadaan darurat dan keadaan sakit
parah atau pada saat sebelum tindakan bedah.

57
2) Insulin kerja pendek (Insulin Short Acting)
Masa kerja insulin reguler pendek dan efeknya terjadi dalam waktu 30 menit
setelah pemberian suntikan. Insulin kerja pendek dapat diberikan secara intravena
untuk terapi ketoasidosis diabetik maupun setelah pembedahan ataupun selama infeksi
akut sehingga insulin dibutuhkan segera (Katzung, 2015). Insulin Short Acting
diberikan sebelum makan untuk menutupi beba karbohidrat, apabila diberikan setelah
makan dapat meningkatkan resiko hiperglikemia postprandial dini diikuti dengan
hipoglikemia yang tertunda (Allison P, 2011)
3) Insulin kerja menengah (Insulin Intermediate Acting)
Insulin Intermediate Acting di formulasikan agar dapat dilarutkan secara
bertahap-tahap ketika diberikan secara subcutan, sehingga durasi kerja dari insulin
lebih panjang, Terdapat 2 sediaan insulin yang sering digunakan yaitu insulin Neutral
Protamine Hagedorn (NPH) (insulin isophane) dan insulin lente (insulin zink
suspense) dengan Onset of action dan durasi kerjanya yang sama. Insulin NPH
merupakan insulin suspensi yang kompleks dengan zink dan protamine di larutan
fosfat, sedangkan insulin lente merupakan campuran dengan cara kristalisasi dan amorf
dalam larutan asetat yang mana dapat menurunkan kelarutan dari insulin. Jangka waktu
efeknya dapat divariasikan dengan cara mencampurkan beberapa bentuk insulin
dengan lama kerja yang berbeda. Contohnya: Humulin 20 = insulin 20% + insulin
isofan 80%, lama kerja 12-24 jam. Selain itu, insulin isophane dan suspensi insulin
seng
4) Insulin kerja panjang (Insulin Long Acting)
Insulin long acting dibuat untuk memperpanjang kerjanya. Biasanya
dikombinasikan dengan insulin lainnya sebelum disuntikkan demi kenyamanan pasien.
Biasanya juga digunakan metode mencampur insulin dengan protein, atau seng atau
dengan mengubah bentuk fisiknya. Contoh : suspensi insulin seng, glargine (lantus),
detemir (levemir). Insulin ini dapat diberikan sekali atau dua kali sehari, tergantung
dosisnya. Dosis yang lebih rendah mungkin tidak berlangsung 24 jam sedangkan dosis
yang lebih tinggi dapat menghambat penyerapan insulin (Allison P, 2011)

58
Tabel II.11 Sediaan Insulin Rapid Acting (ISO, 2016)
Nama Obat Kandungan Bentuk Sediaan dan Gambar
Insulin Actrapid
HM/Actrapid HM
Penfill
Insulin manusia
rekombinan DNA kerja
cepat 100 IU/ml
Vial
Humalog/
Humalog Mix 25
Humalog insulin lispro.
Humalog mix 25
Insulin lispro 25%,
insulin lispro
protamine susp (rDNA
origin) 75%
Cartridge
Novomix 30 Flexpen Indulin aspart 100
IU/ml 30%, insulin
aspart terprotaminasi
70%
Pen
Novorapid Vial &
Flexpen
Insulin aspart 100
IU/ml kerja cepat
Vial, pen

59
2.5 Hubungan antara DM, PGK dan Insulin yang digunakan
Komplikasi yang sering terjadi pada pasien PGK yaitu nefropati diabetika.
Diabetes mempengaruhi pembuluh darah kecil ginjal akibatnya efisiensi ginjal untuk
menyaring darah terganggu. Pasien dengan nefropati mengalami gejala seperti lemas,
mual, pucat sampai keluhan sesak napas akibat penimbunan cairan ditandai dengan
adanya mikroalbuminuria (30mg/hari), disertai dengan peningkatan tekanan darah
sehingga mengakibatkan menurunnya filtrasi glomerulus dan akhirnya menyebabkan
PGK (Misnadiarly, 2006). Pasien DM dengan komplikasi berat seperti pada paseien
PGK sebagian besar tidak lagi diterapi dengan Antidiabetik oral (OAD), hal ini
dikarenakan kemampuan ginjal yang menurun untuk dapat mengekskresi obat di
dalam tubuh, sehingga terapi yang biasa digunakan untuk pasien DM dengan PGK
adalah terapi insulin karena mekanisme kerja yang langsung menuju ke pembuluh
darah dan di distribusi ke seluruh tubuh tanpa melewati proses disentegrasi, absorbsi
dan eksresi di ginjal.
Penggunaan insulin haruslah tepat dan sesuai dengan indikasi untuk pasien DM
dengan gangguan ginjal. Menurut American Diabetes Association (ADA) pada tahun
2018, terapi insulin (dengan atau tanpa obat tambahan) pada pasien DM tipe 2
terdiagnosis yang disertai dengan gejala dan/atau memiliki kadar HbA1c ≥ 10% (86
mmol/mol) dan/atau kadar gula darah ≥300 mg/dL (16,7 mmol/L) atau pada pasien
yang telah terdiagnosis DM tipe 2, bila target HbA1c tidak tercapai dalam 3 bulan
penggunaan 3 obat antihiperglikemik oral. Sasaran pertama terapi hiperglikemia adalah
mengendalikan glukosa darah basal (puasa, sebelum makan). Insulin yang digunakan
untuk mencapai sasaran glukosa darah basal yaitu insulin basal (insulin kerja sedang
atau panjang). Insulin basal biasanya disuntikkan di malam hari dan dikombinasikan
dengan metformin atau terkadang agen non insulin lainnya. Bila kadar HbA1c tetap
tinggi meskipun sasaran glukosa darah basal (puasa) sudah tercapai (atau bila dosis
insulin basal > 0,5 unit/kg/hari), maka, dipertimbangkan untuk menggunakan terapi
intensifikasi insulin. Pilihan untuk terapi intensifikasi insulin adalah kombinasi insulin
basal dengan injeksi tunggal GLP-1 receptor agonist atau kombinasi insulin basal
dengan injeksi tunggal rapid acting insulin analog sebelum makan porsi terbesar (basal

60
plus) atau menghentikan insulin basal dan menginisiasi premixed insulin 2 kali sehari
sebelum sarapan dan sebelum makan siang. Bila salah satu regimen yang dipilih tidak
efektif (misalnya insulin basal plus GLP-1 RA), pertimbangkan untuk beralih ke
regimen lain untuk mencapai target HbA1c (misalnya insulin basal plus injeksi tunggal
rapid-acting insulin 2 kali sehari).
Menurut ADA pada tahun 2018, insulin basal dimulai pada dosis 10 IU perhari
atau 0,1-0,2 IU/kg/hari, tergantung dari derajat hiperglikemia. Dosis dapat ditingkatkan
10-15% atau 2-4 unit sekali atau dua kali seminggu sampai kadar gula darah puasa
mencapai target. Pada rapid acting insulin, baik 1 kali ataupun 2 kali atau lebih
penyuntikan perhari, dosis dapat dimulai dari 4 unit atau 0,1 U/kg, atau 10% dari dosis
basal. Dosis dapat ditingkatkan 10-15% sekali atau dua kali seminggu sampai kadar
pengecekan gula darah mandiri tercapai. Pada premixed insulin, dosis dapat dimulai
sesuai dosis basal, dengan pembagian 2/3 dosis pagi hari dan 1/3 dosis malam hari atau
½ dosis pagi hari dan ½ dosis malam hari. Dosis dapat ditingkatkan 1-2 unit atau 10-
15% sekali atau dua kali seminggu sampai kadar pengecekan gula darah mandiri
tercapai.
2.6 Dekstrosa
2.6.1 Struktur dan Nama Kimia Dekstrosa
Gambar 2.11 Struktur Kimia Glukosa (Pubchem, 2018)

61
Glukosa (D-glukosa/dekstrosa) adalah gula monosakarida yang digunakan
sebagai sumber tenaga utama dalam tubuh. Glukosa merupakan prekursor untuk
mensintesis semua karbohidrat lain di dalam tubuh seperti glikogen, ribosa dan
deoksiribosa dalam asam nukleat, galaktosa dalam laktosa susu, glikolipid,
glikoprotein dan proteoglikan (Murray et al., 2003).
Nama Kimia : Alpha-D-Glucose monohydrate; (Glucosum) monohydricum
Rumus Molekul : C6H14O7
Berat Molekul : 198.171 g/mol (Pubchem, 2018)
2.6.2 Sifat Fisika Kimia Dekstrosa
a) Pemerian : Kristal atau bubuk granular, tidak berwarna atau putih, tidak
berbau dan memiliki rasa manis.
b) Kelarutan : Larut 1:1 dalam air dan 1:100 dalam alkohol; sangat larut
dalam air mendidih; larut dalam alkohol mendidih.
c) Stabilitas :
- Terhadap cahaya : Tidak stabil terhadap sinar pada proses γ sterilisasi
- Terhadap suhu : Tidak stabil pada pemanasan suhu tinggi dan lama (terjadi
penurunan pH); penyimpanan pada suhu < 25 'C
- Terhadap pH : Tidak stabil (terurai menjadi 5-hidroksi metil furfural pada pH
basa). Injeksi dekstrosa stabil pada pH 3.5 - 6.5
- Terhadap oksigen : Tidak stabil (Sweetman, 2009).
2.6.3 Farmakologi Dekstrosa
2.6.3.1 Farmakodinamik Dekstrosa
Dekstrosa merupakan sumber kalori bagi tubuh dan cepat dimetabolisme.
Dekstrosa dapat menurunkan protein tubuh dan ekskresi nitrogen, meningkatkan
deposisi glikogen dan mengurangi atau mencegah ketosis jika diberikan dalam dosis
yang cukup. Larutan dekstrosa 5% bersifat isotonik dan diberikan perifer. Infus
dekstrosa konsentrat memberikan peningkatan asupan kalori dengan volume cairan
yang lebih sedikit. Larutan di atas 10% harus diberikan hanya dengan kateter vena
sentral (Sweetman, 2009).

62
2.6.3.2 Farmakokinetika Dekstrosa
Absorbsi dekstrosa berlangsung cepat di gastrointestinal. Dekstrosa
membutuhkan waktu kira-kira 40 menit untuk mencapai kadar puncak plasma setelah
pemberian secara per oral pada pasien dengan kondisi hipoglikemia. Proses
metabolisme dekstrosa berlangsung melalui piruvat atau asam laktat dengan disertai
pembebasan energi. Pemberian dekstrosa secara infus intravena pada jangka panjang
dapat menyebabkan edema. Pemberian sediaan dekstrosa yang bersifat hiperosmotik,
dikontraindikasikan untuk pasien anuria, pendarahan intrakranial atau intraspinal dan
dehidrasi yang sangat parah (Sweetman, 2009)
2.6.4 Mekanisme Dekstrosa dalam Penatalaksanaan Hiperkalemia
Hipoglikemia merupakan suatu kondisi yang muncul akibat dari pemberian
insulin dalam pengobatan hiperkalemia. Hal ini merupakan suatu kejadian yang umum
terjadi. Dengan kondisi ginjal yang tidak normal maka akan lebih memicu terjadinya
hipoglikemia pada pengobatan hiperkalemia. Resiko hipoglikemia yang ditimbulkan
tersebut dapat diminimalkan dengan pemberian dekstrosa yang memadai dan sesuai
dengan dosis yang telah ditentukan namun tetap dengan melakukan
pemantauan/monitoring kadar gula darah pasien. Berdasarkan penelitian Chothia, MY
(2014) dalam terapi pada pasien PGK dengan kondisi hiperkalemia, ada sebanyak 75%
pasien mengalami hipoglikemia dari total sampel yang diteliti setelah pemberian
insulin sebagai terapi hiperkalemia tersebut. Namun setelah dilakukan penelitian lagi
dapat ditarik sebuah kesimpulan bahwa untuk mengurangi efek hipoglikemia yang
ditimbulkan dapat dilakukan pemberian dekstrosa yang lebih besar yang diberikan
secara bolus, selain itu dapat juga diberikan secara infus selama 60 menit. Koreksi
terhadap kalium (K+) serta glukosa darah harus dilakukan pemantauan/monitoring
dalam waktu beberapa jam.
2.6.5 Permasalahan pada Penggunaan Terapi Dekstrosa
2.6.5.1 Efek Samping Dekstrosa
Pemberian larutan glukosa secara intravena (terutama larutan hiperosmotik yang
juga memiliki pH rendah) dapat menyebabkan nyeri lokal, iritasi pada vena,
tromboflebitis, dan nekrosis jaringan jika terjadi ekstravasasi. Pemberian melalui infus

63
intravena dapat menyebabkan gangguan cairan dan elektrolit termasuk hipokalemia,
hipomagnesemia dan hipofosfatemia. Pemberian melalui infus secara cepat dengan
volume besar atau dalam jangka panjang, larutan isoosmotik dapat menyebabkan
edema; sebaliknya penggunaan cairan hipoosmotik yang lama atau cepat dapat
menyebabkan dehidrasi sebagai konsekuensi dari terinduksinya hiperglikemia
(Sweetman, 2009).
2.6.5.2 Interaksi Obat Dekstrosa
Dalam penggunaannya bersamaan dengan obat lain, diketahui bahwa beberapa
obat lain berpotensi menimbulkan interaksi dengan dekstrosa, diantaranya adalah
magnesium klorida, magnesium sitrat dan magnesium sulfat dimana dekstrosa dapat
menurunkan kerja ketiga obat tersebut dengan meningkatkan klirens ginjal. Tergolong
kategori minor
2.6.6 Jenis-Jenis Dekstrosa
Tabel II.12 Bentuk sediaan dektrosa yang beredar di Indonesia (Sweetman, 2009)
1 Dekstrosa
5%.
Dapat diberikan melalui vena perifer yaitu berdasarkan rute
intravena. Agar tidak menimbulkan adanya glukosuria maka
kecepatan pemberian infus dekstrosa yang dapat diberikan kepada
pasien adalah 0,5 g/kg/jam dengan kecepatan maksimum tidak
melebihi 0,8 g/kg/jam. Dosis pemberian dektrosa tergantung pada
usia, berat badan dan keseimbangan cairan, elektrolit, glukosa serta
asam basa pasien.
2 Dekstrosa
10%.
Direkomendasikan untuk diberikan dengan kateter pada vena
sentral yang besar, bersifat hipertonik. Dipilih vena besar pada
lengan jika digunakan vena perifer dan infus harus dipindah-pindah
tiap hari bila memungkinkan. Kecuali penanganan emergensi pada
kasus hipoglikemia berat, konsentrasi dekstrosa yang lebih tinggi
(20% keatas) harus diberikan melalui vena sentral. Agar tidak
menimbulkan glukosuria maka kecepatan pemberian infus pada
pasien yang dapat diberikan adalah 0,5g/kg/jam.

64
3 Dekstrosa
40%.
Diberikan bila kadar GDs 0-50 mg/dL. Biasanya dikombinasikan
bersama dekstrosa 50% secara IV bolus. Jika kadar GDs
50100mg/dL maka pemberian sediaan dekstrosa 40% dikombinasi
dengan larutan dekstrosa 25% secara IV bolus
4 Dekstrosa
50%.
Digunakan untuk mengobati hipoglikemia yang diinduksi oleh
insulin atau syok karena insulin. Apabila diketahui adanya syok
insulin dan kesadaran pasien terganggu, maka pemberian larutan
gula secara oral merupakan kontraindikasi, sehingga seringkali
diberikan 50 ml dekstrosa 50% secara IV bolus. Dekstrosa 50%
sangat mengiritasi vena sehingga hendaknya diberikan pada
pembuluh vena perifer yang besar atau pembuluh vena sentral.
2.7 Protap atau SOP pemberian insulin dan dekstrosa pada komplikasi
hiperkalemia (Guidelines for the Treatment of Hyperkalaemia in Adults, 2014)
Alihkan kalium dari darah ke dalam sel (penggunaan insulin dan glukosa)
• Penarikan 10 unit Actrapid® insulin menggunakan jarum suntik insulin, kemudian
dilakukan pengecekan volume.
• Tambahkan 50 ml glukosa 50% vial seperti yang ditunjukkan dalam Prosedur Operasi
Standar (SOP) dalam kit hiperkalemia.
• Berikan injeksi IV lambat lebih dari 5 menit (Permulaan tindakan hipokalemik terjadi
dalam 15 menit dan berlangsung setidaknya 60 menit, diamati adanya pengurangan
kalium antara 0,6 hingga 1,0 mmol / L).
• Memantau urea dan elektrolit (U & Es) 30 menit, satu, dua, empat dan enam jam
setelah setiap pemberian insulin / glukosa.
• Jika glukosa serum ≥ 15 mmol / L maka pemberian glukosa tambahan dengan
insulin tidak diperlukan
• Efek dari pemberian insulin / glukosa diamati dalam 15 menit dan bertahan 4-6
jam

65
• dilakukan pemantauan glukosa darah 15 dan 30 menit setelah memulai infus dan
kemudian setiap jam, hingga enam jam setelah infus selesai, terjadinya hipoglikemia
ketika kurang dari 30 g glukosa yang diberikan dengan insulin
• Dalam beberapa keadaan (syok sirkulasi, ketoasidosis diabetikum) glukosa kapiler
pengujian dengan glukometer
2.7.1 Pembuatan 10 unit insulin Actrapid® (larut) dan 50 ml glukosa 50% vial
menggunakan kit hiperkalemia di Indonesia (Guidelines for the Treatment of
Hyperkalaemia in Adults, 2014)
1. Diambil botol Actrapid® dari kulkas farmasi.
2. Ambil tabung glukosa 50% dari kit dan lepaskan tutup pelindungnya.
3. Ukur 10 unit insulin menggunakan jarum suntik insulin dari
kit:
a. Tarik plunger kembali ke tanda 10 unit pada jarum suntik insulin. Periksa 10
unit insulin (10 unit insulin terkandung dalam 0,1ml).
b. Catat pemberian ini dan obat-obatan lainnya yang digunakan untuk mengobati
hiperkalemia pada Kardex begitupun untuk pemeriksaan ganda yang
didokumentasikan pada Kardex.
4. Suntikkan 10 unit insulin ke dalam gelas glukosa 50%, lalu di campur.
6. Ambil Chemoprotect® Spike dari kit dan lepaskan selubung pelindung.
7. Tusuk botol kaca glukosa 50% dengan Chemoprotect® Spike.
8. Pasang syringe 50 ml ke Chemoprotect® Spike dan buat isi vial.
9. Lepaskan jarum suntik 50 ml dari Chemoprotect® Spike dan keluarkan udara
10. Berikan dalam vena besar dengan injeksi IV lambat lebih dari 5 menit.
Pemantauan - glukosa darah harus diukur setelah 15 dan 30 menit dan kemudian setiap
jam selama enam jam. Periksa U & Es 30 menit, satu, dua, empat dan enam jam setelah
setiap pemberian insulin / glukosa.

66
2.8 Tinjauan Kombinasi Insulin dan Dekstrosa
Pada pasien PGK terjadi kelainan pada tubular ginjal yang dapat menyebabkan
gangguan keseimbangan elektrolit, salah satunya adalah peningkatan kadar kalium
(K+) di ekstrasel yang disebut hiperkalemia. Salah satu terapi yang dapat diberikan
untuk mengatasi kondisi hiperkalemia adalah dengan pemberian kombinasi insulin dan
dekstrosa secara intravena.
Dalam mengatasi hiperkalemia, Insulin bekerja menstimulasi uptake K+ oleh otot
skelet dan sel hepatik dengan cara memasukkan K+ ke intrasel, disertai dengan
terjadinya rangsangan pada membran sel terhadap aktivitas Na+ H+. Selanjutnya
Na+ dan K+ tersebut akan dimasukkan ke intrasel sehingga mengakibatkan terjadinya
aktivasi Na+ dan K+ tersebut. Terjadi pengikatan terhadap K+ pada ekstrasel yang
kemudian akan dimasukkan ke intrasel, sehingga akan terjadi penurunan kadar K+
dalam serum (Vijayan, 2014).
Hipoglikemia merupakan suatu kondisi yang muncul akibat dari pemberian
insulin pada pengobatan hiperkalemia pasien PGK dan merupakan suatu kejadian yang
umum. Dengan kondisi ginjal yang tidak normal maka akan lebih memicu terjadinya
hipoglikemia pada pengobatan hiperkalemia. Resiko hipoglikemia dapat diminimalkan
dengan pemberian dekstrosa yang memadai dan sesuai dengan dosis yang ditentukan
namun tetap dengan melakukan pemantauan/monitoring terhadap kadar gula darah
pasien.
Kombinasi insulin dan glukosa memiliki mekanisme untuk menurunkan kadar
K+ dalam plasma atau menurunkan kondisi hiperkalemia, namun dari beberapa
literatur menjelaskan ada beberapa macam dosis yang berbeda untuk kombinasi antara
keduanya. Untuk insulin, regimen yang umum digunakan berdasarkan American Heart
Association Guideline dan Washington Manual of Critical Care adalah 10 unit insulin
reguler yang diberikan secara intravena dengan 25 g dekstrosa intravena selama 15-30
menit, namun dalam studi dosis insulin berkisar antara 5-10 IU dan glukosa antara 25-
60 g. Pada pedoman lain, pemberian dosis kedua 25 g glukosa intravena 60 menit
setelah pemberian regimen berdasarkan pedoman AHA digunakan untuk mencegah
hipoglikemia, penggunaan insulin aspart sebagai pengganti insulin reguler, pemberian

67
secara bolus insulin 5 IU diulang setiap 15 menit ditambah 50g/ jam infus glukosa.
Regimen yang dimaksud termasuk infus intravena 10 IU insulin kerja singkat dan 50 g
glukosa (500 ml dekstrosa 10%) lebih dari 240 menit ditambah 40 mg furosemid (Coca
et al., 2017).
Berdasarkan penelitian yang dilakukan oleh LaRue et al., (2017) sebanyak 675
pasien rawat inap PGK mendapatkan terapi hiperkalemia dengan tujuan untuk
menurunkan kadar serum kalium sebesar 1,1 mEq/L dengan menggunakan 5 unit dan
10 unit insulin IV. Dari total 542 pasien, sebanyak 155 pasien mengalami hipoglikemia
(glukosa darah kurang dari 70 mg / dl) 5 jam setelah pemberian insulin dengan
menggunakan 10 unit insulin. Pemberian insulin dan perubahan kalium serum, dosis
insulin yang lebih rendah yaitu, 5 unit dapat mengurangi kejadian hipoglikemia pada
pasien dengan insufisiensi ginjal. Selain itu, merujuk pada penelitian Vijayan et al.,
(2014) yang meneliti insiden hipoglikemia setelah penatalaksanaan hiperkalemia
dengan insulin di rumah sakit, studi ini menunjukkan bahwa hipoglikemia [glukosa
darah < 3,9 mmol/L (70 mg/dL)] terjadi pada 19 dari 219 pasien (8,7%) dan 58%
hipoglikemia terjadi dengan rejimen yang umum digunakan yaitu 10 unit insulin IV
dengan 25 g dekstrosa. Hasil studi keduanya menunjukkan perlunya dekstrosa
tambahan pada penatalaksanaan hiperkalemia. Rekomendasi lain adalah dengan
pemberian 10 unit insulin reguler dan dekstrosa 25 g diikuti oleh infus 10% dekstrosa
pada 50 mL/jam dengan pemantauan ketat glukosa darah setidaknya selama 3 jam atau
sampai dialisis dimulai.
Berdasarkan penelitian Coca et al., (2017) sebanyak 164 pasien yang mengalami
hiperkalemia diobati dengan 10 unit insulin dan 50 g glukosa. Kadar serum kalium
pasien turun sebanyak 1,18 ± 1,01 mmol/L. Sebanyak 11 pasien rawat inap (6,1%)
mengalami hipoglikemia dan sebanyak 2 pasien (1,2%) mengalami hipoglikemia berat.
Kadar glukosa darah yang lebih rendah sebelum diberikan pengobatan cenderung
mengasosiasikan risiko hipoglikemia yang lebih tinggi. Kombinasi insulin dan glukosa
yang dilakukan dapat mengurangi kadar serum kalium secara efektif dan memiliki
resiko efek samping yang lebih rendah terhadap hipoglikemia.