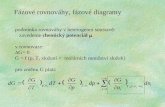Chemické a fázové rovnováhy v heterogenních systémech
description
Transcript of Chemické a fázové rovnováhy v heterogenních systémech

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
1
Chemické a fázové rovnováhyChemické a fázové rovnováhyv heterogenních systémechv heterogenních systémech
http://www.vscht.cz/ipl/osobni/leitner/prednasky/fchr/FCHR.htmhttp://www.vscht.cz/ipl/osobni/leitner/prednasky/fchr/FCHR.htm
77.1 .1 Kalorimetrie - úvod, přehled metodKalorimetrie - úvod, přehled metod
77.2 .2 Měření tepelných kapacitMěření tepelných kapacit
77.3 .3 Měření rozpouštěcích tepelMěření rozpouštěcích tepel
7.4 Měření reakčních tepel7.4 Měření reakčních tepel
77..55 Rovnovážné metody – fázové a chemické rovnováhyRovnovážné metody – fázové a chemické rovnováhy
7.6 Rovnovážné metody – měření EMN galvanických článků7.6 Rovnovážné metody – měření EMN galvanických článků

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
2
Experimentální metody získávání Experimentální metody získávání termodynamických dat pevných látektermodynamických dat pevných látek
http://www.vscht.cz/ipl/termodyn/uvod.htmhttp://www.vscht.cz/ipl/termodyn/uvod.htm

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
3
Vlastnost Jak na to
Tepelné kapacity Cpm
→ Sm = ∫(Cpm/T)dT
Relaxační časAdiabatická kalorimetrie (AC)Diferenční scanovací kalorimetrie (DSC)
Relativní entalpieHm(T) – Hm(Tref)
Vhazovací kalorimetrie (DROP)
Entalpie fázových přeměn I. řádu (ΔtrH, ΔfusH)
Diferenční scanovací kalorimetrie (DSC)Rozpouštěcí kalorimetrie
Slučovací entalpie ΔslH
Reakční kalorimetrie• přímé slučování• jiná reakce (spalování, …)Rozpouštěcí kalorimetrie
Směšovací entalpie ΔHM Směšovací kalorimetrieRozpouštěcí kalorimetrie
Kalorimetrické metodyKalorimetrické metodyMěření termofyzikálních a termochemických veličin
(Cp, H(T2)-H(Tref), ΔtrH, ΔfusH, ΔrH, ΔsolH, ΔH M )

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
4
Klasifikace kalorimetrůKlasifikace kalorimetrů
cc s
dd
d d
TqC K T T
t t
► Izotermní: ΔT = 0, Ts = konst.
► Adiabatický: ΔT = 0, Ts konst.
► Izoperibolický: ΔT 0, Ts = konst.
► Heat-flow: ΔT = konst., Ts konst.
TsTc dZdroj : =
d
t
cdAkumulace :
d
TC
t
Přestup: K T Tc s

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
5
Metoda 10-1 K 100 K 101 K 102 K 103 K
Tepelně pulzníACDSC
DROP
Měření tepelných kapacitMěření tepelných kapacita relativních entalpiía relativních entalpií
m0
lim p mp
Tp
q HC
T T
ref
m m ref m dT
p
T
H T H T C T

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
6
Tepelně pulzní kalor.PPMS (Quantum Design)
2 – 300 K
Hmotnost 15 mg
Přesnost ± 2 %.
m 0x
p xx
MC c c
m
2
max
RIC
T
0 20 40 60 800,0
0,1
0,2
0,3
0,4
0,5
0,6
0,7
T [
K]
t [s]
max expt
T t T
Měření tepelných kapacit Měření tepelných kapacit (1)(1)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
7
LT FitExperimentální Cp data (2-300 K)
a) T < 10 K
2el
pmCT
T
3D
3el ph elpmC C C T T
γel
ΘD
CaNbCaNb22OO66
2 3el D,pmC T cT

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
8
LT FitExperimentální Cp data (2-300 K)
b) T = 10 – 360 K
Metoda trial-and-error + optimalizace (simplex)
Cpm(298,15), Hm(298,15) Hm(0), Sm(298,15)
33
1phEphDph
n
iiCCC
x
x
xx
Θ
T
TC d
1)exp(
)exp(
1
9 Dx
02
43
DDphD
R
2E
E2E
EphE
1exp
exp
1
i
ii
ii
x
xx
TC
R
ΘE αE αD

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
9
Měření tepelných kapacit Měření tepelných kapacit (2)(2)
PPMS (Quantum Design)
0 50 100 150 200 250 300 350 4000
50
100
150
200
Cp
m (
J K
-1m
ol-1
)
T (K)
RT-Exp DSC-Exp LT-Fit
0 10 20 30 40 50 600
2
4
6
8
10
12
T2 (K2)
Cpm
/T (
mJ
K-2m
ol-1)
CaNbCaNb22OO66

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
10
• Kelímek 0,45 cm3 (korund nebo Pt)• Teplota 300 - 1450 oC• Rychlost ohřevu 0,01 - 20 oC/min• Kontinuální nebo krokový režim• Plynná atmosféra definovaného složení (statická nebo dynamická)
• Kalibrace - Al2O3 (standard NIST No.720)
Měření tepelných kapacit Měření tepelných kapacit (3)(3)
Multi HTC 96 SETARAM (Francie)HF-DSC

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
11
Měření tepelných kapacit Měření tepelných kapacit (4)(4)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
12
Tři měření: blank(b), reference(r), vzorek(s)
Postup:1) integrace píků2) korekce ploch píků na blank
Pr,kor = Pr - Pb, Ps,kor = Ps - Pb
3) výpočet sensitivity S = Qr /Pr,kor, Qr = nr ∫Cpm,r dT
4) výpočet hodnoty molární tepelné kapacity vzorkuQs = S.Ps,kor, Cpm,s = Qs /T/ns
Měření tepelných kapacit Měření tepelných kapacit (5)(5)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
13
• Kelímek 5 cm3 (korund nebo Pt)• Teplota 300 - 1500 oC• Plynná atmosféra definovaného složení (statická nebo dynamická)
• Kalibrace - Al2O3 (standard NIST No.720)
Multi HTC 96 SETARAM (Francie)
Měření relativních entalpií Měření relativních entalpií (1)(1)
DROP

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
14
Měření relativních entalpií Měření relativních entalpií (2)(2)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
15
Vyhodnocení experimentálních dat (1)
Přímá měření tepelných kapacit [Ti,Cpm,i]
m 2
CA BpC T
T
2
m, 2
CA B minp i i
i i
F C TT
m, 2
m, 2
m, i 2 2
C2 A B ( 1) 0
A
C2 A B ( ) 0
B
C 12 A B ( ) 0
C
p i ii i
p i i ii i
p ii i i
FC T
T
FC T T
T
FC T
T T

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
16
m 2
CA BpC T
T
2
2 2m,
B 1 1A 298 298 C min
2 298i i ii i
F H T TT
29811
C2982B
298-TA)298()( 22mm T
THTH
min298
CB298A)298(λ 2pmVP
CFF
Vyhodnocení experimentálních dat (2)
Měření relativních entalpií [Ti,Hm,i]
m 298,15KpC

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
17
Vyhodnocení teplotní závislost Cpm pro FeAsz měření relativních entalpií (1)
800 900 1000 1100 1200 130025
30
35
40
45
50
55
60
65
70
75
Cpm
(298) = 50,36 J.K-1.mol
-1
A = 32.696B = 0.0411C = 4,807E5 = 245,8
A = -9.988B = 0.0757C = 6,459E6 = 36,08
Cpm
= A + B.T + C/T2
- VP + VP
FeAs
H
m(T
)-H
m(2
98)
[kJ.
mol
-1]
T [K]

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
18
300 400 500 600 700 800 900 1000 1100 1200
50
55
60
65
70
75
80
85
90
84,47
50,36
- VP
+ VP
FeAs
C
pm [J
.K-1.m
ol-1]
T [K]
Vyhodnocení teplotní závislost Cpm pro FeAsz měření relativních entalpií (2)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
19
HT FitExperimentální Cp data + H data + Cpm(298,15)
2
CA BpmC T
T
, ,
2 2
m,exp m,calc ,exp ,calc2 2
1 1( , , ) min
Cp H
p i m i
N N
p p m mi ii iC H
F A B C C C H H
m2
CA 298,15 298,15 K, LT-Fit
298,.5 pB C
m dpmH C T A B C

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
20
0 200 400 600 800 1000 1200 14000
50
100
150
200
2503NR
C
pm (
J K
-1 m
ol-1
)
T (K)
RT-Exp DSC-Exp LT-Fit HT-Fit (Eq.4) NKR
CaNbCaNb22OO66
Vyhodnocení experimentálních dat (2)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
21
Měření rozpouštěcích tepel Měření rozpouštěcích tepel (1)(1)
o oA 0 A A A AA , A-B , , A-B , ,n s T n l T x n n l T x x
osol m A m 0
A
o o Mm m 0 fus m A
(A) A, , , A, ,
A, , A, , A, , A, , ,
HH H l T x H s T
n
H s T H s T H s T H l T x
Rozpouštění Pd(s) v [Ag-Pd](l)T0= 299 K
T = 1702 K
(TF(Pd) = 1828 K)
no(Pd,s) = 0,387 mmol (41,2 mg)
no(Ag,l) = 5,575 mmol (601,4 mg)
x(Pd,l) = 0.0649
Q = 13,145 J
ΔH M(Pd) = -24349 J mol-1
13.15
16.09
6.48
-9.43
-15
-10
-5
0
5
10
15
20
H (J
)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
22
Měření rozpouštěcích tepel Měření rozpouštěcích tepel (2)(2)
Rozpouštědlo Rozpouštěné látky Teplota (K) Stanovená veličina
HCl Mg2Zn3 298 K ΔfH(Mg2Zn3)
HCl BaCuO2 298 K ΔfH(BaCuO2)
HF/HNO3
Li2O-Al2O3-SiO2(gl)
Li2O-Al2O3-SiO2(cr)298 K ΔcrystH
Al Ce, Ni, CeNi2 1095 K ΔfH(CeNi2)
Ge Cr 1300 K ΔH M[Cr-Ge](l)
2PbO.B2O3
Al2O3, Y2O3,
YAlO3, Y3Al5O12
977 KΔfH(YAlO3)
ΔfH(Y3Al5O12)
3Na2O.4MoO3 Li3N 979 K ΔfH(Li3N)
3Na2O.4MoO3 LiFeO2(α), LiFeO2(β) 974 K ΔtrH(LiFeO2)
3Na2O.4MoO3
Fe3O4, Mn3O4,
(Fe1–xMnx)3O4
976 K ΔH M(Fe1–xMnx)3O4
ethanol/chloroformkofein(cr,I)kofein(cr,II)
298 ΔtrH(C8H10N4O2)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
23
Měření rozpouštěcích tepel Měření rozpouštěcích tepel (3)(3)
Příklad 1: Stanovení parciálních molárních směšovacích entalpií
M o oPd sol Pd m m 0 fus m
Pd
1Pd, , , (Pd) Pd, , Pd, , Pd, ,H l T x H n H s T H s T H s T
n
Luef C. et al. : J. Alloys Compounds 391, 67-76 (2005)
Vzor.n(Pd)
(mmol)
Σn(Pd)
(mmol)x(Pd)
(mJ) (J mol-1) (J mol-1)
1 0.387 0.387 0.06 13145 -24349 -1581
2 0.387 0.774 0.12 12599 -25714 -3050
3 0.409 1.182 0.17 17560 -15344 -3793
4 0.438 1.620 0.23 17391 -18568 -4692
5 0.457 2.076 0.27 20298 -13851 -5238
6 0.465 2.542 0.31 22272 -10443 -5537
7 0.488 3.029 0.35 27647 -1617 -5315
8 0.513 3.543 0.39 27296 -5135 -5304
9 0.528 4.071 0.42 29132 -3135 -5186
10 0.556 4.626 0.45 31136 -2286 -5028
11 0.470 5.096 0.48 27535 292 -4793
sol PdH M PdH MmH

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
24
Měření rozpouštěcích tepel Měření rozpouštěcích tepel (4)(4)
Příklad 1: Pokračování
0.0 0.1 0.2 0.3 0.4 0.5 0.6-40000
-30000
-20000
-10000
0
run #1 (1399 °C) run #2 (1429 °C) run #3 (1429 °C) RK equation
H M
(Pd)
(Jm
ol-1)
xPd(Ag-Pd)
0.0 0.1 0.2 0.3 0.4 0.5 0.6
-6000
-5000
-4000
-3000
-2000
-1000
0 run #1 (1399 °C) run #2 (1429 °C) run #3 (1429 °C) RK equation
H M
(Jm
ol-1
)x
Pd(Ag-Pd)
Mm Ag Pd Ag Pd19141 15925H x x x x
M o osol Pd m m 0 fus mo
Ag Pd
1Ag-Pd, , (Pd) Pd, , Pd, , Pd, ,H l T H n H s T H s T H s T
n n

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
25
Měření rozpouštěcích tepel Měření rozpouštěcích tepel (5)(5)
Kanke Y., Navrotsky A. : J. Solid State Chem. 141, 424-436 (2005)
REsolHm(RE2O3)
(kJ mol-1)
solHm(REAlO3)
(kJ mol-1)
oxH(REAlO3)#
(kJ mol-1)
Y -61,7 ± 1,1 9,24 ± 1,72 -23,62 ± 1,83
La -126,0 ± 4,4 16,64 ± 1,19 -63,17 ± 2,52
Nd -89,1 ± 5,7 15,28 ± 2,88 -41,36 ± 3,44
Sm -79,4 ± 4,1 14,32 ± 2,52 -37,55 ± 3,26
Eu -68,4 ± 1,3 12,79 ± 2,50 -30,52 ± 2,60
Gd -72,6 ± 3,4 12,50 ± 2,40 -32,33 ± 2,96
Dy -50,9 ± 1,2 12,41 ± 1,17 -21,39 ± 1,35
# oxH(REAlO3) = ½[solHm(RE2O3) + solHm(Al2O3)] – solHm(REAlO3), solHm(Al2O3) = 32,9 ± 0,6 kJ mol-1
o o of 0 m 0 m 0 m 0
sol sol
A B , , A B , , A, , B, ,
A B A B
a b a b
a b
H s T H s T aH s T bH s T
H a b H
Příklad 2: Stanovení slučovacích entalpií

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
26
Direct synthesis calorimetry(Prof. Kleppa, University of Chicago)Intermetalické sloučeniny, boridy, karbidy, silicidy, arsenidy…La(s,298) + 2C(s,298) = LaC2(s,1473)
LaC2(298) = LaC2(s,1473)
Fluorine combustion calorimetry(Dr. O’Hare, NIST)Silicidy, nitridy, sulfidy, teluridy, ...Mo3Si(s) + 11F2(g) = 3MoF6(g) + 3SiF4(g)
Si3N4(s) + 6 F2(g) = 3 SiF4(g) + 2N2(g)
Měření reakčních tepel Měření reakčních tepel (1)(1)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
27
Měření reakčních tepel Měření reakčních tepel (2)(2)
Příklad 3: Stanovení slučovací entalpie ze spalných tepel
2 4 6GeTe(s) + 5F (g) = GeF (g) + TeF (g)
GeTe(s)T = 298,15 KSpalné teplo Q[V] = -12721 J g-1
MGeTe = 200,21 g mol-1
or r r g
3 112,721 200,21 3 298,15 8,314.10 2554,3 kJ mol
H U V p U n T
R
o o o of r f 4 f 6
1
GeTe,s GeF ,g TeF ,g
2554,3 1191,8 1380,7 18,2 kJ mol
H H H H
Tomaszkiewicz I. et al. : J. Chem. Thermodynamics 27, 901-919 (1995)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
28
RovnovážnéRovnovážné metody metodyMěření rovnovážných konstant chemických reakcí (→ G)
Měření EMN galvanických článků (→ G)
1
A 0N
i ii
Obecná chemická reakce
Rovnovážná konstanta
or
1
expi
N
ii
G Ta K T
T
R
o o o o or r r m m
1 1
N N
i ii i
G T H T T S T v H T T v S T

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
29
Experimentální stanovení rovnovážné konstantyExperimentální stanovení rovnovážné konstanty
4 2 3SiCl (g) + H (g) = SiHCl (g) + HCl(g)
3
4 2
SiHCl HCl
SiCl H
p pK T
p p
4 2SiCl (g) + 2H (g) = Si(s) + 4HCl(g)
4 2
4 2 4 2
44HCl
Si22 o o o oSiCl H SiCl H SiCl H
4;
2
p pK T n
p p n n n n

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
30
Zpracování rovnovážných dat Zpracování rovnovážných dat (1)(1)
2nd law analysis
Z teplotní závislost rovnovážné konstanty současně určíme hodnoty teplotně nezávislé standardní reakční entalpie rHo(Ts ) a teplotně
nezávislé standardní reakční entropie rSo(Ts ) pro střední teplotu
měření Ts = ½(Tmax+Tmin). Pro studovanou látku musíme znát
teplotní závislost Cpm(T).
o o or r s r slnG T S T H T
K TT T
R R R

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
31
Zpracování rovnovážných dat Zpracování rovnovážných dat (2)(2)
0.6 0.8 1.0 1.2 1.4 1.6 1.8 2.00
4
8
12
16
ln K
1000/T (K-1) o
r sS T A R
lnB
K AT
s
ro o or s r m
1298,15
d 298,15K ( )T N
pi
i
CS T T S S i
T
s
o o or s r r sl
1298,15
d 298,15K ( )T N
p ii
H T C T H H i
or sH T B R

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
32
Zpracování rovnovážných dat Zpracování rovnovážných dat (4)(4)
3rd law analysis
Z hodnoty rovnovážné konstanty při dané teplotě Tj určíme hodnotu
standardní reakční entalpie rHo(298,15 K). Pro studovanou látku
musíme znát teplotní závislost Cpm(T) a hodnotu Som(298,15 K).
or
lnj
j
G TK T
T
R
ro or r r
298,15 298,15
o or sl
1
298,15K d d
298,15K ( )
j jT T
pj j p
N
ii
CG T T S T C T
T
H H i
o o om m mo o
m m
298,15 298,15
298,15K1298,15K d d -funkce
T Tp
p
C G T HS T C T G
T T T

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
33
Zpracování rovnovážných dat Zpracování rovnovážných dat (3)(3)
Příklad 4: Stanovení slučovací entalpie z rovnovážných dat
Iway T. et al.: Metall. Trans. A 17A, 2031-2033 (1986)
2 4WC(s) + 2H (g) = W(s) + CH (g)
T (K) 103/T (K-1) 104 prel(CH4) 104 K lnK
1173 0,853 4,637 4,641 -7,675
1223 0,818 4,108 4,111 -7,797
1273 0,786 3,377 3,380 -7,992
1273 0,786 3,395 3,397 -7,987
1273 0,786 3,393 3,395 -7,988
1323 0,756 2,929 2,931 -8,135
1373 0,728 2,322 2,323 -8,367
1373 0,728 2,274 2,275 -8,388
1423 0,703 2,069 2,069 -8,483
1473 0,679 1,777 1,778 -8,635
1523 0,657 1,593 1,593 -8,745
1573 0,636 1,448 1,448 -8,840
0.6 0.7 0.7 0.8 0.8 0.9-9.0
-8.8
-8.6
-8.4
-8.2
-8.0
-7.8
-7.6lnK = 5,696*(1000/T) - 12,486
ln K
1000/T (K-1)
or
o o -1r r
max min
ln
47357 J, 103,81JK
2 1373K
G aK b
T T
H a S b
T T T
R
R R
4
2
CH
2H
pK
p

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
34
Zpracování rovnovážných dat Zpracování rovnovážných dat (5)(5)
Příklad 4: Pokračování
Iway T. et al.: Metall. Trans. A 17A, 2031-2033 (1986)
o o or r r m
298,15
or mo o -1
r r
298,15
298,15K d 47357 19904 27453J
298,15K d 103,81 34,56 69,25JK
T
p
Tp
H H C T
CS S T
T
o o o -1sl r sl 4
o o o o om r m 4 m m 2
-1 -1
WC,298,15K 298,15K CH ,298,15K 27453 74872 47419Jmol
WC,298,15K 298,15K CH ,298,15K W,298,15K 2 H ,298,15K
69,25 186,25 32,66 2 130,68 26,80JK mol
H H H
S S S S S
o -1sl
o -1 -1m
Tabelované hodnoty (Barin, 1993)
WC,298,15K 40166Jmol
WC,298,15K 32,384JK mol
H
S

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
35
Zpracování rovnovážných dat Zpracování rovnovážných dat (5)(5)
T (K) 104 prel(CH4) 104 K ΔrGo(T ) (J) ΔrHo(298,15 K) (J)
1173 4,637 4,641 74853 -33017
1223 4,108 4,111 79277 -33998
1273 3,377 3,380 84590 -34101
1273 3,395 3,397 84537 -34154
1273 3,393 3,395 84543 -34148
1323 2,929 2,931 89480 -34641
1373 2,322 2,323 95516 -34043
1373 2,274 2,275 95754 -33805
1423 2,069 2,069 100364 -34642
1473 1,777 1,778 105747 -34711
1523 1,593 1,593 110728 -35188
1573 1,448 1,448 115611 -35764
or
o o o -1sl r sl 4
298,15K 34351J
WC,298,15K 298,15K CH ,298,15K 34351 74872 40521Jmol
H
H H H
Příklad 4: Pokračování

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
36
Napětí článku je rozdíl elektrodových potenciálů (závisí na protékajícím proudu I ). Elektromotorické napětí článku (EMN) je napětí
nezatíženého článku (proud I → 0)
anoda oxidace, katoda redukce
Měření EMN galvanických článků (1)

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
37
Měření EMN galvanických článků (2)
G z E F
Probíhá-li v článku při [T,p] vratný děj, pak platí
p p
G ES z
T T
F
p
EH G T S z E T
T
F

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
38
Koncentrační (Concentration)
Základní typy galvanických článků
Chemické (Formation)
2 2Mg(s) MgCl (l) Cl (g)
2
2
MgCl (l)or r
Cl (g)
lna
G G G Tp
R
2 2Mg(s) + Cl (g) = MgCl (l)
2 2 2Mg(l),MgF (s) CaF (s) MgF (s),[Mg-Sn](l)
Mg Mg[Mg-Sn]Mg(l, = 1) = Mg(l, < 1)a a
MMg Mg[Mg-Sn](l)lnG G T a R

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
39
Vodné roztoky anorganických látek (HCl, H2SO4, …)
Používané elektrolyty (1)
2 2 2H S(g),W(s),WS (s) HCl(aq) H (g)
+2 2: 2H S(g) + W(s) = WS (s) + 4H + 4e
+2: 4H + 4e = 2H (g)
2 2 2W(s) + 2H S(g) = WS (s) + 2H (g)
2
2
2
Hor r
H S
ln 4p
G G T Ep
R F

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
40
Roztavené soli (NaCl-KCl, LiCl-KCl-PbCl2, LiCl-LiF, AgBr-LiBr, …)
Používané elektrolyty (2)
2Mg(l) LiCl-KCl-MgCl (l) [Mg-Al](l)
2: Mg(l) + 2Cl = MgCl (l) + 2e
2: MgCl (l) + 2e = Mg(l,[Mg-Al]) + 2Cl
Mg(l) = Mg(l,[Mg-Al])
Mg[Mg-Al](l)ln 2T a ER F

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
41
Pevné elektrolyty (ZrO2-CaO, HfO2-Y2O3, Na2O-xAl2O3, CaF2, MgF2)
Používané elektrolyty (3)
2 2 2 2 2 3 2O (g),BaO(s),BaF (s) BaF (s) BaF (s),ZrO (s),BaZrO (s),O (g)
2 2: 2BaO(s) + 4F = 2BaF (s) + O (g) + 4e
2 2 2 3: 2BaF (s) + 2ZrO (s) + O (g) + 4e = 2BaZrO (s) + 4F
2 2 32BaO (s) + 2ZrO (s) = 2BaZrO (s)
o oox 2G E F

42
Galvanické články s pevnými elektrolyty

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
43
Příklad 5: Stanovení slučovací entalpie z EMN
Galvanické články s pevnými elektrolyty
2 4 2 2 3 2 3Cr(s),CaO(s),CaCr O (s) ThO -Y O (s) Cr(s),Cr O (s)
Jacob K.T. et al. : J. Electrochem. Soc. 139, 517-520 (1992)
2 3 2 4CaO(s) + Cr O (s) = CaCr O (s)
21050 1475K : mV 105,3 1,95.10T E T
Elektrodové reakce:
22 4: CaO(s) + 2Cr(s) + 3O = CaCr O (s) + 6e
22 3: Cr O (s) + 6e = 2Cr(s) + 3O
Úhrnná reakce v článku:

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
44
Příklad 5: Stanovení slučovací entalpie z EMN
Galvanické články s pevnými elektrolyty
Jacob K.T. et al. : J. Electrochem. Soc. 139, 517-520 (1992)
2 3 2 4CaO(s) + Cr O (s) = CaCr O (s)
Úhrnná reakce v článku:
o 1 o 2 3ox Jmol 6 6 96500 105,3 1,95.10 .10 60969 11,291G E T T F
o 1 o 1 1ox ox60969 Jmol 11,291 JK molH S
o o o of 2 4 ox f f 2 3
1
CaCr O CaO Cr O
60,97 635,09 1140,56 1836,62 kJmol
H H H H

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
45
Galvanické články s pevnými elektrolyty
Příklad 5: Stanovení slučovací entalpie z EMN
Příklad 6: Stanovení aktivity z EMN
22 4: CaO(s) + 2Cr(s) + 3O = CaCr O (s) + 6e
22 3: Cr O (s) + 6e = 2Cr(s) + 3O
22 3: 2Cr(s) + 3O = Cr O (s) + 6e
22 3: Cr O (s) + 6e = 2Cr(l) + 3O
2 3 2 4CaO(s) + Cr O (s) = CaCr O (s)
Cr(s) = Cr(l,[Cr-Ni])

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
46
Příklad 6: Stanovení aktivity z EMN
Galvanické články s pevnými elektrolyty
2 3 2 2 3Cr(s),Cr O (s) ZrO -MgO(s) [Ni-Cr](l),Cr O (s)
Katayama Y. et al.: Trans. Jpn. Inst. Metals 28, 558-563 (1987)
Cr 0,5 : mV 275,5 0,17x E T
Cr(s) = Cr(l,[Cr-Ni])
22 3: 2Cr(s) + 3O = Cr O (s) + 6e
22 3: Cr O (s) + 6e = 2Cr(l) + 3O
Elektrodové reakce:
Úhrnná reakce v článku:

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
47
Příklad 6: Stanovení aktivity z EMN
Galvanické články s pevnými elektrolyty
Katayama Y. et al.: Trans. Jpn. Inst. Metals 28, 558-563 (1987)
Úhrnná reakce v článku:
3 1fus Cr[Cr-Ni](l)Cr ln 3 3 96500 275,5 0,17 .10 JmolG G T a E T R F
11783K : 8199,6 JmolT G
Cr(s) = Cr(l,[Cr-Ni])
1Cr[Cr-Ni](l)
17831783K : ln 8199,6 20497 1 11538,78 J mol
2130T T a
R
Cr[Cr-Ni](l) 0,46a

3.11.2010 J.Leitner - Ústav inženýrství pevných látek, VŠCH Praha
48
Literatura
Kubaschewski O., Alcock C.B., Spencer P.J.: Materials Thermochemistry, 6th Ed., Chap.2. Experimental Methods, Pergamon, 1993. Höhne G.W.H., Hemminger W.F., Flammersheim H.-J.: Differential Scanning Calorimetry, 2nd.Ed. Springer, Berlin-Heidelberg 2003. Marsh K.N., O’Hare P.A.G. (Eds.): Solution Calorimetry, Experimental Thermodynamics, Vol. IV, Blackwell, Oxford 1994. Pratt J.N.: Applications of solid electrolytes in thermodynamic studies of materials: a review, Metallurgical Transactions A: Physical Metallurgy and Materials Science 21A (1990) 1223-50. Komarek K. L.: Experimental techniques in high-temperature thermodynamics, Pure and Applied Chemistry 64 (1992) 93-102. Mallika C., Sreedharan O.M., Subasri R.: Use of air/platinum as the reference electrode in solid oxide electrolyte e.m.f. measurements, Eur. Ceram. Soc. 20 (2000) 2297-2313. Kleykamp H.: Highlights of experimental thermodynamics in the field of nuclear fuel development, J. Nuclear Mater. 344 (2005) 1-7.