Atom 2003
Click here to load reader
-
Upload
andrija-denic -
Category
Documents
-
view
215 -
download
4
Transcript of Atom 2003

Atom 1
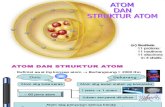
ATOM
Atom (grčki άτομον (atomon) - nedeljiv) je najmanji delić supstance, tj. hemijskog elementa koji ispoljava sve osobine tog
hemijskog elementa. Atom se sastoji od 3 tipa subatomskih čestica:
Elektrona, koji imaju negativno naelektrisanje i zanemarljivo malu masu;Protona, sa pozitivnim naelektrisanjem i
jediničnom masom; iNeutrona, koji imaju jediničnu masu ali
nisu naelektrisani.

Atom 2
Hemijske osobine atoma određuje broj protona u njemu (redni broj), a masu
broj protona i broj neutrona. Atom kao celina je neutralan jer sadrži isti broj
elektrona i protona. Atom postaje naelektrisan tako što primi ili otpusti jedan ili više elektrona i postaje jon.
Hemijske osobine atoma ne zavise od broja neutrona, pa postoje atomi istog elementa sa različitim brojem neutrona
- izotopi.

Atom 3
Atomska jezgra sa nepovoljnim odnosom broja protona i broja neutrona su
nestabilna i putem radioaktivnog raspada prelaze u stabilnije stanje. Osim
navedenih elementarnih čestica postoji čitav niz drugih koje ulaze u sastav atoma
kao što su: mezoni, pozitroni, neutrino itd...
Na današnjem nivou nauke smatra se da elementarne čestice nemaju unutrašnju
strukturu i da su nedeljive i nedimenzionalne.

Atom 4
Elektroni u atomu su raspoređeni u elektronske nivoe. Složeniji atomi
imaju veći broj elektronskih nivoa. Broj nivoa u atomu ne može preći sedam.
U prvom elekrtonskom nivou atom može imati najviše dva elektrona. U poslednjem, sedmom elektronskom
nivou, atom može imati najviše 8 elektrona. Poslednji elektronski nivo se
naziva valentni elektronski nivo i ukoliko ima 8 elektrona dostiže tzv.

Atom 5
Ova konfiguracija može da se postigne i u jedinjenima prilikom obrazovanja tzv.
zajedničkog elektronskog para u kovalentnoj vezi.
Elektronski nivoi su obeleženi slovima latinice: K, L, M, N, O, P i Q.
Elektron može da kruži u orbitalama ili nivoima na 4 različita načina. To su s, p, d i
f orbitale.Raspored orbitala (ili nivoa) u atomu
izgleda ovako: