4 ANTIBODI MONOKLONAL - ashfarkurnia.files.wordpress.com · Ikatan antigen antibodi mengaktivasi...
Transcript of 4 ANTIBODI MONOKLONAL - ashfarkurnia.files.wordpress.com · Ikatan antigen antibodi mengaktivasi...

46
4
ANTIBODI MONOKLONAL
4.1 PENDAHULUAN
Satu abad yang lalu Paul Ehrlich dengan hipotesisnya menyatakan bahwa magic bullet dapat
dikembangkan sebagai target selektif pada suatu penyakit. Visi ini menjadi kenyataan setelah
ditemukannya pengembangan teknik pembuatan antibodi monoklonal oleh Kőhler dan
Milstein pada tahun 1975, hal ini membuka wawasan baru di bidang kesehatan. Antibodi
monoklonal sebagai targeting missiles merupakan imunoterapi yang menjanjikan karena
memiliki sifat mengikat secara spesifik terhadap suatu target antigen atau sel abnormal
sehingga antibodi monoklonal sangat efektif untuk dipakai sebagai dasar terapi kanker.
Antibodi monoklonal sebagai terapi kanker diinjeksikan ke dalam tubuh pasien, molekul itu
akan mencari sel kanker (antigen) sebagai target. Antibodi monoklonal secara potensial
merusak atau menghancurkan aktivitas sel kanker atau dengan cara lain yaitu meningkatkan
respons imun jaringan tubuh melawan kanker. (Adams, G.P., et al., 2005; VonMehren, M., et
al., 2003)
Beberapa jenis kemoterapi dengan target kerja yang selektif (targeted therapy) mulai
digunakan untuk Kanker Paru Karsinoma Bukan Sel Kecil (KPKBSK). Obat-obatan
golongan ini diindikasikan pemberiannya sebagai adjuvan yaitu diberikan setelah pemberian
terapi definitif (kemoterapi atau radioterapi) selesai diberikan. Jenis terapi target antibodi
monoklonal yang mulai digunakan pada KPKBSK adalah obat yang bekerja sebagai inhibitor
epidermal growth factor receptor (EGFR) dan inhibitor vascular endothelial growth factor
(VEGF). (Adams, G.P., et al., 2005)
4.2 DEFINISI
Antibodi merupakan campuran protein di dalam darah dan disekresi mukosa menghasilkan
sistem imun bertujuan untuk melawan antigen asing yang masuk ke dalam sirkulasi darah.
Antibodi dibentuk oleh sel darah putih yang disebut limfosit B. Limfosit B akan

47
mengeluarkan antibodi yang kemudian diletakkan pada permukaannya. Setiap antibodi yang
berbeda akan mengenali dan mengikat hanya satu antigen spesifik. Antigen merupakan suatu
protein yang terdapat pada permukaan bakteri, virus dan sel kanker. Pengikatan antigen akan
memicu multiplikasi sel B dan penglepasan antibodi. Ikatan antigen antibodi mengaktivasi
sistem respons imun yang akan menetralkan dan mengeliminasinya. Antibodi memiliki ber-
bagai macam bentuk dan ukuran walaupun struktur dasarnya berbentuk `Y`(gambar 4.1).
Antibodi tersebut mempunyai 2 fragmen, fragmen antigen binding (Fab) dan fragmen
cristallizable (Fc). Fragmen antigen binding digunakan untuk mengenal dan mengikat
antigen spesifik, tempat melekatnya antigen antibodi yang tepat sesuai regio yang bervariasi
disebut complementary determining region (CDR) dan Fc berfungsi sebagai efektor yang
dapat berinteraksi dengan sel imun atau protein serum. (Albert, B., et al., 2002; Abbas, A.K.,
2005; Nelson, P.N., et al., 2000)
Gambar 4.1 Struktur umum antibodi
Antibodi monoklonal adalah antibodi buatan identifik karena diproduksi oleh salah
satu jenis sel imun saja dan semua klonnya merupakan sel single parent. Antibodi
monoklonal mempunyai sifat khusus yang unik yaitu dapat mengenal suatu molekul,
memberikan informasi tentang molekul spesifik dan sebagai terapi target tanpa merusak sel
sehat sekitarnya. Antibodi monoklonal murni dapat diproduksi dalam jumlah besar dan bebas
kontaminasi. Antibodi monoklonal dapat diperoleh dari sel yang dikembangkan di
laboratorium, reagen tersebut sangat berguna untuk penelitian terapi dan diagnostik
laboratorium. (Albert, B., et al., 2002; Abbas, A.K., 2005; Nelson, P.N., et al., 2000)

48
Antibodi monoklonal dapat diciptakan untuk mengikat antigen tertentu kemudian
dapat mendeteksi atau memurnikannya. Manusia dan tikus mempunyai kemampuan untuk
membentuk antibodi yang dapat mengenali antigen. Antibodi monoklonal tidak hanya
mempertahankan tubuh untuk melawan organisme penyakit tetapi juga dapat menarik
molekul target lainnya di dalam tubuh seperti reseptor protein yang ada pada permukaan sel
normal atau molekul yang khas terdapat pada permukaan sel kanker. Spesifisitas antibodi
yang luar biasa menjadikan zat ini dapat digunakan sebagai terapi. Antibodi mengikat sel
kanker dan berpasangan dengan zat sitotoksik sehingga membentuk suatu kompleks yang
dapat mencari dan menghancurkan sel kanker. (Albert, B., et al., 2002; Abbas, A.K., 2005;
Nelson, P.N., et al., 2000)
4.3 ANTIBODI MONOKLONAL REKOMBINAN
Pemanfaatan antibodi monoklonal dalam bidang kesehatan, baik untuk diagnostik atau
mengatasi penyakit kanker tertentu, telah banyak dilakukan. Beberapa antibodi monoklonal
yang dilakukan untuk pengobatan berasal dari sel mencit atau tikus, sering menimbulkan
reaksi alergi pada pasien yang menerima terapi antibodi monoklonal tersebut. Hal ini
disebabkan karena protein mencit dikenal sebagai antigen asing oleh sel tubuh pasien,
sehingga menimbulkan reaksi respon imun antara lain berupa alergi, inflamasi dan
penghancuran atau destruksi antibodi monoklonal itu sendiri. Untuk mengatasi hal tersebut
maka dikembangkanlah antibodi monoklonal rekombinan manusia, yaitu suatu monoklonal
antibodi yang sebagian atau seluruhnya terdiri dari protein yang berasal dari manusia, untuk
mengurangi efek penolakan oleh sistem imun pasien. (Radji, M., 2011; Tuscano, J.M., et al;
2005)
Beberapa jenis antibodi monoklonal generasi baru yang telah dikembangkan antara
lain:
1. Antibodi monoklonal murine (fully mouse)
Yaitu antibodi murni yang didapatkan dari tikus. Antibodi ini dapat menyebabkan
human anti mouse antibodies (HAMA). Biasanya antibodi ini memiliki akhiran
dengan nama “momab” (contohnya Ibritumomab®
). (Radji, M., 2011; Tuscano, J.M.,
et al; 2005)
2. Antibodi monoklonal kimera (chimaric)
Antibodi monoklonal ini dibuat melalui teknik rekayasa genetika untuk menciptakan
galur mencit atau tikus transgenik yang dapat memproduksi sel hybrid mencit-
manusia yang disebut kimera (chimaric). Bagian variabel molekul antibodi (Fab),

49
termasuk bagian antigen binding site, berasal dari mencit, sedangkan bagian lainnya,
yaitu bagian yang constant (Fc) berasal dari manusia. Memiliki akhiran dengan nama
“ximab” (Rituximab®). (Radji, M., 2011; Tuscano, J.M., et al; 2005)
3. Antibodi monoklonal manusiawi (humanized)
Antibodi ini dibuat secara rekayasa genetika dimana bagian protein yang berasal dari
mencit hanya terbatas pada antigen binding site saja, sedangkan bagian yang lainnya
yaitu bagian variable dan bagian konstan berasal dari manusia. Antibodi ini memiliki
akhiran nama “zumab” (Transtuzumab®
). (Radji, M., 2011; Tuscano, J.M., et al;
2005)
4. Antibodi monoklonal manusia (fully human)
Antibodi ini merupakan antibodi yang paling ideal untuk menghindari terjadinya
respon imun karena protein antibodi yang disuntikkan kedalam tubuh seluruhnya
merupakan protein yang berasal dari manusia. Salah satu pendekatan yang dilakukan
untuk merancang pembentukan antibodi monoklonal yang seluruhnya mengandung
protein manusia tersebut adalah dengan teknik rekayasa genetika untuk menciptakan
mencit transgenik yang membawa gen yang berasal dari manusia, sehingga mampu
memproduksi antibodi yang diinginkan. Pendekatan lainnya adalah merekayasa suatu
binatang transgenik yang dapat mensekresikan antibodi manusia dalam air susu yang
dikeluarkan oleh binatang tersebut. Antibodi yang 100% mengandung protein
manusia memiliki akhiran nama “mumab” (Panitumumab®). (Radji, M., 2011;
Tuscano, J.M., et al; 2005)
Gambar 4.2. Struktur antibodi monoklonal rekombinan. Dari yang paling kiri ke kanan;
antibodi monoklonal fully mouse, chimaric,. humanized, fully human.

50
4.4 CARA PEMBUATAN
Kőhler dan Milstein menjelaskan bagaimana caranya mengisolasi dan mengembangkan
antibodi monoklonal murni spesifik dalam jumlah banyak yang didapat dari campuran
antibodi hasil respons imun. Tikus yang telah diimunisasi dengan antigen khusus ke dalam
sumsum tulang akan menghasilkan sel limfosit B yang memiliki masa waktu hidup terbatas
dalam kultur, hal ini dapat diatasi dengan cara menggabungkan dengan sel limfosit B tumor
(myeloma) yang abadi. Hasil campuran heterogen sel hybridomas dipilih hybridoma yang
memiliki 2 kemampuan yaitu dapat menghasilkan antibodi khusus dan dapat tumbuh di
dalam kultur. Hybridoma ini diperbanyak sesuai klon individualnya dan setiap klon hanya
menghasilkan satu jenis antibodi monoklonal yang permanen dan stabil. Hybridoma yang
berasal dari satu limfosit akan menghasilkan antibodi yang akan mengenali satu jenis antigen.
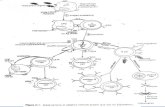
Antibodi inilah yang dikenal sebagai antibodi monoklonal (gambar 4.3).
Gambar 4.3. Skema pembuatan antibody monoklonal dari kultur tikus
Proses pembuatan antibodi monoklonal melalui 5 tahapan yaitu:
1. Imunisasi tikus dan seleksi tikus donor untuk pengembangan sel hybridoma Tikus
diimunisasi dengan antigen tertentu untuk menghasilkan antibodi yang diinginkan.

51
Tikus dimatikan jika titer antibodinya sudah cukup tercapai dalam serum kemudian
limpanya digunakan sebagai sumber sel yang akan digabungkan dengan sel myeloma.
2. Penyaringan produksi antibodi tikus Serum antibodi pada darah tikus itu dinilai
setelah beberapa minggu imunisasi. Titer serum antibodi ditentukan dengan berbagai
macam teknik seperti enzyme link immunosorbent assay (ELISA) dan flow cytometry.
Fusi sel dapat dilakukan bila titer antibodi sudah tinggi jika titer masih rendah maka
harus dilakukan booster sampai respons yang adekuat tercapai. Pembuatan sel
hybridoma secara in vitro diambil dari limpa tikus yang dimatikan.
3. Persiapan sel myeloma Sel myeloma yang didapat dari tumor limfosit abadi tidak
dapat tumbuh jika kekurangan hypoxantine guanine phosphoribosyl transferase
(HGPRT) dan sel limpa normal masa hidupnya terbatas. Antibodi dari sel limpa yang
memiliki masa hidup terbatas menyediakan HGPRT lalu digabungkan dengan sel
myeloma yang hidupnya abadi sehingga dihasilkan suatu hybridoma yang dapat
tumbuh tidak terbatas. Sel myeloma merupakan sel abadi yang dikultur dengan 8-
azaguanine sensitif terhadap medium seleksi hypoxanthine aminopterin thymidine
(HAT). Satu minggu sebelum fusi sel, sel myeloma dikultur dalam 8-azaguanine. Sel
harus mempunyai kemampuan hidup tinggi dan dapat tumbuh cepat. Fusi sel meng-
gunakan medium HAT untuk dapat bertahan hidup dalam kultur.
4. Fusi sel myeloma dengan sel imun limpa Satu sel limpa digabungkan dengan sel
myeloma yang telah dipersiapkan. Fusi ini diselesaikan melalui sentrifugasi sel limpa
dan sel myeloma dalam polyethylene glycol suatu zat yang dapat menggabung-kan
membran sel. Sel yang berhasil mengalami fusi dapat tumbuh pada medium khusus.
Sel itu kemudian didistribusikan ke dalam tempat yang berisi makanan, didapat dari
cairan peritoneal tikus. Sumber makanan sel itu menyediakan growth factor untuk
pertumbuhan sel hybridoma.
5. Pengembangan lebih lanjut kloning sel hybridoma kelompok kecil sel hybridoma
dapat dikembangkan pada kultur jaringan dengan cara seleksi ikatan antigen atau
dikembangkan melalui metode asites tikus. Kloning secara limiting dilution akan
memastikan suatu klon itu berhasil. Kultur hybridoma dapat dipertahankan secara in
vitro dalam tabung kultur (10-60 ug/ml) dan in vivo pada tikus, hidup tumbuh di
dalam suatu asites tikus. Konsentrasi antibodi dalam serum dan cairan tubuh lain 1-10
ug/ml.

52
4.5 MEKANISME KERJA
Antibodi monoklonal menggunakan mekanisme kombinasi untuk meningkatkan efek
sitotoksik sel tumor. Mekanisme komponen sistem imun adalah antibody dependent cellular
cytotoxicity (ADCC), complement dependent cytotoxicity (CDC), mengubah signal transduksi
sel tumor atau menghilangkan sel permukaan antigen. Antibodi dapat digunakan sebagai
target muatan (radioisotop, obat atau toksin) untuk membunuh sel tumor atau mengaktivasi
prodrug di tumor, antibody directed enzyme prodrug therapy (ADEPT). Antibodi
monoklonal digunakan secara sinergis melengkapi mekanisme kerja kemoterapi untuk
melawan tumor. (Adams, G.P., et al., 2005)
4.5.1 Antibody dependent cellular cytotoxicity (ADCC)
Antibody dependent cellular cytotoxicity (ADCC) terjadi jika antibodi mengikat antigen sel
tumor dan Fc antibodi melekat dengan reseptor Fc pada permukaan sel imun efektor.
Interaksi Fc reseptor ini berdasarkan kemanjuran antitumor dan sangat penting pada
pemilihan suatu antibodi monoklonal. Sel efektor yang berperan masih belum jelas tapi
diasumsikan sel fagosit mononuklear dan atau natural killer (NK). Struktur Fc domain
dimanipulasi untuk menyesuaikan jarak antibodi dan interaksi dengan Fc reseptor. Antibody
dependent cellular cytotoxicity (ADCC) dapat meningkatkan respons klinis secara langsung
menginduksi destruksi tumor melalui presentasi antigen dan menginduksi respons sel T
tumor. Antibodi monoklonal berikatan dengan antigen permukaan sel tumor melalui Fc
reseptor permukaan sel NK. Hal ini memicu penglepasan perforin dan granzymes untuk
menghancurkan sel tumor (gambar 4.4a). Sel-sel yang hancur ditangkap antigen presenting
cell (APC) lalu dipresentasikan pada sel B sehingga memicu penglepasan antibodi kemudian
antibodi ini akan berikatan dengan target antigen (gambar 4.4b-d). Sel cytotoxic T
lymphocytes (CTLs) dapat mengenali dan membunuh sel target antigen (gambar 4.4d).
(Adams, G.P., et al., 2005)
Gambar 4.4. Skema mekanisme kerja Antibody Dependent Cellular Cytotoxicity (ADCC)

53
4.5.2 Complement dependent cytotoxicity (CDC)
Pengikatan antibodi monoklonal dengan antigen permukaan sel akan mengawali kaskade
komplement. Complement dependent cytotoxicity (CDC) merupakan suatu metode pembunuh
sel tumor yang lain dari antibodi. Imunoglobulin G1 dan G3 sangat efektif pada CDC melalui
jalur klasik aktivasi komplemen (gambar 4.5a). Formasi kompleks antigen antibodi
merupakan komplemen C1q berikatan dengan IgG sehingga memicu komplemen protein lain
untuk mengawali penglepasan proteolitik sel efektor kemotaktik/agen aktivasi C3a dan C5a
(gambar 4.5b). Kaskade komplemen ini diakhiri dengan formasi membrane attack
complex (MAC) (gambar 4.5c) sehingga terbentuk suatu lubang pada sel
membran. Membrane attack complex (MAC) memfasilitasi keluar masuknya air dan
Na+ yang akan menyababkan sel target lisis (gambar 4.5d). (Adams, G.P., et al., 2005)
Gambar 4.5. Skema mekanisme kerja Complement Dependent Cytotoxicity (CDC)
4.5.3 Perubahan transduksi signal
Reseptor growth factor merupakan suatu antigen target tumor, ekspresinya berlebihan pada
keganasan. Aktivasi transduksi signal pada kondisi normal akan menginduksi respons
mitogenik dan meningkatkan kelangsungan hidup sel, hal ini diikuti dengan ekspresi
perkembangan sel tumor yang berlebihan yang juga menyebabkan tumor tidak sentitif
terhadap zat kemoterapi. Antibodi monoklonal sangat potensial menormalkan laju
perkembangan sel dan membuat sel sensitif terhadap zat sitotoksik dengan menghilangkan
signal reseptor ini. Target antibodi EGFR merupakan inhibitor yang kuat untuk transduksi
signal. Terapi antibodi monoklonal memberikan efek penurunan densitas ekspresi target
antigen contohnya penurunan konsentrasi EGFR permukaan sel tumor atau membersihkan
ligan seperti VEGF. Pengikatan ligand reseptor growth factor memicu dimerisasi dan aktivasi
kaskade signal (gambar 4.6a) sehingga terjadi proliferasi sel dan hambatan terhadap zat

54
sitotoksik (gambar 4.6b). Antibodi monoklonal menghambat signal dengan cara menghambat
dimerisasi atau mengganggu ikatan ligand (gambar 4.6c). (Adams, G.P., et al., 2005)
Gambar 4.6. Skema mekanisme kerja pada transduksi sinyal
4.5.5 Imunomodulasi
Beberapa percobaan menunjukkan antibodi yang langsung melawan cytotoxic T lymphocyte
antigen 4 (CTLA 4) terbukti dapat menginduksi regresi imun. Pola toksisitas yang diteliti
pada uji klinis memperlihatkan hubungan perlekatan CTLA 4 dengan ligand dapat
menginduksi respons autoimun, hal ini terlihat pada aktivasi sel T dependent. Gabungan
antibodi anti-CTLA 4 dengan antibodi monoklonal menginduksi ADCC, kemoterapi
sitotoksik atau radioterapi sehingga dapat meningkatkan respons imun terhadap antigen
spesifik tumor. (Adams, G.P., et al., 2005)
4.5.5 Penghantaran muatan sitotoksik
Antibodi monoklonal pada terapi kanker akan melawan target sel tumor dengan cara
mengikat sel spesifik tumor dan menginduksi respons imun. Antibodi monoklonal telah
digunakan secara luas dalam percobaan sebagai zat sitotoksik sel-sel tumor. Modifikasi
antibodi monoklonal dilakukan dengan tujuan sebagai zat penghantar radioisotop, toksin
katalik, obat-obatan, sitokin, enzim atau zat konjugasi aktif lainnya. Pola antibodi bispesifik
pada kedua bagian Fab memungkinkan untuk mengikat target antigen dan sel efektor.
(Adams, G.P., et al., 2005)
4.5.6 Antibodi directed enzyme prodrug therapy (ADEPT)
Antibodi directed enzyme prodrug therapy (ADEPT) menggunakan antibodi monoklonal
sebagai penghantar untuk sampai ke sel tumor kemudian enzim mengaktifkan prodrug pada
tumor, hal ini dapat meningkatkan dosis active drug di dalam tumor. Konjugasi antibodi
monoklonal dan enzim mengikat antigen permukaan sel tumor (gambar 4.7a) kemudian zat
sitotoksik dalam bentuk inaktif prodrug akan mengikat konjugasi antibodi monoklonal dan

55
enzim permukaan sel tumor (gambar 4.7b-c) akhirnya inaktivasi prodrug terpecah dan
melepaskan active drug di dalam tumor (gambar 4.7d). (Adams, G.P., et al., 2005)
Gambar 4.7. Skema mekanisme kerja pada imunomodulasi
4.6 TARGET TERAPI
Terapi target didefinisikan sebagai obat atau molekul untuk membunuh sel tumor melalui
interaksi target yang terdapat pada sel ganas. Terapi target ditujukan bagaimana secara
selektif melawan molekul pada permukaan sel dan jalur signal metabolik sel ganas. Terapi
target secara potensial dapat memisahkan sel normal selanjutnya mengurangi toksisiti dan
memperbaiki kualiti hidup. Jenis terapi target tergantung cara kerja dan target spesifik,
bermacam zat yang dapat diklasifikasikan ke dalam subkategori yaitu antibodi monoklonal,
inhibitor tyrosine kinase, inhibitor proteosome, inhibitor cyclin dependent kinase (CKD),
inhibitor Raf kinase, angiogenic agents, inhibitormatrix metalloproteinase, inhibitor
farnesyltransferase, inhibitor deacetylase, inhibitor cox-2, teknologi antisense dan terapi
gen. Terapi target pada KPKBSK yang digunakan adalah inhibitor EGFR antibodi
monoklonal ″Trastuzumab″ (Herceptin), ″Cetuximab″ (Erbitux), inhibitor EGFR tyrosine
kinase ″Gefitinib″ (Irresa), inhibitor angiogenesismetalloproteinase, inhibitor VEGF antibodi
monoklonal ″Bevacizumab″ (Avastin) dan inhibisi tranduksi signal antisense oligonucleotide
protein kinase C alpha. (Herbst, R.S., 2002; Herbst, R.S., 2003)
Epidermal Growth Factor Receptor (EGFR) dan Tyrosine Kinase (TK)
Reseptor growth factor sangat penting untuk mengatur proses seluler tumor seperti
proliferasi, differensiasi, pertahanan, angiogenesis dan migrasi. Reseptor growth factor terdiri
dari HER-1 (epidermal growth factor [EGFR] atau c-erb B1), HER-2 (c-erb B-2), HER3 (c-
erb B-3) dan HER4 (c-erb B4). Epidermal growth factor receptor (EGFR)/HER 1 melekat
pada bagian ekstraseluler (EGF, transforming growth factor α (TGF-α) dan growth

56
factor lainnya), bagian transmembran dan bagian tyrosine kinase intraseluler. (Herbst, R.S.,
2003)
Epidermal growth factor receptor EGFR berikatan dengan ligand menyebabkan
homodimerisasi atau heterodimerisasi reseptor HER famili yang lain dan
mengaktifkantyrosine kinase (TK). Fosforilasi reseptor tyrosine menerima signal protein
intraseluler dan mengubah signal ekstraseluler menjadi transduksi signal intraseluler.
Molekul efektoradapter seperti growth factor reseptor bound protein 2 (Grb2) dan Src
homology collagen protein (Shc) berperan sebagai dasar untuk merangkai elemen signal yang
dibutuhkan untuk aktivasi proliferasi seluler. Molekul enzim lainnya yang mengaktifkan
EGFR TK fosforilasi adalah son of sevenless (SOS), phosphatidyl inositol 3 kinase (PI3K)
dan Grb2-associated binder 1 (Gab 1). (Herbst, R.S., 2003)
Jalur transduksi signal multipel diawali fosforilasi EGFR termasuk kaskade signal Ras
(oncogen) - mitogen activated protein kinase (MAPK). Scr dan jalur signal tranducers and
activator of transcription (STAT) secara luas digunakan sebagai signal growth untuk
menginduksi gen trankripsi dan menimbulkan berbagai macam respons sel. Proliferasi seluler
hasil aktivasi EGFR TK terjadi melalui beberapa jalur transduksi signal. Signal proliferasi
jalur MAPK terjadi setelah molekul adapter mengaktivasi kompleks EGFR timbul langkah
aktivasi dari Ras, Raf , MAP / Erk kinase (MEK1) dan extracellular regulated kinase (Erk)
protein yang akan meningkatkan aktiviti faktor transkripsi untuk proliferasi dan aktivasi
progresi siklus sel. (Herbst, R.S., 2003)
Aktivasi EGFR TK mempengaruhi progresi tumor soliter. Transforming growth
factor α (TGFα) dan EGF menginduksi angiogenesis serta permeabiliti sel vaskuler dengan
meningkatkan ekspresi VEGF tumor. Peningkatan ekspresi VEGF tumor akan menghasilkan
ketidakseimbangan antara faktor pro dan antiangiogenik di dalam tumor yang akhirnya
menimbulkan vaskularisasi dan pertumbuhan baru. Peningkatan densiti mikrovaskuler
merupakan suatu peningkatan aktivasi EGFR TK. Epidermal growth factor receptor tyrosine
kinase (EGFR TK) juga berinteraksi dengan jalur komponen yang mempengaruhi sel - sel
adhesi, hal ini penting untuk invasi tumor sel ke jaringan yang berdekatan. Epidermal growth
factor receptor tyrosine kinase (EGFR TK) juga mengaktivasi matrix metalloproteinase dan
stimulasi motiliti sel tumor yang akhirnya menambah metastasis. Aktivasi EGFR TK secara
tidak langsung menghambat apoptosis sel tumor, meningkatkan tahan hidup sel tumor dan
resisten terhadap terapi sitotosik. Aktiviti ini disebabkan oleh PI3K suatu signal molekul
penting jalur antiapoptotik yang mempengaruhi faktor transkripsi nuclear factor κB (NF κB)

57
dan juga mengatur jalur aktiviti Ras MAPK pada proliferasi seluler (gambar 4.8). (Herbst,
R.S., 2003)
Ekspresi EGFR meningkat pada keganasan dan ditemukan 40-80% pada KPKBSK.
Ekspresi EGFR secara histologis sering meningkat pada squamous cell carcinoma,large cell
carcinoma dan sedikit meningkat pada small cell carcinoma. Titer EGFR meningkat pada
KPKBSK stage IV dibandingkan stage I, II dan juga meningkat pada kasus yang berkaitan
dengan mediastinal. Ekspresi EGFR sangat penting dalam perkembangan dan progresi
keganasan, beberapa penelitian didapatkan korelasi positif antara ekspresi EGFR yang
berlebihan, invasi tumor dan rendahnya lama tahan hidup. (Herbst, R.S., 2003)
Gambar 4.8. Skema aktivitas jarus RAS-MAPK pada proliferasi seluler
4.6 HAMBATAN DALAM TERAPI
Distribusi antigen sel ganas sangat heterogen sehingga beberapa sel dapat mengenali antigen
tumor dan sel lainnya tidak. Densitas antigen bervariasi bila rendah antibodi monoklonal
tidak efektif. Aliran darah tumor tidak selalu optimal bila antibodi monoklonal dihantarkan
melalui darah maka sulit untuk mengandalkan terapi ini. Tekanan interstisial yang tinggi
dalam tumor dapat mencegah ikatan dengan antibodi monoklonal. Antigen tumor selalu
dilepaskan sehingga antibodi mengikat antigen bebas dan bukan sel tumor. Antibodi

58
monoklonal diperoleh dari sel tikus kemungkinan masih ada respons imun antibodinya yang
disebut respons human anti mouse antibodies (HAMA). Respons ini tidak hanya menurunkan
kemanjuran terapi antibodi monoklonal tapi juga menyisihkan kemungkinan terapi ulangan.
Reaksi silang antibodi monoklonal dengan antigen jaringan normal jarang sehingga aplikasi
antibodi monoklonal memberikan hasil yang baik pada keganasan hematologi dan tumor
soliter walaupun terdapat beberapa rintangan. (VonMehren, M., 2003)
4.7 BEBERAPA CONTOH PRODUK DI PASARAN
Transtuzumab
″Trastuzumab″ (Herceptin) merupakan suatu antibodi monoklonal humanized yang
menghambat sel pertumbuhan dengan cara mengikat bagian ekstraseluler reseptor
HER2 protein tyrosine kinase. ″Trastuzumab″ juga menginduksi ADCC melalui sel NK dan
monosit untuk melawan sel ganas. ″Trastuzumab″ mempunyai efek samping berupa disfungsi
jantung (27% pada terapi kombinasi dan 8% terapi tunggal), mielosupresi dan diare. Ekspresi
protein HER2 yang berlebihan ditemukan pada jaringan tumor KPKBSK dengan
menggunakan teknik immunohistochemistry (IHC) 20%, fluorescence in situ hybridization
(FISH) 6% dan kadar serum HER2 > 15 ng/ml pada ELISA 6%. Immunohistochemistry
(IHC) didapatkan 66 spesimen memberikan hasil positif dan ELISA didapatkan 13 spesimen
positif tetapi tidak satupun spesimen positif pada FISH. (Segota, E., et al., 2004; Heinmoller,
P., et al., 2003)
Kombinasi ″trastazumab″ dan kemoterapi memberikan hasil lebih baik growth
inhibitor pada sel yang mengekspresi HER2. Kombinasi ″trastuzumab″ dengan kemoterapi
terbukti secara klinis memberikan keuntungan pasien kanker payudara metastasis HER2
positif. Penelitian uji klinis randomisasi fase II efek penambahan kombinasi ″trastazumab″
dengan kemoterapi standar (gemcitabine dan cisplatin) pada pasien KPKBSK HER2 positif
memberikan hasil toleransi yang baik secara klinis. Kombinasi paclitaxel, carboplatin dan
″trastuzumab″ dapat diberikan pada KPKBSK stage lanjut dengan toksisiti yang tidak lebih
buruk dibandingkan dengan terapi tanpa ″trastuzumab″. Strategi yang paling menjanjikan
dari target HER2 adalah penggunaan kombinasi inhibitor EGRF TK dengan inhibitor
HER2 dimerization. (Bunn, P.A., et al., 2001; Vogel, C.L., et al., 2002; Lanjer, C.J., et al.,
2004)

59
Cetuximab
″Cetuximab″ (Erbitux) merupakan antibodi monoklonal chimeric yang bekerja
mengikat EGFR pada bagian ekstraseluler. ″Cetuximab″ memberikan efek samping ruam
acneiform, folikulitis pada wajah dan dada serta dilaporkan juga reaksi hipersensitif.
Response rate (RR) lebih tinggi bila terjadi ruam pada kulit. Penelitian fase II monoterapi
″cetuximab″ pasien KPKBSK rekuren dan metastasis yang dideteksi EGFRnya dan yang
telah diberikan satu atau lebih regimen kemoterapi sebelumnya, didapatkan 2 dari 29
(6,9%) parsial respons (PR) dan 5 pasien (17,2%) penyakitnya stabil. Uji klinis fase II pasien
KPKBSK stage IIIB/IV rekuren atau metastasis didapatkan respons, 3,3% PR (2/60 pasien)
dan 25% penyakitnya stabil (15/60 pasien). Hal ini menunjukkan toleransi ″cetuximab″
sangat baik. (Lynch, T.J., et al., 2004; Theinelt, C.D., et al., 2005)
Efikasi ″cituximab″ ditambah kemoterapi lainnya telah diteliti. Penelitian fase I pada
KPKBSK didapatkan PR 2 dari 19 pasien (10,5%) dengan dosis multipel ″cetuximab″ dan
cisplatin. Uji klinis randomisasi terkontrol kemoterapi naive pasien KPKBSK stadium lanjut
dengan ekspresi EGFR berlebihan didapatkan RR yang tinggi pada regimen ″cetuximab″,
vinorelbine dan cisplatin dibandingkan hanya dengan ″vinorelbine″ dan ″cisplatin″ saja
(31,7% vs 20,0%). Penelitian lain kombinasi ″cetuximab″ dilaporkan bahwa didapatkan RR
yang hampir sama. Kombinasi ″cetuximab″ dengan docetaxel kemoterapi pada KPKBSK
refrakter/resisten didapatkan 28% (13/47) PR dan 17% (8/47) penyakitnya stabil.
″Cetuximab″ yang ditambahkan regimen paclitaxel + carboplatin atau regimen gemcitabine +
carboplatine pada KPKBSK naïve didapatkan masing – masing RR 26% (31 pasien) dan
28,6% (35 pasien). (Lynch, T.J., et al., 2004; Theinelt, C.D., et al., 2005)
Bevacizumab
″Bevacizumab″ (Avastin) merupakan antibodi monoklonal humanized yang bekerja
pada target VEGF, menstimulasi formasi pembuluh darah baru tumor. ″Bevacizumab″
mempunyai efek samping berupa hipertensi sedang dan efek yang jarang terjadi adalah
perforasi intestinal. Beberapa inhibitor angiogenesis telah diteliti pada KPKBSK termasuk
VEGF, VEGFR antibodi dan inhibitor VEGFR TK. Penelitian terbaik inhibitor angiogenesis
adalah ″bevacizumab″ suatu antiVEGF antibodi yang dikombinasikan dengan kemoterapi
dan ″erlotinib″ pada KPKBSK stage lanjut atau rekuren. Uji klinis randomisasi terkontrol 99
pasien KPKBSK stage IIIB/IV atau rekuren, ″bevacizumab″ ditambahkan pada paclitaxel +
carboplatin memberikan respons dan time to progression (TTP) yang baik dibandingkan
dengan paclitaxel + carboplatin saja. Median TTP jauh lebih bermakna pada pasien yang

60
mendapatkan regimen ″bevacizumab″ dosis tinggi (15mg/kg) daripada yang mendapatkan
dosis kecil (7,5mg/kg) (7,4 vs 4,2 bulan p=0,023). Tidak ada perbedaan yang bermakna pada
TTP pada grup ″bevacizumab″ dosis rendah dibandingkan paclitaxel + carboplatin saja.
(Johnson, D.S., et al., 2005)
Hasil awal uji klinis fase I/II ″bevacizumab″ dan ″erlotinib″ pada KPKBSK stage
IIB/IV atau rekuren didapatkan PR 8 dari 40 pasien (20%) dan penyakit stabil 26 dari 40
pasien (65%), median survival time 12,6 bulan dan progression free survival 6,2 bulan.
Eastern Cooperative Oncology Group (ECOG) E4599 trial membandingkan regimen
paclitaxel + carboplatin dengan ″bevacizumab″ (PCB) dan tanpa ″bevacizumab″ (PC) pada
KPKBSK stage lanjut. Hal ini merupakan uji klinis fase III pertama yang menunjukkan
keuntungan survival terapi lini pertama kombinasi target biologi dengan kemoterapi,
dilaporkan RR 27% pada PCB dibandingkan 10% pada PC, progression free survival (PFS)
(6,4 vs 4,5 bulan) dan median survival rates (12,5 vs 10,3 bulan) dengan ″bevacizumab″.
″Bevacizumab″ memberikan toleransi yang baik bila dikombinasi dengan regimen paclitaxel
+ carboplatin yang akan mengubah toksisiti regimen kemoterapi. ″Bevacizumab″ mempunyai
efek samping hipertensi, proteinuria dan hemoragik. Kasus hemoragik sangat kecil tetapi
dilaporkan terjadi hemoragik pulmoner yang merupakan sebab hambatan angiogenesis.
Hilangnya neovessel dalam jumlah besar pada sentral tumor menyebabkan perdarahan ke
dalam kaviti tumor yang nekrosis. (Johnson, D.S., et al., 2005)
4.8 REFERENSI
1. Kőhler, G. dan Milstein, C. (1975). Continous cultures of fused cells secreting antibody of
predifined specificity. Nature. 256: 495-7.
2. Waldmann, T.A. (2003). Immunotherapy: past, present and future. Nature Medicine. 9: 269-77.
3. VonMehren, M., Adams, G.P., Weiner, L.M. (2003). Monoclonal antibody therapy for cancer.
Annu Rev Med. 54: 343-69.
4. Adams, G.P., dan Weiner, L.M. (2005). Monoclonal antibody therapy of cancer. Nature
Biotechnology. 23: 1147-57.
5. Jusuf, A., Harryanto, A., Syahruddin, E., Endardjo. S., Mudjiantoro, S., Sutandio, N. (2005).
Kanker paru jenis karsinoma bukan sel kecil pedoman diagnosis dan penatalaksanaan di
Indonesia. (Jusuf A, Syahruddin E, penyunting). Jakarta: PDPI. 14-5.
6. Alberts, B., Johnson, A., Lewis, J., Raff, M., Robert, K., Walter, P. (2002). Manipulating
proteins, DNA, and RNA. In: Anderson MS, Dilernia B, editors. Molecular biology of the cell.
4th ed.New York: Garland Science. 469-78.
7. Abbas AK, Lichtman AH. Antibodies and antigens. In: Schmitt WR, Krehling H, editors.
(2005). Cellular and molecular immunology. 5th ed. Philadelphia: Elsevier Saunders. 43-64.
8. Nelson PN, Reynolds GM, Waldron EE, Ward E, Giannopoulos K, Murray PG. (2000).

61
Demystified monoclonal antibodies. J Clin Pathol: Mol Pathol. 53: 111-7.
9. Research in focus monoclonal antibodies. Available from:
URL: http://www.mrc.ac.uk/pdf_mon_antibodies.pdf.
10. Monoclonal antibodies. Available from:
URL: http://en.wikipedia.org/wiki/Monoclonal_antibodies.
11. Monoclonal antibodies. Available from:
URL: http://users.rcn.com/BiologyPages/Monoclonal.html.
12. Tuscano JM, Noonan K, Mulrooney T. (2005).Monoclonal antibodies: case studies in novel
therapies. In: Frankel C, editor. A continuing education program for oncology
nurses.Pittsburgh: OES. 5-8.
13. Ward PA, Adams J, Faustman D, Gebhart GF, Geistfeld JG, Imbaratto JW, et al. (1999).
Monoclonal antibody production. In: Grossblatt N, editor. A report of the commitee on methods
of producing monoclonal antibodies institute for laboratory animal research national research
council. Washington DC: National Academy Press. 6-8.
14. Immunotherapy for cancer. Monoclonal antibodies. Available from:
URL: http://www.meds.com/immunotherapy.
15. American Cancer Society. (2005). Cancer facts & figures 2005. Atlanta: ACS.
16. Syahruddin E. (2006). Characteristic of patients in Indonesian association for the study of lung
cancer data. In: Committee PIPKRA, editors. Abstracts of the 4th Scientific Respiratory
Medicine Meeting. Jakarta PIPKRA. 51.
17. Jemal A, Murray T, Ward E, Samuels A, Tiwari RC, Ghafoor A, et al. (2005). Cancer statistic
2005. CA Cancer J Clin. 55: 10-30.
18. Isobe T, Herbst RS, Onn A. (2005). Current management of advanced non small cell lung
cancer: targeted therapy. Semin Oncol. 32: 315-28.
19. Ostoros G, Kovacs G, Szondy K, Dome B. (2005). New therapies for non-small cell lung
cancer. Orv Hetil. 146: 1135-41.
20. Herbst RS. (2002). Targeted therapy in non small cell lung cancer. Oncology (Williston Park).
16: 19-24.
21. Maione P, Rossi A, Airoma G, Ferrara C, Castaldo V. (2004). The role of targeted therapy in
non small cell lung cancer. Crit Rev Oncol Hematol. 51: 29-44.
22. Mishra BK, Parikh PM. (2006). Targeted therapy in oncology. MJAFI. 62: 169-73.
23. Herbst RS, Bunn PA. (2003). Targeting the epidermal growth factor receptor in non small cell
lung cancer. Clin Cancer Res. 9: 5813-24.
24. Herbst RS, Shin DM. (2002). Monoclonal antibodies to target epidermal growth factor receptor
positive tumors: a new paradigm for cancer therapy. Cancer. 94: 1593-611.
25. Ettinger DS. (2006). Clinical implications of EGFR expression in the development and
progression of solid tumors: focus on non small cell lung cancer. The oncologist. 11: 358-73.
26. Segota E, Bukowski RM. (2004). The promise of targeted therapy: cancer drugs become more
specific. Cleveland Clin J Med. 71: 551-60.
27. Heinmőller P, Gross C, Beyser K, Schmidtgen C, Maass G, Pedrocchi M, et al. HER 2 status in
non small cell lung cancer: result from patient screening for enrollment to a phase II study of
herceptin. Clin Cancer Res 2003; 9: 5238-44.
28. Bunn PA, Helfrich B, Soriano AF, Franklin WA, Garcia MV, Hirsch FR, et al. (2001).
Expression of HER 2/neu in human lung cancer cell lines by immunohistochemistry and
fluorescence in situ hybridization and its relationship to in vitro cytotoxicity by trastuzumab
and chemotherapeutic agents. Clin Cancer Res. 7: 3239-50.
29. Vogel CL, Cobleigh MA, Tripathy D, Gutheil JC, Harris LN, Fehrenbacher L, et al. (2002).

62
Efficacy and safety of trastuzumab as a single agent in first line treatment of HER 2
overexpressing metastatic breast cancer. J Clin Oncol. 20: 719-26.
30. Gatzemeier U, Groth G, Butts C, Zandwijk NV, Shepherd F, Ardizzoni A, et al. Randomized
phase II trial of gemcitabine-cisplatin with or without trastuzumab in HER 2 positive non small
cell lung cancer. Annals of oncology 2004; 15: 19-27.
31. Lanjer CJ, Stephenson P, Thor A, Vangel M, Johnson DH. (2004). Trastuzumab in the
treatment of advanced non small cell lung cancer: is there a role? focus on eastern cooperative
oncology group study 2598. J Clin Oncol. 22: 1180-7.
32. Swanton C, Futreal A, Eisen T. (2006). Her2 targeted therapies in non small cell lung cancer:
novel agents in the treatment of lung cancer: advances in EGFR targeted agents. Clin Cancer
Res. 12: 4377-83.
33. Lynch TJ, Lilenbaum R, Bonomi P Ansari R, Govindan R, Janne PA, et al. (2004). A phase II
trial of cetuximab as therapy for recurrent non small cell lung cancer (NSCLC). Proc Am Soc
Clin Oncol. 22: abst 7084.
34. Rosell R, Daniel C, Ramlau R, Szczesna A, Constenla M, Mennecier B, et al. (2004).
Randomized phase II study of cetuximab in combination with cisplatin (C) and vinorelbine (V)
vs CV alone in the first line treatment of patients (pts) with epidermal growth factor receptor
(EGFR) expressing advanced non small cell lung cancer (NSCLC). Proc Am Soc Clin Oncol.
22: abstr 7012.
35. Thienelt CD, Bunn PA, Hanna N, Rosenberg A, Needle MN, Long ME, et al. (2005).
Multicenter phase I/II study of cituximab with paclitaxel and carboplatin in untreated patients
with stage IV non small cell lung cancer. J Clin Oncol. 23: 8786-93.
36. Robert F, Blumenschein G, Herbst RS, Fossella FV, Tseng J, Saleh MN. (2005). Phase I/IIa
study of cetuximab with gemcitabine plus carboplatin in patients with chemotherapy naïve
advanced non small cell lung cancer. J Clin Oncol. 23: 9089-96.
37. Sandler AB, Johnson DH, Herbst RS. (2004). Anti vascular endothelial growth factor
monoclonals in non small cell lung cancer. Clin Cancer Res. 10: 4258-62.
38. Johnson DH, Fehrenbacher L, Novotny WF, Herbst RS, Nemunatis JJ, Joblons DM, et al.
(2004). Randomized phase II trial comparing bevacizumab plus carboplatin and paclitaxel with
carboplatin and paclitaxel alone in previously untreated locally advanced or metasatic non small
cell lung cancer. J Clin Oncol. 22: 2184-91.
39. Herbst RS, Johnson DH, Mininberg E, Carbone DP, Henderson T, Kim ES, et al. (2005). Phase
I/II trial evaluating the anti vascular endothelial growth factor monoclonal antibody
bevacizumab in combination with HER1/epidermal growth factor receptor tyrosine kinase
inhibitor erlotinib for patient with recurrent non small cell lung cancer. J Clin Oncol. 23: 2544-
55.
40. Fundamentally transforming the way cancer is treated. Avialable from:
URL: http://www.biooncology.com/bioonc/approach/index.m