TRANSPORTE ELECTRONICO Y FOSFORILACION OXIDATIVA · 2013. 11. 5. · transporte electrónico unidas...
Transcript of TRANSPORTE ELECTRONICO Y FOSFORILACION OXIDATIVA · 2013. 11. 5. · transporte electrónico unidas...
-
TRANSPORTE ELECTRONICO
Y FOSFORILACION OXIDATIVA
-
1.- CADENA TRANSPORTADORA DE ELECTRONES
• La glucólisis y el ciclo del ácido cítrico generan
una cantidad relativamente baja de energía en
forma de ATP.
• Sin embargo se tiene que en la glucólisis, en la
reacción de la piruvato deshidrogenasa y en el
ciclo del ácido cítrico ocurren seis pasos de
deshidrogenación reduciendo 10 moles de
NAD+ a NADH y 2 moles de FAD a FADH2 por
mol de glucosa.
-
• NADH y FADH2, se reoxidan mediante las proteínas de
transporte electrónico unidas a la membrana
mitocondrial interna.
• Estas proteínas se ensamblan en cinco complejos
multiproteicos, denominados I, II, III, IV y V.
• Los complejos I, II, III y IV aceptan electrones desde un
transportador electrónico relativamente móvil y pasan
los electrones a otro transportador móvil.
• La energía liberada por las acciones de los complejos I,
III y IV impulsa la síntesis de ATP por el complejo V.
-
Complejo I
• El NADH se oxida en el primer paso del
transporte electrónico por el complejo I, o NADH
deshidrogenasa.
-
• Este complejo contiene el mononucleótido de
flavina (FMN) como grupo complementario
estrechamente unido.
• También tiene algunos centros hierro-azufre,
que transfieren los electrones desde la flavina
reducida a otro transportador respiratorio, la
coenzima Q.
-
Complejo II
• El complejo II, también llamado succinatodeshidrogenasa, recibe electrones de laoxidación del succinato.
-
• Al igual que la NADH deshidrogenasa, la
succinato deshidrogenasa transfiere los
electrones a través de los centros hierro-azufre
a la coenzima Q.
-
Coenzima Q
• La coenzima Q (CoQ) también llamada
ubiquinona, lleva electrones hacia la cadena
respiratoria, no sólo desde el NADH sino
también desde el succinato y desde
intermediarios de la oxidación de los ácidos
grasos.
• Este transportador electrónico lipídico, se
desplaza libremente a través de la membrana.
-
Complejo III
• El complejo III, también llamado citocromo creductasa, oxida la forma reducida de la
coenzima Q y reduce a su vez el citocromo c.
-
Citocromo c
• Los citocromos son un grupo de hemoproteínasrojas o pardas que tienen unos espectros de luzvisible característicos.
• Los principales citocromos respiratorios se clasificancomo b, c o a, según las longitudes de onda de losmáximos de absorción espectral.
• Los citocromos experimentan una oxidorreducción através del metal que forma el complejo en ellos, yque pasa por ciclos de estados +2 y +3 del hierrohemo y de estados +1 y +2 del cobre en loscitocromos a y a3 .
• Así pues, los citocromos son transportadores de unelectrón.
-
Complejo IV
• El complejo IV, también llamado citocromo c
oxidasa, acopla la oxidación del citocromo c con
la reducción del O2 a agua.
-
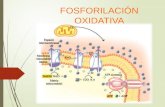
2.- FOSFORILACION OXIDATIVA
• El modelo denominado acoplamiento
quimiosmótico explica el mecanismo mediante
el cual la energía liberada en la respiración se
utiliza para impulsar la síntesis de ATP.
• Este modelo propone que la energía del
transporte electrónico impulsa un sistema de
transporte activo, que de alguna forma bombea
protones fuera de la matriz mitocondrial al
espacio intermembrana.
-
• Los protones del exterior tienen tendencia
termodinámica a volver a pasar al interior, para
igualar el pH a ambos lados de la membrana.
• Cuando los protones vuelven a entrar en la
matriz, esa energía se gasta, y parte de ella se
utiliza para impulsar la síntesis de ATP.
-
• La energía liberada por la descarga de este gradientepuede acoplarse con la fosforilación de ADP a ATP.
• En este proceso interviene el complejo Fo F1 (complejoV también llamado ATP sintasa).
• La porción Fo del complejo se extiende a través de lamembrana interna y se cree que contiene un canalespecífico para la vuelta de los protones a la matrizmitocondrial.
• La energía libre que se libera cuando el H+ pasa poreste canal para regresar a la matriz se aprovecha dealguna manera para impulsar la síntesis de ATP,catalizada por el componente F1 del complejo
-
NADH 3 ATP
FADH2 2 ATP
•Glicolisis = 2 NADH
•Piruv desh. = 2 NADH
•Ciclo Krebs = 6 NADH
2 FADH2
-
• Rendimiento energético
-
Lanzaderas
• En NADH generado en la glucólisis debe
transferir los equivalentes reductores a la
mitocondria, para su reoxidación por la cadena
respiratoria.
• En este proceso se debe reducir un sustrato por
el NADH en el citoplasma, luego este sustrato
reducido pasa a la matriz mitocondrial a través
de un transporte específico.
• A continuación el sustrato se reoxida en el
interior de la matriz y pasa de vuelta al
citoplasma.
-
1.- Lanzadera dihidroxiacetona fosfato/glicerol-3-
fosfato.
Cerebro
-
2.- Lanzadera malato/aspartato
Hígado y corazón.
-
INHIBIDORES
Rotenona
Amital
Antimicina A•Cianuro
•CO
•Azida de
sodio
-
• Rotenona: insecticida que bloquea el flujo
electrónico desde el NADH a la coenzima Q
• Amital: fármaco que actúa de la misma forma
que la rotenona.
• Antimicina A: antibiotico que bloquea el flujo
electrónico desde el citocromo b al c1
• Cianuro, azida y monóxido de carbono: son
inhibidores de la citocromo oxidasa