Sintesis Senyawa Calkon
-
Upload
kharisma-candra-sari -
Category
Documents
-
view
359 -
download
32
Transcript of Sintesis Senyawa Calkon

i
SINTESIS SENYAWA ANALOG BISCALKON SERTA UJI
AKTIVITASNYA SEBAGAI ANTIBAKTERI
SKRIPSI
KHARISMA CANDRA SARI
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS AIRLANGGA
2011

ii
SINTESIS SENYAWA ANALAOG BISCALKON SERTA UJI
AKTIVITASNYA SEBAGAI ANTIBAKTERI
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh
Gelar Sarjana Sains Bidang Kimia pada
Fakultas Sains dan Teknologi
Universitas Airlangga
Disetujui oleh:
Pembimbing I,
Drs. Hery Suwito, M.Si
NIP. 19630308 198701 1 001
Pembimbing II,
Dr. Alfinda Novi K., DEA
NIP. 19671115 199102 2 001

iii
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : Sintesis Senyawa Analog Biscalkon serta Uji
Aktivitasnya sebagai Antibakteri
Penyusun : Kharisma Candra Sari
NIM : 080710136
Tanggal Ujian : 27 Juli 2011
Disetujui Oleh
Mengetahui,
Ketua Program Studi Kimia
FSAINTEK Universitas Airlangga
Dr. Alfinda Novi Kristanti, DEA
NIP. 19671115 199102 2 001
Pembimbing I,
Drs. Hery Suwito, M.Si
NIP. 19630308 198701 1 001
Pembimbing II,
Dr. Alfinda Novi K., DEA
NIP. 19671115 199102 2 001

iv
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam
lingkungan Universitas Airlangga. Diperkenankan untuk dipakai sebagai referensi
kepustakaan, tetapi pengutipan harus seizin penyusun dan harus menyebutkan
sumbernya sesuai kebiasaan ilmiah. Dokumen skripsi ini merupakan hak milik
Universitas Airlangga.

v
KATA PENGANTAR
Penulis ingin mengucapkan puji syukur kepada Allah SWT dengan segala
kerendahan hati, sebab dengan segala rahmat-Nya, penulis mampu
menyelesaikan skripsi ini yang berjudul “Sintesis Senyawa Analog Biscalkon
serta Uji Aktivitasnya sebagai Antibakteri”.
Tak lupa penulis juga ingin mengucapkan terima kasih yang tulus kepada :
1. Bapak Drs. Hery Suwito, M.Si sebagai dosen pembimbing I dan Ibu Dr.
Alfinda Novi Kristanti, DEA sebagai dosen pembimbing II yang telah
memberikan bimbingan, saran, serta masukan dengan penuh kesabaran
hingga skripsi ini dapat terselesaikan
2. Ibu Dr. Muji Harsini sebagai dosen wali yang telah memberikan saran dan
bimbingan selama masa perkuliahan
3. Bapak Drs. Mulyadi Tanjung, MS dan Ibu Dr. Pratiwi Pudjiastuti, M.Si
yang telah memberikan bantuan dalam pengukuran serta intepretasi
spektra NMR dan MS
4. Seluruh dosen Departemen Kimia Fakultas Sains dan Teknologi
Universitas Airlangga yang telah memberikan ilmu baik akademik
maupun nonakademik yang sangat berharga
5. Dosen-dosen Departemen Biologi Fakultas Sains dan Teknologi
Universitas Airlangga khususnya Ibu Jun, Ibu Ni’mah, dan Ibu Fat yang
telah memberikan waktu, bimbingan, serta saran dengan penuh kesabaran

vi
6. Mama dan Papa tercinta, adik tersayang (Kharisma Candra Sasi), serta
seluruh keluarga besar yang telah memberikan doa dan dukungan yang
tulus baik secara moral dan materi selama ini
7. Seluruh teman-teman Kimia 2007, khususnya Sugarplum (Amalia, Eka,
Intan, Rulina), kelompok sintesis (Nina, Dika, Susdian), serta teman-teman
kelompok skripsi Organik dan Biokimia atas semangat, kerjasama dan
dukungan selama ini, terima kasih atas kebersamaan selama empat tahun
yang menjadikan segalanya indah dan bermakna
8. Segenap warga Kimia, kakak & adik angkatan, karyawan (khususnya Pak
Damam, Pak Kamto, Mbak Yuli, Mas Fendi) atas bantuannya secara
langsung maupun tidak langsung dalam penyelesaian skripsi ini
9. Orang-orang yang selalu ada dan memberikan semangat serta harapan
Penulis sangat mengharapkan skripsi ini mampu memberikan informasi
mengenai perkembangan ilmu sintesis organik dan kimia bahan alam. Penulis
menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Maka dari itu kami
terbuka dengan berbagai kritik dan saran agar menjadi lebih baik. Untuk segala
kekurangan dan kesalahan, penulis mohon maaf yang sebesar-besarnya.
Surabaya, 11 Juli 2011
Penyusun,
Kharisma Candra Sari

vii
Sari, Kharisma Candra, 2011, Sintesis Senyawa Analog Bis-Calkon serta Uji
Aktivitasnya sebagai Antibakteri, skripsi ini dibawah bimbingan Drs. Hery
Suwito, M.Si dan Dr. Alfinda Novi Kristanti, DEA, Departemen Kimia
Fakultas Sains dan Teknologi Universitas Airlangga
ABSTRAK
Penelitian ini bertujuan untuk mensintesis senyawa analog biscalkon melalui
reaksi kondensasi aldol dengan katalis basa dari bahan dasar vanilin dan N-metil-
piperidin-4-on, serta untuk mengetahui aktivitasnya sebagai antibakteri. Vanilin
yang digunakan diperoleh adalah vanilin pasaran yang direkristalisasi. Hasil KLT
menunjukkan bahwa senyawa hasil sintesis masih mengandung vanilin dan hasil
spektroskopi masa menunjukkan berat molekul yang tidak sesuai dengan senyawa
target yang diinginkan. Hal ini menunjukkan bahwa sulit untuk memperoleh
senyawa target yang diinginkan. Oleh karena itu, melalui metode sintesis yang
sama dengan sebelumnya, bahan dasar vanilin diganti dengan 2,5-
dimetoksibenzaldehid. Identifikasi senyawa tersebut dilakukan dengan metode
spektroskopi, meliputi uji UV-VIS, IR, 1H-RMI,
13C-RMI, dan MS. Senyawa
hasil sintesis adalah 3,5-bis-(2,5-dimetoksi benzilidin)-N-metil piperidin-4-on. Uji
antibakteri dilakukan terhadap bakteri Staphylococcus aureus dan Escherichia
coli dengan metode difusi cakram. Dari diameter zona hambat dapat diketahui
bahwa senyawa target memiliki aktivitas sebagai antibakteri.
Kata kunci : vanilin, antibakteri, Staphylococcus aureus, Escherichia coli

viii
Sari, Kharisma Candra 2011, Synthesis Bis-Chalcone Analogue Compound
and The Bioactivity as Antibacterial Agent, This Research is Under
Guidance of Drs. Hery Suwito, M.Si and Dr. Alfinda Novi Kristanti, DEA,
Department of Chemistry, Science and Technology Faculty, Universitas
Airlangga.
ABSTRACT
The purpose of this research are to syntesize a bis-chalcone analogue by using
aldol condensation with a base catalyst from vanillin and N-methyl-piperidin-4-
on, as well as to determine the antibacterial activity. The vanillin was obtained
from recrystallized vanillin. The separation using thin layer chromatograhphy
(TLC) showed that the target molecule still consist of vanillin and based on the
result of mass spectroscopic indicates that the molecular weight was not
correspond to the target molecule. Therefore, through the same synthesis method
as before, vanillin as starting material was substituted with 2-5-
dimethoxybenzaldehyde. The new target molecule is 3,5-bis-(2,5-dimethoxy
benzilidin)-1-methyl piperidin-4-one. The structure of the target molecule was
identified using spectroscopy methods, such as UV-VIS, IR, NMR, and MS. The
antibacterial activity of the target molecule conducted on Staphylococcus aureus
and Escherichia coli by disc diffusion method. Inhibitory zone showed that the
compounds have activity as an antibacterial agent.
Keywords : vanillin, antibacterial, Staphylococcus aureus, Escherichia coli

ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ............................................................................................ i
LEMBAR PERNYATAAN ................................................................................. ii
LEMBAR PENGESAHAN ................................................................................. iii
LEMBAR PEDOMAN PENGGUNAAN SKRIPSI ............................................ iv
KATA PENGANTAR .......................................................................................... v
ABSTRAK ........................................................................................................... vii
DAFTAR ISI ........................................................................................................ ix
DAFTAR TABEL ................................................................................................ xi
DAFTAR GAMBAR ........................................................................................... xii
DAFTAR LAMPIRAN ........................................................................................ xiii
BAB I PENDAHULUAN ..................................................................................... 1
1.1 Latar Belakang Masalah ................................................................... 1
1.2 Rumusan Masalah ............................................................................. 5
1.3 Tujuan Penelitian .............................................................................. 6
1.4 Manfaat Penelitian ............................................................................ 6
BAB II TINJAUAN PUSTAKA ........................................................................... 7
2.1 Senyawa Calkon................................................................................ 7
2.2 Retrosintesis ...................................................................................... 8
2.3 Kondensasi Aldol .............................................................................. 10
2.4 Vanilin............................................................................................... 12
2.5 Senyawa Antibakteri ......................................................................... 13
2.6 Bakteri ............................................................................................... 15
2.7 Kromatografi ..................................................................................... 18
2.8 Spektroskopi ..................................................................................... 19
BAB III METODE PENELITIAN........................................................................ 26
3.1 Tempat dan Waktu Penelitian ........................................................... 26
3.2 Alat dan Bahan penelitian ................................................................. 26
3.3 Tahapan Penelitian ............................................................................ 27

x
3.4 Diagram alir penelitian ..................................................................... 32
BAB IV HASIL DAN PEMBAHASAN .............................................................. 33
4.1 Menguji Kemurnian Vanilin ............................................................. 33
4.2 Sintesis Calkon.................................................................................. 34
4.3 Analisis Spektroskopi ....................................................................... 36
4.4 Uji Aktivitas Antibakteri................................................................... 41
BAB V KESIMPULAN DAN SARAN ................................................................ 44
5.1 Kesimpulan ....................................................................................... 45
5.2 Saran ................................................................................................. 45
DAFTAR PUSTAKA ........................................................................................... 46

xi
DAFTAR TABEL
Nomor Judul Tabel Halaman
4.1 Harga Rf vanilin dengan tiga sistem eluen ..................................................... 33
4.2 Harga Rf senyawa calkon (5) dengan tiga sistem eluen .................................. 36

xii
DAFTAR GAMBAR
Nomor Judul Gambar Halaman
2.1 Analisis retrosintesis senyawa target (4) & (5) ............................................... 9
2.2 Mekanisme reaksi Claisen Schmidt pada calkon ............................................ 11
4.1 Unit aromatis senyawa target .......................................................................... 38
4.2 Prediksi struktur senyawa berdasarkan spektrum RMI proton ....................... 39
4.3 Prediksi struktur senyawa berdasarkan spektrum RMI karbon....................... 40
4.4 Struktur tetrasiklin ........................................................................................... 41
4.5 Grafik zona hambat bakteri Staphylococcus aureus ....................................... 42
4.6 Grafik zona hambat bakteri Escherichia coli .................................................. 43

xiii
DAFTAR LAMPIRAN
Nomor Judul Lampiran
1. Spektrum IR Vanilin
2. Spektrum MS Senyawa (4)
3. Spektrum UV-Vis Senyawa (5)
4. Spektrum Inframerah Senyawa (5)
5. Spektrum MS Senyawa (5)
6. Spektrum RMI Proton dan Karbon Senyawa (5)
7. Diameter Zona Hambat Senyawa Uji terhadap Staphylococcus aureus
8. Diameter Zona Hambat Senyawa Uji terhadap Escherichia coli

xiv
BAB I
PENDAHULUAN
1. 1 Latar Belakang Masalah
Di dalam kehidupan, lingkungan organisme tidak dapat dipisahkan dari
bakteri. Sekalipun lingkungan terlihat bersih, namun sebenarnya terdapat jutaan
bakteri tersebar di lingkungan tersebut. Bakteri ada yang bersifat menguntungkan
ada pula yang bersifat merugikan (Pelczar dan Chan, 1988). Bakteri yang bersifat
merugikan dan menyebabkan penyakit disebut bakteri patogen. Bakteri patogen
ini adalah mikroorganisme yang banyak menyebabkan penyakit infeksi. Di negara
berkembang, penyakit infeksi yang disebabkan oleh bakteri menduduki peringkat
cukup tinggi dalam urutan penyakit yang diderita penduduk dan penyebab
kematian yang cukup besar (Rahayu, 2009).
Contoh bakteri yang dapat menyebabkan penyakit infeksi adalah
Staphylococcus aureus dan Escherichia coli. Bakteri S. aureus merupakan bakteri
gram positif yang menyebabkan penyakit diantaranya : infeksi saluran pernafasan,
pembengkakan organ, endocarditis, dan toxic shock syndrome (Elliott, 2007).
Sedangkan bakteri E. Coli merupakan bakteri gram negatif yang menyebabkan
penyakit seperti : infeksi kandung kemih, gastroentritis meningitis pada bayi, dan
yang paling banyak adalah diare (Elliott, 2007).
Walaupun telah banyak zat antibiotik yang ditemukan untuk mengatasi
penyakit akibat bakteri patogen, fakta menunjukkan masalah penyakit ini masih
berkelanjutan (Mulyati, 2009). Hal tersebut terjadi karena adanya perkembangan
1

xv
resistensi bakteri terhadap antibiotik, seperti Staphylococcus aureus yang
diketahui mempunyai sifat resisten terhadap beberapa antibiotik seperti metisilin,
penisilin, nafsilin, dan oksasilin (Bailey, 2002). Oleh sebab itu perlu dilakukan
sintesis senyawa lain yang juga potensial sebagai antibakteri.
Dewasa ini banyak senyawa baru yang telah disintesis karena dianggap
potensial sebagai antibakteri. Salah satunya adalah senyawa calkon (1). Senyawa
ini dikatakan potensial untuk berbagai aktifitas biologis dan farmakologis, seperti:
antibakteri, antiinflamasi, antifungal, antiviral, dan antioksidan (Mokle, 2010).
(1)
Calkon memiliki gugus karbonil α,β-tak jenuh yang reaktif yang memiliki
potensi sebagai antibakteri (Prasad, 2008). Gugus karbonil α,β-takjenuh diketahui
dapat menghambat kerja enzim dan menyebabkan metabolisme sel terganggu
sehingga menyebabkan kematian sel.
Beberapa contoh senyawa calkon hasil sintesis yang telah dilaporkan
memiliki aktivitas sebagai antibakteri adalah sebagai berikut: Senyawa 4-(3-
diklorofenil-3-oxopropenil) benzaldehid (2) yang memiliki nilai MIC (Minimum
Inhibit Concentration) terhadap bakteri S.aureus sebesar 64µg/ml, dan nilai MIC
terhadap E.coli sebesar >64µg/ml (Chen, et al., 2010). Struktur senyawa (2) ini
memiliki satu buah gugus karbonil α,β-tak jenuh.
2

xvi
Cl
Cl
CHO
O
(2)
Liu, et al., (2007) di dalam jurnal penelitiannya juga melaporkan bahwa
senyawa (3) memiliki aktivitas antibakteri terhadap S. aureus dengan nilai MIC
sebesar 6,3 µg/ml.
OCH 3
H3CO OH
N
Cl
CH3
O
(3)
Menurut Liu, et al., (2007), senyawa (3) tersebut memiliki gugus OH dan
N-metilpiperidin yang diduga meningkatkan aktivitas antibakteri. Senyawa (3)
tersebut merupakan yang paling aktif bila dibandingkan dengan senyawa lain
yang tidak memiliki kedua gugus tersebut.
Fakta lain terkait dengan struktur calkon dan aktivitasnya sebagai
antibakteri juga diungkapkan oleh Patil, et al., (2009) dalam jurnal penelitiannya
yang menyatakan bahwa senyawa yang mengikat gugus metoksi dan hidroksi
pada aromatis memperlihatkan aktivitas antibakteri lebih baik dibandingkan
dengan yang tidak.
3

xvii
Dari fakta-fakta di atas, maka pada penelitian ini akan disintesis suatu
senyawa target yang memiliki dua buah gugus karbonil α,β-tak jenuh, gugus
metoksi, hidroksi, dan N-metilpiperidin dengan harapan akan memiliki aktivitas
antibakteri dan tidak resisten. Berikut ini adalah struktur senyawa target yang
akan disintesis :
N
O
CH3
H3CO
HO
OCH 3
OH
3,5-bis-(4-hidroksi-3-metoksibenzilidin)-1-metilpiperidin-4-on
(4)
Dari analisis retrosintesis, senyawa target 3,5-bis(4-hidroksi-3-
metoksibenzilidin)-1-metilpiperidin-4-on dapat disintesis dari vanilin dan N-
metilpiperidin-4-on melalui mekanisme kondensasi Claisen-Schmidt dengan
katalis basa. Pada strukturnya, vanilin memiliki substituen metoksi dan hidroksi
yang terikat pada benzaldehid, sehingga diasumsikan vanilin memiliki potensi
untuk menjadi bahan dasar sintesis senyawa biscalkon (4) yang bersifat bioaktif.
Selain itu, vanilin adalah senyawa yang murah dan mudah didapatkan.
Selanjutnya senyawa hasil sintesis tersebut akan diuji aktivitas
antibakterinya terhadap bakteri S.aureus dan E.coli yang masing-masing mewakili
bakteri gram positif dan negatif. Sintesis senyawa ini juga diharapkan mampu
memberikan nilai tambah pada vanilin.
4

xviii
Pada penelitian ini juga dilakukan sintesis 3,5-bis-(2,5-
dimetoksibenzilidin)-1-metilpiperidin-4-on (5). Berikut ini adalah struktur
senyawa 3,5-bis-(2,5-dimetoksibenzilidin)-1-metilpiperidin-4-on :
OCH 3
OCH 3
N
CH3
OCH 3
OCH 3
O
(5)
Dari analisis retrosintesis, penggunaan vanilin sebagai bahan dasar dapat
diganti dengan 2,5-dimetoksibenzaldehid untuk menghasilkan senyawa 3,5-bis-
(2,5-dimetoksibenzilidin)-1-metilpiperidin-4-on. Senyawa hasil sintesis (5) ini
juga akan diuji aktivitas antibakterinya menggunakan Staphylococcus aureus dan
Escherichia coli.
1. 2 Rumusan Masalah
Dari latar belakang di atas maka dapat dirumuskan permasalahan sebagai
berikut.
1. Apakah senyawa 3,5-bis-(4-hidroksi-3-metoksibenzilidin)-1-
metilpiperidin-4-on dapat disintesis dari vanilin dan N-metil-
piperidin-4-on ?
2. Apakah senyawa 3,5-bis-(2,5-dimetoksibenzilidin)-1-
metilpiperidin-4-on dapat disintesis dari 2,5-dimetoksibenzaldehid
dan N-metil-piperidin-4-on ?
5

xix
3. Apakah senyawa target memiliki aktivitas sebagai antibakteri ?
1. 3 Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mensintesis senyawa 3,5-bis-(4-hidroksi-3-metoksibenzilidin)-1-
metilpiperidin-4-on dari bahan dasar vanilin dan N-metil-piperidin-
4-on.
2. Mensintesis senyawa 3,5-bis-(2,5-dimetoksibenzilidin)-1-
metilpiperidin-4-on dari bahan dasar 2,5-dimetoksibenzaldehid dan
N-metil-piperidin-4-on.
3. Menguji bioaktivitas senyawa target sebagai antibakteri.
1. 4 Manfaat Penelitian
Manfaat dari penelitian ini adalah memberikan informasi apakah kedua
senyawa target dapat disintesis melalui kondensasi Claisen-Smidt dan juga
memberikan informasi tentang bioaktifitasnya sebagai antibakteri. Penelitian ini
juga diharapkan dapat memberikan sumbangan terhadap perkembangan ilmu
sintesis organik dan kimia bahan alam.
6

xx
BAB II
TINJAUAN PUSTAKA
2. 1 Senyawa Calkon
Senyawa calkon (1) adalah senyawa golongan flavonoid yang jumlahnya
terbatas di alam. Karena alasan tersebut calkon juga sering disebut sebagai
flavonoid minor (Harborne, 1987). Calkon memiliki nama IUPAC 1,3-difenil-2-
propena-1-on. Senyawa calkon merupakan senyawa intermediet yang bisa
digunakan untuk sintesis berbagai senyawa heteroatom.
Sesuai dengan strukturnya, senyawa calkon (1) mempunyai dua cincin
aromatis yang dihubungkan dengan tiga atom karbon yang memiliki gugus
karbonil α,β-tak jenuh (Patil, 2009). Gugus karbonil α,β-tak jenuh yang reaktif
tersebut pada beberapa penelitian sebelumnya telah dilaporkan memiliki aktivitas
biologis sebagai antibakteri, antiinflamasi, antioksidan, antiviral, antimalaria, dan
antikanker (Patil, 2009). Gugus karbonil α,β-takjenuh diketahui dapat
menghambat kerja enzim dan menyebabkan metabolisme sel terganggu sehingga
menyebabkan kematian sel.
Senyawa calkon bisa didapat melalui isolasi tanaman maupun sintesis.
Contoh senyawa calkon yang dilaporkan memiliki aktivitas sebagai antibakteri
adalah 2,4-dihidroksi-3,6-dimetoksicalkon (Usman dkk, 2006). Senyawa (7) yang
didapat melalui isolasi tanaman Cryptocarya costata ini dilaporkan memiliki
aktivitas antibakteri sebesar 35,4%. Berikut ini adalah struktur senyawanya :
7

xxi
HO
H3CO
OCH 3
O
(7)
2. 2 Retrosintesis
Apabila akan melakukan sintesis suatu senyawa organik, langkah awal
yang dilakukan adalah melakukan analisis retrosintesis. Analisis retrosintesis ini
berfungsi untuk mengetahui apakah suatu senyawa baru dapat disintesis dari
senyawa awal. Senyawa awal yang digunakan untuk sintesis juga harus
dipertimbangkan ketersediaannya dan harganya di pasaran. Analisis retrosintesis
ini diawali dengan melakukan diskoneksi terhadap molekul senyawa target.
Diskoneksi adalah analisis yang memutus suatu ikatan dan mengubah molekul ke
dalam molekul awal yang mungkin. Dari tahap diskoneksi ini akan dihasilkan
fragmen umum biasanya berupa ion yang disebut sinton (Warren,1995). Selain
diskoneksi, langkah yang dapat diambil pada analisis retrosintesis adalah IGF
(Interkonvensi Gugus Fungsi). IGF merupakan penggantian suatu gugus fungsi
dengan gugus fungsi lain sehingga memungkinkan terjadinya reaksi. Gambar 2.1
berikut menunjukkan analisis retrosintesis dari kedua senyawa target (4) & (5) :
8

xxii
Retrosintesis senyawa (4) :
N
H3CO
HO
OCH 3
OH
CH3
O
N
H3CO
HO
OCH 3
OH
CH3
OOH OH
H3CO
HO
H
O
Vanilin
N
O
CH3
N-metilpiperidin-4-on
Retrosintesis senyawa (5) :
N
CH3
O
N
CH3
OOH OH
OCH 3
OCH 3
OCH 3
OCH 3
OCH 3
OCH 3
OCH 3
OCH 3
H
O
N
O
CH3
N-metilpiperidin-4-on
OCH 3
OCH 3
2,5-dimetoksibenzaldehid
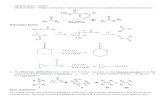
Gambar 2.1 Analisis retrosintesis senyawa target (4) & (5)
IGF
IGF
9

xxiii
2. 3 Kondensasi Aldol
Reaksi kondensasi adalah reaksi dimana dua molekul atau lebih bergabung
menjadi satu molekul yang lebih besar dengan atau tanpa hilangnya suatu molekul
kecil (Fessenden, 1986). Reaksi kondensasi aldol merupakan reaksi antara dua
senyawa karbonil yang melibatkan enolat dan gugus karbonil. Prinsip dasar
reaksi ini adalah adisi ikatan rangkap C=O pada sebuah senyawa karbonil oleh
senyawa karbonil lainnya membentuk β-hidroksi karbonil. Pada reaksi ini
diperlukan sebuah basa agar sebuah senyawa karbonil dapat membentuk ion
enolat. Ion enolat dapat terbentuk dari senyawa karbonil yang memiliki hidrogen-
α. Oleh karena itu dapat dikatakan bahwa syarat utama terbentuknya senyawa
aldehid-alkohol (aldol) ini adalah adanya atom hidrogen yang berposisi-α
terhadap gugus karbonil. Kemudian, ion enolat inilah yang menyerang atom
karbon pada C=O. Saat ion enolat menyerang gugus karbonil, maka terjadi reaksi
adisi karbonil sehingga terbentuklah gugus hidroksi yang berposisi β terhadap
karbonil. Senyawa yang terbentuk adalah ion alkoksida yang kurang stabil. Oleh
karena itu ion alkoksida tersebut dengan mudah menarik proton dari air dan
menghasilkan aldol. Produk yang muncul bisa dengan mudah terdehidrasi dan
menghasilkan suatu senyawa karbonil α,β tak jenuh (Fessenden, 1986).
Apabila suatu senyawa karbonil yang tidak memiliki hidrogen α
direaksikan dengan karbonil yang memiliki hidrogen α, maka reaksi yang terjadi
adalah reaksi kondensasi aldol silang (Claisen-Schmidt). Kondensasi aldol silang
dapat terjadi dalam suasana asam maupun basa.
10

xxiv
Suatu senyawa calkon dapat disintesis melalui reaksi Claisen-Schmidt
(Patil, 2009). Berikut ini adalah mekanisme reaksi Claisen-Schmidt untuk sintesis
senyawa target (4) dalam suasana basa :
N
O
CH3
H
N
O
CH3
N
O
CH3
N
O
CH3
H2O+
H
O
OMe
OHN
O
CH3
OMe
OH
O
N
O
CH3
OMe
OH
OH
H+
N
O
CH3
OMe
OH
OH
HH
N
O
CH3
OMe
OH
OH
N
O
CH3
OMe
OH
OH
OH
Enolat
H2O+
Gambar 2.2 Mekanisme reaksi Claisen Schmidt pada calkon
11

xxv
2. 4 Vanilin
Vanilin merupakan suatu senyawa yang terdapat dalam tanaman vanili.
Tanaman vanili ini banyak tumbuh di daerah panas dan lembab yang tersebar di
wilayah Amerika tengah dan selatan. Selain itu vanili juga tersebar di daerah yang
beriklim tropis seperti Indonesia. Berikut ini adalah klasifikasi dari tanaman
vanili:
Kerajaan : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Orchidales
Famili : Orchidaceae
Genus : Vanilla
Spesies : Vanilla planifolia
Tanaman vanili banyak dimanfaatkan sebagai penambah aroma pada
makanan karena tanaman ini memiliki bau yang khas. Aroma yang khas tersebut
berasal dari senyawa vanilin. Senyawa vanilin (6) memiliki nama IUPAC 4-
hidroksi-3-metoksibenzaldehid. Vanilin pertama kali disintesis dari eugenol.
Selain itu vanilin juga dapat disintesis dari lignin. Struktur senyawa vanilin adalah
sebagai berikut :
H3CO
HO
H
O
(6)
12

xxvi
Rumus molekul vanilin adalah C8H8O3, memiliki massa molekul relatif
152,14g/mol, massa jenis sebesar 1,056 g/L, titik leleh 80-81°C, dan titik didih
285°C. Vanilin memiliki bentuk kristal jarum berwarna putih kekuningan, dan
memiliki bau khas. Vanilin mudah larut dalam alkohol, kloroform, asam asetat
glasial, minyak, dan pelarut alkali hidroksida (Merck Index, 1967).
2.5 Senyawa Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengurangi
pertumbuhan bakteri, khususnya bakteri yang merugikan manusia. Suatu senyawa
dikatakan potensial sebagai antibakteri apabila senyawa tersebut memiliki
toksisitas selektif terhadap bakteri. Hal tersebut berarti senyawa antibakteri itu
hanya berbahaya bagi bakteri, tetapi relatif tidak membahayakan bagi sel yang
lain. Berdasarkan sifat toksisitas selektif, ada senyawa antibakteri yang bersifat
menghambat pertumbuhan bakteri disebut bakteriostatik dan ada yang bersifat
membunuh bakteri disebut bakterisida (Bailey, 2002).
Berdasarkan mekanisme kerjanya, senyawa antibakteri dibagi menjadi 5
kelompok, yaitu :
a. merusak dinding sel yaitu dengan menghambat pembentukan
peptidoglikan pada dinding sel mengakibatkan enzim mengalami autolisis
sehingga sel mengalami kerusakan.
b. mengganggu permeabilitas sel yaitu dengan merusak membran sel. Fungsi
membran sel adalah mempertahankan bahan-bahan dalam sel serta
mengatur aliran keluar masuknya bahan lain. Adanya kerusakan pada
13

xxvii
membran ini mengakibatkan terhambatnya pertumbuhan sel atau
kematian.
c. merubah molekul protein dan asam nukleat yaitu dengan
mendenaturasikan protein dan asam nukleat sehingga kerusakan sel tidak
dapat diperbaiki lagi karena hidup suatu sel tergantung pada molekul
protein dan asam nukleat dalam keadaan alamiah.
d. menghambat kerja enzim dengan mengganggu reaksi biokimiawi yaitu
dengan menempelnya zat antibakteri yang menyerupai substrat pada sisi
aktif enzim. Penghambatan ini dengan mengakibatkan terganggunya
metabolisme sel.
e. menghambat sintesis asam nukleat dan protein. Gangguan pada
pembentukan atau fungsi-fungsi DNA, RNA dan protein dapat
mengakibatkan kerusakan total pada sel, karena zat-zat tersebut memegang
peranan penting dalam proses kehidupan normal sel (Pelczar dan Chan,
1988).
Contoh senyawa antibakteri yang banyak digunakan adalah penisilin (8).
Berikut ini adalah struktur senyawa penisilin :
N
O
HN
S
RO
HO
O
(8)
Cincin beta laktam yang terdapat pada senyawa ini diketahui berperan
dalam menghambat sistesis dinding sel bakteri. Senyawa antibakteri lain yang
14

xxviii
banyak digunakan adalah kloramfenikol (9). Senyawa ini menghambat
pertumbuhan bakteri melalui mekanisme penghambatan sintesis protein pada sel
bakteri. Chloramphenicol menghambat proses transpeptidase (dikatalisis oleh
enzim peptidil transferase) dengan cara memblok pengikatan aminoasil pada
tRNA ke acceptor site pada mRNA di rhibosome -messenger (mRNA) complex.
Berikut ini adalah struktur senyawa kloramfenikol :
O2N
OH
OH
N
Cl
Cl
O
(9)
2. 6 Bakteri
Bakteri adalah mikroorganisme bersel satu. Inti sel bakteri tidak
bermembran disebut prokariot dan melekat pada sitoplasma. Sel bakteri memiliki
bentuk bulat, batang dan spiral dan berukuran mikron. Struktur tubuh bakteri
umumnya tersusun atas: inti sel, sitoplasma, membran sitoplasma, dinding sel,
kapsul, flagel, pili, dan spora. Berdasarkan pewarnaan, bakteri digolongkan ke
dalam dua golongan, yaitu bakteri gram positif dan gram negatif. Perbedaan
warna pada kedua golongan bakteri tersebut terjadi karena perbedaan struktur
pada dinding selnya. Pada umumnya bakteri tumbuh pada batas suhu ekstrim (0-
90°C). Pada keadaan ekstrim, seperti pada temperatur dan pH yang ekstrim,
15

xxix
bakteri dapat membentuk spora. Di antara bakteri ada yang dapat menimbulkan
penyakit pada tumbuhan, hewan, maupun mikroba lainnya (Pelczar dan Chan,
1988). Akan tetapi tidak semua bakteri bersifat merugikan, ada juga bakteri yang
menguntungkan, seperti bakteri penghasil antibiotik, enzim, biopestisida, dan
fermentasi makanan.
2. 6. 1 Staphylococcus aureus
Staphylococcus aureus merupakan golongan bakteri gram positif dan
bersifat fakultatif aerob. Bakteri ini berbentuk bulat dengan diameter antara 0,8-
1,0 µm yang tersusun dalam kelompok-kelompok tidak teratur, tidak bergerak,
dan tidak membentuk spora. Koloni pada biakan padat membentuk bulat halus,
berkilau-kilau, membentuk pigmen berwarna kuning emas (Jawetz, et al., 1982).
Berikut ini adalah klasifikasi dari Staphylococcus aureus :
Domain : Bacteria
Filum : Firmicules
Kelas : Bacilli
Ordo : Bacillales
Famili : Staphylococcaceae
Genus : Staphylococcus
Spesies : Staphylococcus aureus
Staphylococcus aureus mudah tumbuh pada berbagai media. Bakteri ini
dapat tumbuh pada suhu antara 12-44°C tetapi tumbuh paling optimum pada suhu
sekitar 37°C. Staphylococcus aureus memiliki kemampuan menghasilkan banyak
zat ekstraseluler, sehingga bakteri ini dapat menyebar luas ke dalam jaringan dan
16

xxx
berkembangbiak dan selanjutnya mengakibatkan penyakit. Bila bakteri ini berada
pada individu yang sehat, maka sel inangnya hanya berperan sebagai karier.
Infeksi hanya terjadi jika resistensi tubuh inang melemah karena adanya
perubahan hormon, adanya luka, penggunaan obat, atau hal lain yang dapat
melemahkan imunitas sel inang. Bakteri ini dapat menyebabkan peritonis, cystitis
dan meningitis (Jawetz et al., 1982). Staphylococcus aureus mempunyai sifat
resistan terhadap beberapa antibiotik seperti metisilin, penisilin, nafsilin, dan
oksasilin (Bailey, 2002).
2. 6. 2 Escherichia coli
Escherichia coli merupakan golongan bakteri gram negatif dan bersifat
fakultatif aerob. Bakteri ini pertama kali ditemukan oleh Theodor Escherich tahun
1885. Bakteri ini berbentuk batang. Berikut ini adalah klasifikasi dari Escherichia
coli :
Domain : Bacteria
Filum : Proteobacteria
Kelas : Gamma Proteobacteria
Ordo : Enterobacteriales
Famili : Enterobacteriaceae
Genus : Escherichia
Spesies : Escherichia coli
Escherichia coli tumbuh baik pada hampir semua media yang biasa
dipakai di laboratorium mikrobiologi. Escherichia coli adalah bakteri yang
banyak ditemukan di dalam usus besar manusia. Bakteri ini dapat menyebabkan
17

xxxi
infeksi primer pada usus misalnya diare pada anak serta dapat menimbulkan
infeksi pada jaringan tubuh lain di usus . E. coli merupakan spesi normal di dalam
usus manusia dan akan menimbulkan penyakit bila masuk ke dalam organ atau
jaringan lain. Escherichia coli juga dapat menimbulkan pneumonia, infeksi
kandung kemih, gastroentritis dan meningitis pada bayi, dan yang paling banyak
adalah diare (Elliott, 2007).
2. 7 Kromatografi
Teknik pemisahan dan pemurnian yang umum digunakan adalah
kromatografi. Kromatografi berasal dari bahasa yunani yaitu kromatos yang
berarti warna dan graphos yang berarti menulis. Kromatografi merupakan teknik
pemisahan suatu campuran menjadi komponen-komponennya berdasarkan
perbedaan distribusinya ke dalam fasa gerak dan fasa diam atau berdasarkan pada
perbedaan adsorpsi pada fasa diam. Fasa gerak pada kromatografi membawa zat
terlarut melalui media hingga terpisah dari zat terlarut lainnya. Berdasarkan fasa
gerak dan fasa diamnya kromatografi dibedakan menjadi: kromatografi cair-padat,
cair-cair, gas-padat, dan gas-cair (Touchstone, 1992). Metode kromatografi yang
sering digunakan untuk pemisahan antara lain : kromatografi lapis tipis,
kromatografi kolom, kromatografi cair vakum, dan kromatografi kolom cepat.
Kromatografi lapis tipis (KLT) adalah salah satu metode yang sering
digunakan untuk menguji kemurnian suatu senyawa. KLT berupa lapisan tipis
yang memiliki ketebalan sekitar 0,1-2 mm. Lapisan tipis tersebut tersusun atas
fasa diam yang dilapiskan diatas pelat penyangga. Fasa diam yang digunakan
18

xxxii
pada umumnya adalah silika gel, alumina, selulosa, dan poliamida. Pelat
penyangga dapat berupa kaca gelas, pelat polimer, dan pelat aluminium. Di antara
fasa diam tersebut, yang banyak dipakai adalah silika gel. Fasa diam ini berfungsi
sebagai penyerap. Sedangkan fasa gerak dalam KLT adalah eluen, biasanya
berupa campuran pelarut tergantung dari sifat polaritas senyawa kimia yang akan
dipisahkan (Gritter, 1991).
Senyawa yang akan diuji dilarutkan dalam pelarut yang sesuai, lalu
ditotolkan pada pelat KLT menggunakan pipa kapiler. Setelah kering, pelat
dimasukkan ke dalam bejana yang berisi eluen. Begitu proses elusi selesai, pelat
KLT diambil dari bejana dan dikeringkan. Hasil kromatogram yang berupa bercak
noda dapat dilihat dengan bantuan sinar UV atau direaksikan dengan pereaksi
warna seperti cerium sulfat. Suatu senyawa dikatakan murni apabila hanya
menampakkan satu noda dalam uji menggunakan tiga eluen yang berbeda. Data
yang didapatkan berupa Rf yaitu faktor retardasi dengan perhitungan :
2. 8 Spektroskopi
Metode spektroskopi digunakan dalam penentuan struktur molekul suatu
senyawa organik. Spektroskopi merupakan ilmu yang mempelajari tentang
antaraksi antara energi cahaya. Panjang gelombang dimana suatu senyawa organik
dapat menyerap energi cahaya tergantung dari struktur senyawa tersebut. Karena
itulah metode ini dapat digunakan untuk menentukan struktur suatu senyawa yang
tidak diketahui (Fessenden, 1986). Spektroskopi yang sering digunakan untuk
19

xxxiii
menentukan struktur suatu senyawa organik antara lain adalah spektroskopi UV-
Vis, inframerah, Resonansi Magnetik Inti, dan spektroskopi massa.
2. 8. 1 Spektroskopi ultraviolet-visibel
Spektroskopi UV-Vis adalah suatu metode yang digunakan untuk
mengetahui ada atau tidaknya senyawa yang memiliki ikatan rangkap
terkonjugasi. Prinsip dari spektroskopi ini adalah transisi elektron. Energi yang
diserap oleh molekul senyawa akan menyebabkan elektron yang berada pada
tingkat energi dasar mengalami eksitasi ke tingkat energi yang lebih tinggi
(Fessenden, 1986).
Absorbansi radiasi elektromagnetik pada daerah ultraviolet dan daerah
sinar tampak sesuai dengan transisi molekul antara tingkat energi elektron pi dan
elektron bebas. Pada daerah UV dengan panjang gelombang di bawah 200 nm,
tidak nampak pita absorbansi. Pada daerah panjang gelombang 200-400 nm
merupakan daerah dekat UV, senyawa tidak berwarna terukur pada panjang
gelombang ini, sedangkan daerah sinar tampak ditunjukkan pada panjang
gelombang 400-700 nm, senyawa yang berwarna terukur pada panjang gelombang
ini (Iverson, 1998). Analisis calkon akan menghasilkan spektrum puncak pada
daerah panjang gelombang 230-270 nm dan 340-390 nm (Markham,1981).
2. 8. 2 Spektroskopi inframerah
Metode spektroskopi inframerah biasa digunakan untuk menentukan
gugus-gugus fungsi yang terdapat pada suatu senyawa. Spektroskopi ini terjadi
karena adanya radiasi inframerah yang diserap oleh molekul senyawa organik dan
menyebabkan terjadinya vibrasi molekul. Vibrasi molekul terdiri dari dua tipe
20

xxxiv
yaitu vibrasi tekuk dan vibrasi ulur. Pada vibrasi ulur terjadi perubahan jarak yang
semakin menjauh antar dua atom dalam molekul, sedangkan pada vibrasi tekuk
terjadi perubahan sudut ikatan antara atom dalam molekul (Silverstein,1991).
Untuk mengidentifikasi gugus-gugus fungsi pada suatu senyawa
digunakan daerah dengan bilangan gelombang 4000-1600 cm-1
. Daerah dengan
bilangan gelombang tersebut disebut daerah gugus fungsi, sedangkan daerah
dengan bilangan gelombang di bawah 1400 cm-1
disebut daerah sidik jari karena
pada daerah ini banyak terjadi absorpsi uluran dan tekukan sehingga gugus fungsi
tidak dapat diamati dengan cermat (Fessenden, 1986), tetapi pada daerah ini setiap
senyawa organik memiliki resapan yang unik, sehingga dapat pula digunakan
untuk membuktikan apakah senyawa yang mirip benar-benar merupakan senyawa
yang sama.
Radiasi yang diserap tiap molekul tidak sama, tergantung dari gugus-
gugus fungsi yang terdapat dalam senyawa tersebut. Misalnya gugus OH muncul
pada daerah 3000-3700 cm-1
dengan pita yang melebar, gugus C=O akan
menghasilkan pita tajam pada daerah 1600-1750 cm-1
, dan lain sebagainya
(Fessenden, 1986).
Analisis calkon akan menghasilkan spektrum dengan pita-pita pada
bilangan gelombang 1600-1750 cm-1
kerena memiliki gugus karbonil, gugus C=C
pada 1550-1650 cm-1
, dan pada 3000-3300 cm-1
kerena memiliki gugus C-H
aromatis (Fessenden,1986).
21

xxxv
2. 8. 3 Spektroskopi resonansi magnetik inti
Spektroskopi resonansi magnet inti (RMI) adalah suatu metode penentuan
struktur molekul yang didasarkan pada penyerapan energi oleh partikel yang
sedang berputar dalam medan magnet yang kuat. Jumlah dan tempat proton
dalam molekul organik menentukan bentuk spektrum yang dihasilkan (Sudjadi,
1983). Spektroskopi ini meliputi dua jenis yaitu : spektroskopi RMI proton dan
spektroskopi RMI karbon. RMI proton memberikan informasi mengenai atom-
atom hidrogen pada molekul organik, sedangkan RMI karbon memberikan
informasi tentang struktur yang terkait dengan atom-atom karbon suatu senyawa
(Fessenden, 1986).
Salah satu kelebihan metode spektroskopi ini dibanding metode lainnya
adalah cuplikan dapat diperoleh kembali, tidak mengalami perubahan setelah
pengukuran, dan dapat digunakan lagi untuk pengukuran berikutnya (Harborne,
1987).
2. 8. 3. 1 Spektroskopi resonansi magnetik inti proton (H1-RMI)
Spektrum RMI proton digunakan untuk menentukan struktur senyawa
dengan mengukur momen magnet atom hidrogennya. Metode ini memberikan
informasi tentang letak atom hidrogen pada molekul senyawa berdasarkan posisi
sinyal, jumlah H lewat integrasi, dan interaksi kopling antar H yang bersebelahan
melalui data multiplisitas. Spektrum ini tidak dapat memberikan keterangan
langsung mengenai struktur karbon dari suatu senyawa (Harborne, 1987).
Spektrum 1H-RMI sering terlihat di daerah 0-14 ppm.
22

xxxvi
Spektrum 1H-RMI merupakan hasil rekaman sejumlah atom hidrogen yang
berada dalam lingkungan kimia yang berlainan. Karena alasan itulah maka pelarut
untuk pengukuran RMI ini harus inert dan tanpa proton. Oleh sebab itu,
pengukuran spektroskopi RMI menggunakan pelarut seperti karbontetraklorida
(CCl4), deuterokloroform (CDCl3), deuterium oksida (D2O), atau
dimetilsulfoksida terdeuterasi (Silverstein,1991).
Analisis calkon akan menghasilkan spektrum pada 1H-RMI yang dapat
diamati dari munculnya spektra pada daerah 9 ppm yang menunjukkan adanya
gugus karbonil dan munculnya spektra pada daerah sekitar 7 ppm yang
menandakan adanya gugus aromatis, selain itu juga munculnya spektra pada
daerah 5-6 ppm yang menandakan adanya ikatan rangkap alkena.
2. 8. 3. 2 Spektroskopi resonansi magnetik inti karbon (13
C-RMI)
Spektrum 13
C-RMI memberikan informasi mengenai jumlah atom C dalam
senyawa, jenis atom C, serta jenis hibridisasi atom C berdasarkan nilai geseran
kimia. Atom C yang memiliki lingkungan kimia yang berbeda akan menunjukkan
geseran yang khas, misalnya atom karbon alifatis menunjukkan geseran antara 0-
40 ppm, atom karbon aromatis pada 120-150 ppm, dan atom karbon keton pada
160-200 ppm (Harborne, 1987). Pelarut yang digunakan dalam pengukuran
spektroskopi 13
C-RMI sama dengan yang digunakan dalam pengukuran
spektroskopi 1H-RMI.
Spektrum yang dihasilkan spektroskopi ini dapat berupa spektrum
dekopling proton yaitu sinyal yang muncul tidak mengalami penguraian karena C
tidak terkopling dengan H sehingga tiap tipe atom karbon muncul sebagai singlet,
23

xxxvii
atau spektrum kopling proton yaitu sinyal yang muncul untuk tiap tipe karbon
diuraikan oleh proton-proton yang terikat langsung dengan atom karbon tersebut.
Tipe atom karbon pada spektrum kopling proton ini ada 4 macam yaitu: atom
karbon primer CH3 memberikan sinyal kuartet, atom karbon CH2 memberikan
sinyal triplet, atom karbon tersier CH memberikan sinyal doublet dan atom karbon
kuartener C memberikan sinyal singlet (Fessenden, 1986).
Analisis seyawa calkon menggunakan 13
C-RMI dapat diamati dari
munculnya sinyal karbon karbonil yang muncul di daerah sekitar 200 ppm, dan
sinyal karbon aromatis akan muncul di daerah sekitar 120-150 ppm.
2. 8. 4 Spektroskopi massa (MS)
Spektroskopi massa merupakan pemisahan dan pengukuran ion
berdasarkan rasio massa terhadap muatan (m/z). Metode ini berfungsi untuk
menentukan pola fragmentasi dan berat molekul suatu senyawa. Kelebihan
metode ini dibandingkan metode lainnya adalah sampel yang diperlukan untuk
analisis hanya sedikit (Markham, 1988).
Pada spektroskopi massa, terjadi tumbukan antar molekul suatu senyawa
organik. Adanya elektron berenergi tinggi yang tidak stabil, menyebabkan sebuah
elektron lepas dari molekul tersebut membentuk fragmen ion berupa radikal
kation yang disebut ion molekuler (Watson, 1985).
M + e- M
+ • + 2e
-
(ion molekuler)
Pada spektrum massa akan tampak sederetan sinyal yang
menunjukkan pecahan senyawa induk yang bermuatan. Puncak yang paling tajam
24

xxxviii
merupakan base peak. Base peak merupakan fragmen molekul yang paling stabil.
Kebanyakan base peak merupakan puncak dari ion molekuler, meskipun tidak
selalu seperti itu (Silverstein, 1991).
25

xxxix
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan pada bulan Januari – Juni 2011 di Laboratorium
Kimia Organik, Departemen Kimia, Fakultas Sains dan Teknologi, Universitas
Airlangga. Untuk uji spektroskopi UV-Vis dilakukan di Laboratorium Penelitian,
Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga. Untuk
uji spektroskopi IR dilakukan di Laboratorium Instrumentasi, Departemen Kimia,
Fakultas MIPA, Universitas Negeri Surabaya. Uji spektroskopi RMI dilakukan di
LIPI Bandung. Uji MS dilakukan di Laboratorium Institut Teknologi Bandung.
Sedangkan untuk uji antibakteri dilakukan di Laboratorium Biokimia, Depertemen
Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga.
3.2 Alat dan Bahan Penelitian
3.2.1 Alat penelitian
Alat-alat yang digunakan pada penelitian ini adalah alat pendingin refluks,
labu leher tiga, hot plate, magnetic stirer, corong Buchner, Fischer John
Melting Point Apparatus, neraca analitik, termometer, seperangkat alat KLT, dan
alat-alat gelas yang biasa digunakan di Laboratorium Kimia Organik.
Instrumen yang digunakan untuk identifikasi adalah spektrometer
ultraviolet-visibel Shimadzu, spektrometer infra merah, spektrometer resonansi
magnet inti (1H-RMI dan
13C-RMI) Bruker 400 MHz, dan spektrometer HRMS.
26

xl
Alat-alat yang digunakan untuk uji antibakteri adalah cawan petri, pinset,
pengaduk, pembakar bunsen, mikroskop, autoclave, pipet tetes, pipet mikro,
papan spot tes, oven, tabung kuvet, botol kultur 100 ml, paper disc, ose, dan
jangka sorong.
3.2.2 Bahan penelitian
Bahan-bahan yang digunakan untuk sintesis meliputi : bubuk vanilin, 2,5-
dimetoksibenzaldehid, N-metil piperidin-4-on, etanol, natrium hidroksida, kertas
saring Whatman 40. Bahan-bahan kimia yang diperlukan untuk uji kemurnian
meliputi : pelarut organik seperti etil asetat, etanol, kloroform, dan n-heksana.
Bahan-bahan yang digunakan untuk uji antibakteri meliputi : bakteri Escherichia
coli dan bakteri Staphylococcus aureus yang diperoleh dari Laboratorium
Mikrobiologi Departemen Biologi Fakultas Saintek Universitas Airlangga,
Nutrien Agar (NA), media uji Muller-Hinton Agar (MHA), alumunium foil,
aquades, tissu, dan kapas.
3.3 Tahapan Penelitian
3.3.1 Penyiapan bahan
Bubuk vanilin direkristalisasi dengan campuran metanol-air. Vanilin
dilarutkan dengan metanol panas, kemudian setelah vanilin tepat larut,
ditambahkan air sedikit demi sedikit hingga kristal terbentuk kembali. Kristal
yang telah terbentuk kemudian disaring. Vanilin hasil rekristalisasi kemudian diuji
kemurniannya dengan KLT dan menguji sifat fisiknya dengan mengukur titik
lelehnya menggunakan Fischer John Melting Point Apparatus dengan mengamati
27

xli
saat kristal mulai meleleh sampai tepat meleleh semua dan juga dilakukan uji
spektroskopi IR ( Harborne, 1987).
3.3.2 Sintesis calkon
Sebanyak 6 mmol (0,9 gram) vanilin dilarutkan dengan etanol 90%
sebanyak 10 ml kemudian dimasukkan ke dalam labu alas bulat leher tiga yang
pada masing-masing lehernya diberi termometer, refluks, dan corong tetes. Lalu
ke dalamnya ditambahkan 3 mmol (0,34 gram) N-metil piperidin-4-on. Campuran
didinginkan dan diaduk dengan stirer selama satu jam dan dijaga suhunya agar di
bawah tetap 10°C. Refluks dilakukan dengan penangas es. Apabila suhunya sudah
di bawah 10°C, NaOH 40% sebanyak 3 ml ditambahkan tetes demi tetes ke dalam
campuran melalui corong tetes. Campuran tetap didinginkan selama satu jam
dengan suhu sekitar 10°C. Setelah satu jam, es diambil, dan campuran direfluks
pada suhu kamar selama empat jam. Setelah empat jam, endapan yang terbentuk
disaring menggunakan corong Buchner. Setelah disaring, senyawa yang tebentuk
kemudian direkristalisasi dengan pelarut yang sesuai (Suwito, 2010). Dengan cara
yang sama senyawa berikutnya (5) dapat disintesis dengan mengganti vanillin
dengan 2,5-dimetoksibenzaldehid.
3.3.3 Uji kemurnian dengan KLT
Untuk mengetahui kemurnian senyawa hasil sintesis, digunakan uji KLT.
Pertama, senyawa hasil sintesis dilarutkan dengan pelarut yang sesuai. Kemudian
sampel senyawa ditotolkan pada plat KLT menggunakan pipa kapiler. Plat KLT
tersebut dielusi mengggunakan tiga macam eluen yang berbeda di dalam bejana.
Setelah prosos elusi selesai, plat diangkat dari bejana dan dikeringkan. Setelah
28

xlii
kering, noda pada plat KLT dilihat di bawah sinar UV. Senyawa dikatakan murni
jika hanya menampakkan satu noda dengan tiga sistem eluen yang berbeda.
3. 3. 4 Uji sifat fisik
Senyawa hasil sintesis diukur titik lelehnya dengan menggunakan Fischer
John Melting Point Apparatus. Senyawa ditempatkan pada plat yang tersedia pada
alat, kemudian diatur temperaturnya, Lalu mengamati temperatur saat kristal
mulai meleleh sampai tepat meleleh sempurna. Senyawa dikatakan murni apabila
renyang suhu dari mulai meleleh hingga meleleh sempurna lebih kecil atau sama
dengan 2°C.
3. 3. 5 Uji spektroskopi
3.3.5.1 Uji UV-Vis
Melarutkan senyawa hasil sintesis dengan etanol. Kemudian mengukur
panjang gelombang maksimumnya dengan spektrofotometer UV-Vis.
3.3.5.2 Uji spektroskopi IR
Senyawa hasil sintesis digerus bersama dengan KBr sebanyak 10-100 mg
lalu dicetak menggunakan alat hidrolik membentuk pelet. Pelet lalu diukur
vibrasinya pada bilangan gelombang 4000-650 cm-1
.
3.3.5.3 Uji spektroskopi RMI
Senyawa hasil sintesis dilarutkan terlebih dulu menggunakan pelarut
CDCl3, lalu spektrum proton RMI diukur pada pergeseran 0-14 ppm, sedangkan
spektrum karbon RMI diukur pada pergeseran 0-200 ppm.
29

xliii
3.3.5.4 Uji spektroskopi MS
Sampel senyawa hasil sintesis dilarutkan terlebih dulu, kemudian
dianalisis menggunakan HRMS. Spektrum yang dihasilkan memberikan informasi
tentang pola fragmentasi dan berat molekul senyawa.
3.3.6 Uji aktivitas antibakteri
3.3.6.1 Pembuatan larutan uji
Senyawa murni hasil sintesis dilarutkan dengan pelarut yang sesuai hingga
diperoleh konsentrasi larutan 1000 ppm. Kemudian dibuat variasi konsentrasinya
sebesar 25, 50, 75, 100, 200, 300, 400, dan 500 ppm.
3.3.6.2 Pembuatan media tumbuh untuk peremajaan bakteri
Media pertumbuhan Nutrient Agar (NA) dibuat sebanyak 2 gram yang
dilarutkan pada 100 ml akuades. Media tersebut kemudian disterilisasi
menggunakan autoclave selama 45 menit. Setelah itu didiamkan hingga memadat.
Setelah media NA memadat, bakteri digoreskan pada permukaan media
menggunakan kawat ose steril. Kemudian biakan tersebut diinkubasi pada suhu
37°C.
3.3.6.3 Metode difusi cakram
Suspensi bakteri uji (dibuat dengan Optical Density (OD) 0,1 pada panjang
gelombang 625 nm) sebanyak 10 ml diletakkan dalam cawan petri lalu dituangkan
15 ml media MHA yang sudah disterilisasi. Setelah media uji tersebut memadat,
pada permukaan agar MHA, diletakkan paper disk steril diameter 5 mm dengan
jarak antarkertas berjauhan. Kemudian pada kertas cakram tersebut diinjeksikan
masing-masing sebanyak 10 L senyawa hasil sintesis yang sebelumnya
30

xliv
dilarutkan terlebih dahulu dengan pelarut yang sesuai. Injeksi larutan senyawa
hasil sintesis dilakukan pada beberapa cawan dengan variasi konsentrasi 25, 50,
75, 100, 200, 300, 400, dan 500 ppm. Sebagai kontrol positif digunakan antibiotik
tetrasiklin. Adanya aktivitas antibakteri ditunjukkan dengan terbentuknya daerah
penghambatan di sekitar paper disc setelah diinkubasi selama 24 - 48 jam pada
suhu ruang (Zonby and Starzky, 1986 ; Bailey and Scott, 2002). Diameter daerah
penghambatan tersebut diukur dengan menggunakan jangka sorong.
31

xlv
3.4 Diagram Alir Penelitian
Uji sifat fisik titik
leleh
Senyawa murni
Uji antibakteri
UV-Vis IR RMI MS
Uji Spektroskopi
Sintesis senyawa
target (4)
Penyiapan bahan
Sintesis senyawa
target (5)
Uji Kemurnian dengan
KLT
32

xlvi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Menguji Kemurnian Vanilin
Vanilin yang digunakan dalam sintesis senyawa ini adalah vanilin yang
beredar di pasaran. Untuk menghilangkan pengotor-pengotor di dalamnya,
dilakukan rekristalisasi menggunakan pelarut etanol-air. Kemudian untuk
mengetahui kemurnian vanilin yang telah direkristalisasi, dilakukan uji kemurnian
menggunakan kromatografi lapis tipis (KLT) dan uji titik leleh. Hasil KLT dengan
tiga macam sistem eluen menunjukkan satu noda. Data Rf tertera pada Tabel 4.1.
Tabel 4.1 Harga Rf vanilin dengan tiga sistem eluen
Eluen Rf
n-heksana : Etil Asetat
7:3 0,78
n- heksana : Etil Asetat
5:5 0,51
n-heksana : Etil Asetat
3:7 0,37
Titik leleh senyawa hasil sintesis diamati dengan alat Fisher John Melting
Point Aparatus adalah sebesar 81-83°C. Dengan demikian dapat dikatakan bahwa
vanilin tersebut sudah murni. Selain menguji KLT dan titik leleh, dilakukan juga
uji spektroskopi infra merah (spektrum IR vanilin ditampilkan pada Lampiran 1).
Pita yang muncul pada bilangan gelombang 3175,5 cm -1
merupakan pita ulur OH.
Untuk Vibrasi ulur C-O-C pada gugus metoksi (O-CH3) vanilin muncul dengan
intensitas kuat pada bilangan gelombang 1159 cm-1
. Pita serapan untuk vibrasi
33

xlvii
ulur karbonil muncul pada bilangan gelombang 1670 cm -1
. Sedangkan absorpsi
untuk vibrasi ikatan C=C yang khas pada aril muncul sebagai deretan empat pita
pada bilangan gelombang antara 1511, 1458, 1428, dam 1379 cm-1
.
4.2 Sintesis Calkon
Hal pertama yang dilakukan pada sintesis ini adalah melarutkan vanilin
pada etanol. Kemudian menambahkan berturut-turut n-metil piperidin-4-on dan
NaOH 40%. Penambahan basa kuat ini dilakukan di akhir untuk meminimalkan
terjadinya reaksi samping yang mungkin terjadi dan bertujuan untuk membentuk
ion enolat. Reaksi ini berlangsung selama satu jam pada suhu di bawah 10ºC dan
dilanjutkan selama empat jam pada suhu kamar. Produk akhir yang terbentuk
adalah endapan berwarna kuning kecoklatan, dan apabila dibiarkan, lama
kelamaan warna endapannya menjadi kehitaman. Selanjutnya dilakukan uji
kemurnian menggunakan KLT dan uji titik leleh. Endapan yang terbentuk diuji
titik lelehnya menggunakan Fisher John Melting Point Aparatus dan didapat titik
leleh lebih dari 400ºC. Hasil KLT menunjukkan harga Rf yang sama dengan
vanilin, sehingga diduga produk yang terbentuk masih mengandung vanilin.
Sintesis ini kemudian diulang sebanyak dua kali, dilanjutkan dengan penggantian
bahan dasar berupa vanilin murni, tetapi hasil yang didapat tetap sama.
Produk yang terbentuk tersebut kemudian diuji spektroskopi masa
(spektrum MS senyawa (4) tertera pada Lampiran 2). Berat molekul senyawa
dapat diketahui dari puncak ion molekul pada spektrum. Hasil spektrum MS
produk, menunjukkan puncak ion molekul sebesar 469,0 m/z. Berdasarkan
34

xlviii
spektrum tersebut, menunjukkan bahwa produk hasil sintesis ini bukanlah
senyawa target yang diinginkan karena berat molekul senyawa target yang
seharusnya adalah 381, sedangkan pada kenyataannya tidak menunjukkan
demikian.
Tidak terbentuknya senyawa target yang diharapkan ini diduga karena
penggunaan 4-hidroksi-3-metoksi benzaldehid atau vanilin sebagai salah satu
pereaksi. Keasaman hidrogen pada gugus –OH pada vanilin dianggap sebagai
pengganggu dalam reaksi kondensasi aldol ini, sehingga senyawa target tidak
dapat terbentuk (Sastrohamidjojo dan Pranowo, 2009). Oleh karena itu,
penggunaan vanilin pada reaksi kondensasi aldol silang ini digantikan dengan 2,5-
dimetoksi benzaldehid (10). Tanpa adanya gugus –OH, diharapkan senyawa
target dapat terbentuk dengan mudah. Berikut ini adalah struktur senyawa 2,5-
dimetoksi benzaldehid.
OMe
OMe
H
O
(10)
Dengan cara yang sama, senyawa 2,5-dimetoksi benzaldehid direaksikan
dengan N-metil piperidin-4-on dalam suasana basa, dengan perbandingan mol 2:1.
Endapan yang dihasilkan berwarna kuning muda kemudian direkristalisasi
menggunakan pelarut etanol-air menghasilkan kristal berbentuk jarum.
35

xlix
Senyawa hasil sintesis diuji kemurniannya menggunakan kromatografi
lapis tipis dengan tiga macam eluen yang berbeda yang menunjukkan satu noda.
Harga Rf tertera pada Tabel 4.2.
Tabel 4.2 Harga Rf senyawa calkon (5) dengan tiga sistem eluen
Eluen Rf
n- heksana : Etil Asetat
7:3 0,11
n- heksana : Etil Asetat
8:2 0,14
n-heksana : Aseton
8:2 0,26
Kristal yang terbentuk juga diuji titik lelehnya menggunakan Fisher John
Melting Point Aparatus dan diperoleh titik leleh sebesar 136-138ºC. Dengan
demikian dapat dikatakan bahwa senyawa calkon hasil sintesis berbahan dasar
2,5-dimetoksi benzaldehid telah murni. Senyawa hasil sintesis (5) memiliki berat
sebesar 1,02 gram (dengan rendemen sebesar 83,129 %).
4. 3 Analisis Spektroskopi
4.3.1 Analisis spektroskopi UV-Vis
Senyawa target yang terbentuk diuji spektroskopi UV-Vis dengan rentang
panjang gelombang 200-400 nm (spektrum UV-Vis senyawa (5) dapat dilihat
pada Lampiran 3). Senyawa target dilarutkan terlebih dahulu dengan klorofom,
lalu diukur absorbansinya. Puncak yang muncul adalah pada panjang gelombang
279 nm, 309 nm, dan 380 nm. Pada panjang gelombang 380 nm diduga
merupakan daerah serapan gugus karbonil α-β takjenuh ditambah perpanjangan
36

l
ikatan rangkap dan substituen yang terikat. Sedangkan pada panjang gelombang
279 dan 309 diduga merupakan daerah serapan untuk gugus diena terkonjugasi
(fenil) ditambah perpanjangan ikatan rangkap dan substituen yang terikat. Pada
literatur, analisis calkon akan menghasilkan spektrum puncak pada daerah
panjang gelombang 230-280 nm dan 340-390 nm (Markham,1981).
4.3.2 Analisis spektroskopi inframerah
Senyawa hasil sintesis diuji spektroskopi infra merah menggunakan pellet
KBr. Spektra infra merah senyawa hasil sintesis (5) tertera pada Lampiran 4.
Gugus-gugus fungsi senyawa tersebut keluar sebagai pita-pita serapan pada
bilangan gelombang tertentu yang spesifik. Vibrasi ulur C=O dari senyawa hasil
sintesis muncul pada bilangan gelombang 1665 cm-1
. Absorpsi untuk vibrasi
ikatan C=C yang khas pada aril muncul sebagai deretan empat pita pada bilangan
gelombang antara 1603-1487 cm-1
. Selanjutnya untuk vibrasi ulur C-H pada aril
muncul pita serapan dengan intensitas lemah pada bilangan gelombang 3000 cm-1
.
Vibrasi tekuk ikatan =C-H pada molekul target memunculkan pita pada bilangan
gelombang 916,5 cm-1
. Sedangkan vibrasi ulur C-O-C gugus metoksi (O-CH3)
pada senyawa target muncul dengan intensitas kuat pada bilangan gelombang
1171 cm-1
.
4.3.3 Analisis spektroskopi masa
Senyawa target baru yang terbentuk dianalisis menggunakan spektroskopi
masa (spektrum MS senyawa hasil sintesis (5) tertera pada Lampiran 5). Analisis
ini digunakan untuk mengetahui berat molekul dari senyawa target. Berdasarkan
hasil spektrum MS [M+H]+ , didapatkan puncak ion molekul sebesar 410 m/z.
37

li
Dengan demikian dapat diprediksi bahwa senyawa target memiliki berat molekul
sebesar 409.
4.3.4 Analisis spektroskopi resonansi magnetik inti
Spektrum RMI proton menunjukkan 8 sinyal yang muncul pada
pergeseran kimia δ 2,3 ; 3,6; 3,78; 3,79; 6,75; 6,83; 6,87; dan 7,99 ppm (spektrum
tertera pada Lampiran 6). Proton pada gugus karbonil α,β-tak jenuh muncul pada
pergeseran kimia δ 7,99 (2H, s). Sinyal ini memiliki integrasi 2H sehingga
diperkirakan pada pergeseran kimia tersebut terdapat dua buah proton yang
identik (berada pada lingkungan kimia yang sama). Sinyal ini muncul pada
pergeseran kimia yang paling deshielding sebab kerapatan elektron pada posisi β
menjadi lebih kecil akibat adanya resonansi. Pada gugus aromatis masing-masing
terdapat tiga buah proton yang terdistribusi pada pergeseran kimia δ (ppm): 6,75
(2H, d, J3=3,25); 6,83 (2H, d, J2=9,1); dan 6,87 (2H, dd, J3=3,25, J2=9,1) .
Masing-masing sinyal muncul dengan integrasi 2H sehingga senyawa target
diprediksi memiliki dua buah gugus aromatis yang identik. Dari sinyal-sinyal
tersebut dapat disimpulkan bahwa senyawa ini memiliki dua unit aromatis yang
identik seperti pada Gambar 4.1 :
Hb Hc
Ha
Gambar 4.1 Unit aromatis senyawa target
Adanya gugus metoksi (-OCH3) ditandai dengan munculnya sinyal pada
pergeseran kimia δ 3,79 (6H, s) dan 3,78 (6H, s). Kedua sinyal ini muncul dengan
intensitas tinggi dan masing-masing memiliki integrasi 6H, yang mengindikasikan
38

lii
bahwa adanya dua buah gugus metoksi yang identik. Sinyal yang
mengindikasikan adanya gugus N-CH3 muncul pada pergeseran kimia δ 2,37 ppm
(3H, s). Sedangkan unit CH2 pada gugus N-metil piperidin-4-on ditandai dengan
munculnya sinyal pada pergeseran kimia δ 3,65 ppm (4H,s). Sinyal ini memiliki
intensitas tinggi dan menunjukkan jumlah proton dua kali lipatnya, sehingga
diperkirakan terdapat dua metilen yang identik. Berdasarkan spektrum RMI
proton senyawa hasil sintesis, diperkirakan memiliki struktur sebagai berikut :
N
OO
O
O
OC
H3C
H3C
CH3
CH3
H H
H
H H H
H
H
H H
H2,37
3,65
3,79
6,7
6,83
6,87
7,99
2,372,37
6,87
6,83
6,7
7,99
3,65
3,79 3,79
3,79
Gambar 4.2 Prediksi struktur senyawa berdasarkan spektrum RMI proton
Spektrum RMI karbon terdapat 12 sinyal yang muncul pada masing-
masing pergeseran kimia 45,72; 55,79; 56,23; 57,18; 111,9; 114,9; 116,49;
125,36, 132,56; 133,46; 153,0; dan 186,97 ppm. Total atom karbon yang
teridentifikasi adalah 24 buah dengan rincian : 9 buah atom C kuartener, 8 buah C
tersier, 2 buah atom C sekunder, dan 5 buah atom C primer. Atom C kuartener
pada karbonil muncul pada pergeseran kimia yang paling deshielding yaitu 186,97
ppm. Sedangkan atom C kuartener pada gugus aromatis yang mengikat metoksi
muncul pada pergeseran kimia 153,0 ppm dengan intensitas tinggi. Hal itu
menunjukkan bahwa pada pergeseran kimia tersebut muncul 4 buah atom C yang
39

liii
hampir identik. Untuk atom C kuartener pada posisi α terhadap karbonil muncul
pada pergeseran kimia 132,56 ppm dengan integrasi menunjukkan adanya dua
atom karbon yang identik. Sedangkan untuk atom C tersier pada posisi β terhadap
karbonil muncul lebih deshielding pada pergeseran kimia 133,46 ppm. Sinyal
yang muncul pada pergeseran kimia 111,9; 114,9; dan 116,49 ppm merupakan
atom C tersier penyusun aromatis. Ketiga sinyal tersebut memiliki integrasi yang
menunjukkan munculnya dua atom karbon yang identik pada tiap pergeseran
kimia. Sedangkan sinyal yang mengindikasikan keberadaan C primer pada 4 buah
substituen metoksi (-OCH3) muncul pada pergeseran kimia hampir berdekatan
yaitu 57,18 dan 56,23 ppm. Pada pergeseran kimia 55,97 muncul sinyal yang
mengindikasikan adanya C sekunder (CH2-N-CH2). Sedangkan pada pergeseran
kimia yang paling shielding yaitu 45,72 ppm menunjukkan atom C primer pada
N-CH3. Berdasarkan spektrum RMI karbon senyawa hasil sintesis, diperkirakan
memiliki struktur sebagai berikut :
C
C
C
C
C
C C
C
C
N
C
C
C C
C
C
C
C
C
C
OO
O
O
OCH3
H3C
H3C
CH3
CH3
153,0 133,47
132,56125.36116,49
114,90111,90
57,18
56,23
55,97
45,72
186,97
153,0
153,0153,0
133,47
132,56 125.36
114,90
116,49
111,90
57,18
56,23
55,97
Gambar 4.3 Prediksi struktur senyawa berdasarkan spektrum RMI karbon
40

liv
4.4 Uji Aktivitas Antibakteri
Senyawa hasil sintesis kemudian diuji aktivitas antibakterinya terhadap
Staphylococcus aureus dan Escherichia coli dengan metode difusi menggunakan
kertas cakram. Pada metode difusi dengan kertas cakram hanya didapatkan data
kualitatif saja, yaitu ada atau tidaknya aktivitas antibakteri pada senyawa hasil
sintesis.
Senyawa hasil sintesis diuji aktivitas antibakterinya terhadap
Staphylococcus aureus dan Escherichia coli dengan 8 variasi konsentrasi yaitu 25,
50, 75, 100, 200, 300, 400, dan 500 ppm. Larutan uji masing-masing diteteskan
pada kertas cakram sebanyak 10 µL. Kertas cakram diletakkan pada media padat
Mueller Hinton Agar (MHA) yang telah diberi suspensi bakteri. Sebagai kontrol
negatif digunakan pelarut larutan uji DMSO 5% untuk memastikan bahwa pelarut
yang digunakan untuk mengencerkan senyawa uji tidak mempengaruhi aktivitas
antibakteri. Sedangkan sebagai kontrol positif digunakan tetrasiklin yang dibuat
dengan konsentrasi sama seperti larutan senyawa uji. Hal ini untuk
membandingkan zona hambat senyawa uji. Tetrasiklin dipilih karena memiliki
gugus karbonil α,β-tak jenuh pada strukturnya. Berikut ini adalah struktur
tetrasiklin.
Gambar 4.4 Struktur senyawa tetrasiklin
41

lv
Pengamatan dilakukan setelah waktu inkubasi selama 48 jam. Ada atau
tidaknya aktivitas antibakteri dapat dilihat dari daerah bening di sekitar kertas
cakram. Daerah bening tersebut merupakan zona yang pertumbuhan bakterinya
telah dihambat oleh senyawa uji. Hasil pengukuran zona hambat senyawa hasil
sintesis terhadap bakteri Staphylococcus aureus dan Escherichia coli dapat dilihat
pada tabel yang tertera pada Lampiran 7.
Dari data yang tertera pada tabel, menunjukkan bahwa pada bakteri
Staphylococcus aureus dan Escherichia coli yang menunjukkan daerah hambat
paling besar adalah pada konsentrasi 500 ppm. Jumlah atau konsentrasi zat
antimikroba sangat menentukan kehidupan mikroba yang terpapar. Jadi semakin
tinggi konsentrasi senyawa antimikroba, sel-sel mikroba yang terbunuh makin
banyak, sehingga semakin besar pula diameter daerah hambat di sekeliling kertas
cakram (Faradiani, 2010). Berikut ini adalah grafik zona hambat bakteri terhadap
konsentrasi larutan uji.
Gambar 4.5 Grafik zona hambat bakteri Staphylococcus aureus
42

lvi
Gambar 4.6 Grafik zona hambat bakteri Escherichia coli
Dari grafik terlihat bahwa diameter daerah hambat pada bakteri
Staphylococcus aureus tidak mengalami peningkatan yang signifikan seiring
dengan meningkatnya konsentrasi. Berbeda dengan Escherichia coli yang
mengalami peningkatan cukup signifikan seiring dengan meningkatnya
konsentrasi. Hal ini dapat dipengaruhi oleh perbedaan struktur penyusun dinding
sel kedua bakteri tersebut. Staphylococcus aureus merupakan kelompok bakteri
gram positif yang memiliki dinding sel lebih tebal yaitu 15-80 nm yang tersusun
atas peptidoglikan dengan ketebalan 40-50%. Sedangkan Escherichia coli
termasuk dalam kelompok bakteri gram negatif hanya memiliki ketebalan dinding
sel 10-15 nm dengan ketebalan peptidoglikan 5%. (Pelczar dan Chan, 1988).
Struktur dinding sel bakteri gram positif yang tebal dan mampat ini diduga
mempengaruhi interaksi senyawa dengan sel sehingga menyebabkan
Staphylococcus aureus lebih kebal dibandingkan dengan Escherichia coli.
43

lvii
Kemampuan senyawa uji dalam menghambat pertumbuhan bakteri juga
dipengaruhi oleh beberapa faktor, salah satunya adalah permeabilitas sel.
Fessenden and Fessenden (1986) mengatakan bahwa membran sel merupakan
membran yang terbentuk dari protein yang tertanam dan menyatu dengan suatu
lapisan rangkap (bilayer) molekul-molekul fosfogliserida dengan ujung
hidrofobiknya yang menghadap ke dalam dan ujung hidrofiliknya yang
menghadap keluar. Suatu senyawa yang bersifat polar akan sulit menembus
membran sel ini. Misalkan suatu senyawa antibakteri yang sangat berpotensi
ternyata hanya menghasilkan diameter daerah hambat kecil, semata-mata
dikarenakan ketidakmampuannya berdifusi ke dalam membran sel tersebut
(Rositasari, 2011).
44

lviii
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil dan pembahasan, maka didapatkan kesimpulan sebagai berikut :
1. Senyawa 3,5-bis-(4-hidroksi-3-metoksibenzilidin)-1-metilpiperidin-4-on
tidak dapat disintesis dari vanilin dan 1-metil-piperidin-4-on.
2. Senyawa 3,5-bis-(2,5-dimetoksibenzilidin)-1-metilpiperidin-4-on dapat
disintesis dari bahan dasar 2,5-dimetoksibenzaldehid dan 1-metil-
piperidin-4-on.
3. Senyawa target memiliki bioaktivitas sebagai antibakteri terhadap bakteri
Staphylococcus aureus dan Escherichia coli.
5.2 Saran
1. Perlu dilakukan identifikasi sifat bahan dasar sebelum melakukan sintesis
untuk meminimalkan terjadinya kesalahan pada proses sintesis.
2. Perlu dilakukan penelitian lebih lanjut tentang aktivitas senyawa target
sebagai antibakteri agar dapat diketahui nilai MIC (Minimum Inhibit
Concentration) terhadap bakteri gram positif dan negatif.
45

lix
DAFTAR PUSTAKA
Bailey, W. R., and Scott, E. G., 2002, Diagnotic Microbiology, 11th
Ed, The CV
Mosby Company, Saint Louis.
Chen, Z. H., Zheng, C. J., Sun, L. P., Piao, H. R., 2010, Synthesis of new chalcone
derivatives containing a rhodanine-3-acetic acid moiety with potential
anti-bacterial activity, European J.Med.Chem vol 45, p : 5739-5743.
Elliot, T., Worhhington, T., Osman, H., Gill, M., 2007, Medical Microbiology &
Infection, 4th
Ed, Blackwell Publishing Inc, Victoria.
Faradiani, N. A., 2010, Isolasi, Identifikasi, Senyawa Fenolik Rimpang Jahe
Merah Alpinia purpurata dan Uji Aktivita Antibakteri, Skripsi, Fakultas
Sains dan Teknologi, Universitas Airlangga, Surabaya.
Fessenden, R. J., and Fessenden, J. S., 1986, Kimia Organik, Edisi Ketiga,
Terjemahan oleh A.H. Pudjaatmaka, Erlangga, Jakarta.
Gritter, R.J., Robbit, J.M., dan Schwarting, A.F., 1991, Pengantar Kromatografi,
Edisi Kedua, Terjemahan oleh K. Padmawinata, ITB, Bandung.
Harborne, J. B., 1987, Metode Fitokimia, Penentuan Cara Modern Menganalisis
Tumbuhan, Terjemahan oleh K. Padmawinata dan Iwang Soediro, Terbitan
ke-2, ITB, Bandung
Hart. H., Craine. L., Hart. D., 2003 Kimia Organik Suatu Kuliah Singkat, edisi
kesebelas, Jakarta, Erlangga.
Iverson L., 1998, Study Guide and Problem Book Organic Chemistry, 2nd
Ed,
Saunders College, New York.
Jawetz, E., Melnick, J.L., and Adelberg, E.A., 1982, Review of Medical
Mirobiology, Lange Medical Publication, California.
Liu, X.L., Xu Y.J., Go M.L., 2007, Functionalized chalcones with basic
functionalities have antibacterial activity againts drug sensitive
Staphylococcus aureus, J. Med. Chem vol 43, p : 1681-1687.
Markham, K. R., 1988, Cara Mengidentifikasi Flafonoid, Terjemahan oleh K.
Padmawinata, Penerbit ITB, Bandung.
Mokle, S. S., Khansole, S. V., Patil, R. B., Vibhute, Y. B., 2010, Synthesis and
Antibacterial Activity of Some New Chalcones and Flavones Having 2-
Chloro-8-Metoxhyquinolinyl Moiety, Int J. Pharm & Bio Sci vol 1(1), p :
1-7.
46

lx
Mulja, M. H., dan Suharman, 1995, Analisis Instrumental, Airlangga University
Press, Surabaya.
Mulyati, S. E., 2009, Uji Aktivitas Antibakteri Etil Asetat Daun Ceremai
Phyllanthus acidus L. terhadap S.aureus dan E.coli dan
Bioautografinya, Skripsi, Fakultas Farmasi Universitas Muhammadiyah
Surakarta, Surakarta.
Patil, C. B., Mahajan, S. K., Katti, S. A., 2009, Chalcone: A Versatile Molecule,
J.Pharm Sci & Res vol 1(3), p : 11-22.
Pelczar, M.J., dan Chan, E.S.C., 1988, Dasar-dasar Mikrobiologi, Jilid 1, UI-
Press, Jakarta.
Prasad, Y.R., P. Rao, A.L., Rambabu, R., , 2008, Synthesis and Antimicrobial
Activity of Some Chalcone Derivatives, Int. J. Pharm Sci vol 5(3), p:
461-466.
Rahayu, H. A., 2005, Studi Hubungan Kuantitatif Sifat Kimia Fisika dengan
Aktivitas Antibakteri Turunan N-Benzoil Sefaleksin (Parameter Sifat
Lipofilik f Rekker, Elektronik Op Hammet dan Sterik B, Sterimol Verloop
terhadap Staphylococcus aureus ATCC29293), Skripsi, Fakultas Farmasi
Universitas Airlangga, Surabaya.
Rositasari, D., 2010, Sintesis Karakterisasi Senyawa Koordinasi Zn(II)-kurkumin
dan Uji Aktivitas Antibakteri terhadap Staphylococcus aureus, Skripsi,
Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya.
Sastrohamidjojo, H., dan Pranowo, H.D., 2009, Sintesis Senyawa Organik,
Erlangga, Jakarta.
Shriner, R. L., Hermann, C. K. F., Morril, T. C., Curtin, D. Y., Fuson, R. C., 1998,
The Systematic Identification of Organic Compound, 7th
Ed, John Wiley
and Sons, inc., New York
Silverstein, R.M., Bassler, G.C., and Morill, T.C., 1991, Spectrometri
Identification of Organic Compounds, 5th
Ed, John Willey and Sons, inc.,
New York.
Sudjadi, 1983, Penentuan Struktur Senyawa Organik, Penerbit Ghalia Indonesia,
Jakarta.
Suwito, H., Puspaningsih, N. N. T., 2010, Calkon Teranulasi Onkoprotein MDM2
pada Terapi Antikanker, Laporan Hibah Penelitian Strategi Nasional,
Unair.
Touchstone, J. C., 1992, Practice of Thin Layer Chromatography, 3rd
Ed, John
Willey and Sons, inc., New York.
47

lxi
Usman, H., Jalaludin, M. N., Harlim, T., Hakim E. H., Achmad, S. A., Syah, Y.
M., Latip, J., Said, I. M., 2006, Senyawa Kalkon Baru Bersifat Antibakteri
dari Tumbuhan Cryptocarya costata , J.MIPA vol 16(1), p : 37-40.
Watson, J., 1985, Introduction to Mass Spectrometry, 2nd
Ed, Raven Press, New
York.
Warren, S., 1995, Periptaan Sintesis Organik, Terjemahan oleh S.
Reksohadiprodjo, Gadjah Mada University Press, Yogyakarta.
Zonby, J. G., Starzyk, M. J., 1986, Screening Method for Recovery of Methicillin-
Resistant Staphylococcus aureus from Primary Plates, J. Clin. Microbiol
vol 24(2), p : 186-188.
48

lxii
LAMPIRAN
Lampiran 1
Spektrum IR Vanilin

lxiii
Lampiran 2
Spektrum MS Senyawa (4)

lxiv
Lampiran 3
Spektrum UV-Vis Senyawa (5)

lxv
Lampiran 4
Spektrum Inframerah Senyawa (5)

lxvi
Lampiran 5
Spektrum MS Senyawa (5)

lxvii
Lampiran 6
Spektra RMI Proton dan Karbon Senyawa (5)

lxviii

lxix
Lampiran 7
Diameter Zona Hambat Senyawa Uji terhadap Staphylococcus aureus
No. Senyawa Uji
(ppm)
Diameter daerah hambat (mm) Rata-rata
Replikasi I Replikasi II Replikasi III
1. 25 5,4 5,3 5,4 5,36
2. 50 5,1 5,2 5,4 5,23
3. 75 5,2 5,5 5,4 5,36
4. 100 5,4 5,5 5,5 5,46
5. 200 5,1 5,4 5,2 5,23
6. 300 5,2 5,5 5,1 5,26
7. 400 6,5 5,6 5,5 5,86
8. 500 6,5 5,69 5,59 5,93
9. Kontrol(-) 5,0 5,0 5,0 5,0
10. Kontrol(+)
100 ppm
7,3 7,07 6,4 6,92
11. Kontrol(+)
500 ppm
11,4 12,2 11,3 11,63

lxx
Lampiran 8
Diameter Zona Hambat Senyawa Uji terhadap Escherichia coli
No. Senyawa Uji
(ppm)
Diameter daerah hambat (mm) Rata-rata
Replikasi I Replikasi II Replikasi III
1. 25 5,3 6,5 5,3 5,7
2. 50 6,3 6,3 6,1 6,23
3. 75 7,1 6,4 7,1 6,86
4. 100 7,3 7,4 7,2 7,3
5. 200 7,4 7,15 6,35 6,96
6. 300 8,3 7,35 7,45 7,7
7. 400 8,3 8,25 8,3 8,28
8. 500 8,4 8,1 8,4 8,3
9. Kontrol (-) 5,0 5,0 5,0 5,0
10. Kontrol(+)
100 ppm
7,5 7,2 7,4 7,36
11. Kontrol(+)
500 ppm
9,15 9,1 9,4 9,22