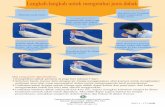
Pemeriksaan dahak
-
Upload
joni-iswanto -
Category
Documents
-
view
4.421 -
download
2
Transcript of Pemeriksaan dahak

PANDUAN
PEMERIKSAAN MIKROSKOPIS DAHAK

PEMERIKSAAN DAHAKYANG BERKUALITAS
A. PENGUMPULAN DAHAK
B. PEMBUATAN SEDIAAN APUS
E. PEWARNAAN SEDIAAN APUS
G. PEMBACAAN SEDIAAN APUS
I. PEMELIHARAAN MIKROSKOP
F. LAIN-LAIN

BAGIAN A
PENGUMPULAN DAHAK

URUTAN PENGUMPULAN DAHAK:• Petugas Poliklinik mengisi Formulir Permohonan
Pemeriksaan dahak (TB05) bagian atas utk dibawah pasien ke Lab
• Petugas Lab mendaftarkan / menuliskan nama pasien dalam buku TB06 sekaligus utk pemberiaan nomor identitas sediaan.
• Nomor identitas sediaan tsb ditulis pada badan pot dahak yg bersih kemudian pot tsb diberikan kepada pasien; Petugas menjelaskan bagaimana cara pengeluaran dahak yg baik; bila perlu dampingi pasien ybs.
• Dahak yg diterima dari pasien perlu diperiksa kualitasnya (bukan air liur) dan jumlahnya cukup (5cc)
• Letakkan specimen dahak tsb ditempat yg terlindung dari cahaya matahari langsung.


BAGIAN B
CARA MEMBUAT APUSAN DAHAK

URUTAN PEMBUATAN SEDIAAN APUS:
• Sediakan kaca sediaan yg baru & bersih
• Beri nomor identitas sediaan pada kaca sediaan tsb seperti nomor yg tertera di badan pot dahak
• Buat olesan dahak yg rata dgn ukuran 2x3 cm diatas kaca sediaan (jangan terlalu tebal – jangan terlalu tipis)
• Biarkan sediaan apus tsb kering sendiri di udara
• Setelah kering lakukan fiksasi sediaan diatas nyala api spiritus
• Simpan sediaan yg telah difiksasi tsb dalam kotak sediaan bersama Form TB05 dari pasien tsb
• Untuk PS sediaan2 yg telah difiksasi tsb dikirim ke PRM setiap minggu sekali untuk diwarnai & dibaca.

TULIS NOMOR IDENTITAS SEDIAAN
SESUAI BPN
CONTOH: 02/15/237A






BAGIAN C
PEWARNAAN SEDIAAN DAHAK

URUTAN PEWARNAAN ZHIEL NEELSEN:
• Letakkan sediaan yg telah difiksasi diatas rak (apusan menghadap keatas, ada jarak atar sediaan)
• Genangi dgn larutan.Carbol Fuchsin 0,3% (menutup seluruh kaca sediaan)
• Panaskan dgn nyala api spiritus (sampai menguap, jangan sampai mendidih)
• Diamkan minimal 5 menit
• Bilas dgn air mengalir pelan (sampai warna merah terbuang)
• Cuci dgn lar. Asam Alkohol 3% (sampai warna merah fuchsin hilang)

URUTAN PEWARNAAN ZHIEL NEELSEN(LANJUTAN):
• Bilas dgn air mengalir pelan
• Genangi dgn larutan Methylen Blue 0,3%
• Diamkan 20 - 30 detik
• Bilas dgn alir mengalir pelan
• Keringkan sediaan diatas rak pengiring diudara terbuka (jangan dibawah sinar matahari langsung)
• Sediaan yg sudah kering siap diperiksa dgn mikroskop binokuler.

PERLENGKAPAN YG DIBUTUHKANUTK PEWARNAAN SEDIAAN













BAGIAN D
PEMBACAAN SEDIAAN APUSAN DAHAK










NEGATIF PALSU(dilaporkan NEG tapi sebetulnya POS)
KONSEKUENSI:• Penderita TBC tdk diobati dgn akibat penyakit terus berlanjut, terjadi penularan atau
penderita meninggal• Pengobatan tahap intensif menjadi tdk lengkap, dgn akibat pengobatan tdk memadai dan
berpotensi menyebabkan terjadinya resisten terhadap obat
PENCEGAHAN:• Beri label pada pot dahak, sediaan dan form2 lab dgn teliti• Spesimen harus mengandung dahak dan bukan air liur• Pilih bagian purulen utk membuat apusan• Pembuatan apusan – ditengah, tdk terlalu tebal atau terlalu tipis, ukuran 3 x 2 Cm• Panasi carbol fuchsin sampai keluar uap, jangan sampai mendidih• Pewarnaan dgn carbol fuchsin – minimal 5 menit• Pencucian dgn asam alkohol (utk dekolorisasi) – sampai tdk ada lagi warna carbol fuchsin
yg keluar dari sediaan – maksimum 3 menit• Kontra warna dgn methylen blue – maksimum 30 detik• Mikroskop harus dalam keadaan baik, lensa2 dlm keadaan bersih• Uji kualitas reagens harus dilakukan secara teratur• Periksa nomor Reg Lab, cocokan dgn Form Permohonan Lab (TB.05) sebelum mencatat
hasil pemeriksaanJANGAN TERGESA-GESA,
PERIKSA APUSAN DAHAK SELAMA MINIMAL 5 MENIT SEBELUM MELAPORKAN HASIL NEGATIF

POSITIF PALSU(dilaporkan POS tapi sebetulnya NEG)
KONSEKUENSI:• Penderita mendapat pengobatan yang tidak perlu• Pengobatan diberikan lebih lama dari yang dibutuhkan• Terbuangnya obat-obatan
PENCEGAHAN:• Pastikan petugas laboratorium dapat mengenali BTA dgn baik• Beri label pada pot dahak, sediaan dan formulir2 lab dgn teliti• Selalu gunakan kaca sediaan baru yang tidak bergores• Gunakan tangkai bambu / lidi hanya sekali pakai• Jangan biarkan carbol fuchsin mengering diatas sediaan• Lakukan pencucian dgn asam alkohol (dekolorisasi) dgn baik• Aplikator minyak imersi tdk boleh menyentuh sediaan• Mikroskop harus terawat baik, lensa2 dlm keadaan bersih, dan
disimpan dgn benar• Lakukan uji kualitas reagens secara teratur• Periksa nomor Reg Lab, cocokan dgn Form Permohonan Lab
(TB.05) sebelum mencatat hasil pemeriksaan

BAGIAN E
PEMELIHARAAN MIKROSKOP






Beberapa bahan pembersih dapat merusak lensa setelah digunakan beberapa waktu
XXXylol
√XAseton / keton
√XBenzene / bensin
√XAlkohol
√√Ethyl eter / alkohol (80/20)
√√Rekomendasi pabrik
Penggunaan sekali-sekali
Penggunaan jangka panjangBahan Pembersih

BAGIAN F
LAIN-LAIN

MINYAK IMERSI – UJI SEDERHANA



Sunrise at Toba Lake
Terima Kasih
Semoga Bermanfaat