Metalli Ceramici Polimeri -...
Transcript of Metalli Ceramici Polimeri -...
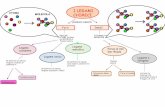
(a) Legami atomici primari o forti
•legame ionico
•legame covalente
•legame metallico
(b) Legami atomici e molecolari secondari o deboli
•legame di Van der Waals
•legame idrogeno
Forza di legame anione-catione
4pe0 a2
Z1Z2 e2
Fatt= - Frep= - nb
a(n+1)
Fnetta=Fatt + Frep
e = 1.60 x 10-19 C
e0 = 8.85 x 10-12 C2/(N m2)
+ -
dipolo atomico fluttuante
- +
dipolo atomico indotto
Legami secondari:
interazione dipolo-dipolo indotto in gas nobili
Legami secondari:
interazione dipolo-dipolo in molecole polari
H2O 1.84 debey
HCl 1.03 debey
NH3 1.46 debey
Struttura dei materiali
Solidi cristallini trasposizione regolare e ripetitiva nello spazio di una
unità strutturale di base (cella elementare o cella unitaria);
monocristallini e policristallini
Strutture cristalline sono suddivise in gruppi (sistemi cristallini) in
base alla geometria della cella unitaria, indipendentemente dalla
posizione degli atomi all'interno della cella.
I sistemi cristallini sono completamente descritti da
6 parametri reticolari: a, b, c, a, b, g
Sistemi cristallini
solido cristallino cella unitaria
sistema di coordinate (x, y, z):
origine in un vertice della cella
assi coincidono gli spigoli della cella
cubico
triclino esagonale
ortorombico
romboedrico
monoclino
tetragonale
7 sistemi cristallini
14 Reticoli di Bravais
(a) cubica a facce centrate (CFC) Cu, Ni, Ag, Au, Fe g, ...
(b) cubica a corpo centrato (CCC)
Fe a, Cr, W, Mo...
(c) esagonale compatta (EC) Zn, Cd, Co, Ti...
Materiali metallici
Cubica a facce centrate (CFC)
4 atomi per cella
12 numero di coordinazione
0.74 fattore di compattazione atomica
Esercizio 1
Calcolare il fattore di compattazione atomica (FCA) per la
cella elementare CFC, assumendo gli atomi sferici.
FCA = volume atomi per cella elementare CFC
volume della cella CFC
Esercizio 2
Il rame ha struttura CFC. Sapendo che il peso atomico è
63.54 g/mole ed il raggio atomico 0.1278 nm, calcolare la densità del
rame.
Cubica a corpo centrato (CCC)
2 numero di atomi per cella
8 numero di coordinazione
68 % fattore di compattazione atomica
Esercizio 3
Il Fe a 20 °C ha struttura CCC. Calcolare la costante reticolare a
della cella elementare del ferro, sapendo che il raggio atomico
del ferro è pari a 0.124 nm.
Esercizio 4
Calcolare il fattore di compattazione atomica (FCA) per la
cella elementare CCC, assumendo gli atomi sferici.
Esercizio 5
Il Mo ha struttura CCC, densità 10.2 g/cm3 e peso atomico 95,94 g/mole.
Calcolare il raggio atomico ed il fattore di compattazione atomica (FCA)
Esagonale compatta (EC)
6 numero di atomi per cella
12 numero di coordinazione
0.74 fattore di compattazione atomica
1.633 valore teorico di c/a
Esercizio 6
Calcolare il volume della cella elementare esagonale compatta (EC)
dello Zn sapendo che a=0.2665 nm e c=0.4947 nm.