Fisiologi ginjal
-
Upload
zulia-ahmad-burhani -
Category
Documents
-
view
92 -
download
1
description
Transcript of Fisiologi ginjal

Filtrasi glomerulus
Filtrasi glomerular melibatkan ultrafiltrasi plasma. Istilah ini mencerminkan fakta bahwa penghalang filtrasi glomerulus adalah saringan molekul yang sangat halus yang memungkinkan penyaringan molekul kecil tapi membatasi bagian dari makromolekul (misalnya, protein plasma).
The Barrier Glomerular Filtration Memiliki Tiga Lapisan
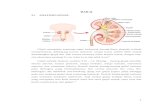
Ultrafiltrasi plasma melewati glomerulus dari kapiler darah ke dalam ruang kapsul Bowman melalui filtrasi glomerulus penghalang (Gambar 23.13). Penghalang ini terdiri dari tiga lapisan. Yang pertama, endotelium kapiler, adalah disebut fenestra lamina karena mengandung pori-pori atau jendela (fenestrae). Pada sekitar 50 sampai 100 nm diameter, ini pori-pori yang terlalu besar untuk membatasi bagian dari protein plasma. Lapisan kedua, membran basal, terdiri dari meshwork fibril halus tertanam dalam matriks seperti gel. Lapisan ketiga terdiri dari podocytes, yang merupakan lapisan visceral kapsul Bowman. Podocytes ("Sel kaki") adalah sel-sel epitel dengan ekstensi yang mengakhiri dalam proses kaki, yang beristirahat di lapisan luar dari basement membran (lihat Gambar. 23,13). Ruang antara proses kaki yang berdekatan, yang disebut pori-pori celah, adalah sekitar 20 nm lebar dan dijembatani oleh diafragma celah filtrasi. Kunci komponen diafragma adalah molekul yang disebut nefron, yang membentuk struktur ritsleting-seperti; antara Prongs dari ritsleting pori-pori persegi panjang. Nefron adalah bermutasi pada sindrom nefrotik kongenital, langka, mewarisi kondisi yang ditandai dengan penyaringan berlebihan plasma protein. The filtrat glomerular biasanya mengambil ekstraselular rute, melalui lubang di sel endotel lapisan, membran basal, dan pori-pori yang berdekatan antara nefron molekul.
Ukuran, Bentuk, dan Charge Listrik Mempengaruhi yang Filterability makromolekul
Sifat permeabilitas filtrasi glomerular penghalang telah dipelajari dengan menentukan bagaimana molekul baik ukuran yang berbeda melewatinya. 23,1 daftar beberapa Tabel molekul yang telah diuji. Jari-jari molekul yang dihitung dari koefisien difusi. Konsentrasi molekul dalam cairan filtrat glomerular (dikumpulkan dari Kapsul Bowman) dibandingkan dengan konsentrasi dalam plasma air. Sebuah rasio 1 menunjukkan filterability lengkap, dan rasio nol menunjukkan pengecualian lengkap oleh filtrasi glomerulus penghalang. Ukuran molekul merupakan faktor penting yang mempengaruhi filterability. Semua molekul dengan bobot kurang dari 10.000 secara bebas filterable, asalkan mereka tidak terikat pada protein plasma. Molekul dengan bobot lebih besar dari 10.000 Pengalaman lebih pembatasan perjalanan melalui filtrasi glomerular penghalang. Sangat besar molekul (misalnya, berat molekul, 100.000) tidak bisa melewati sama sekali. Kebanyakan protein plasma adalah molekul besar, sehingga mereka tidak lumayan disaring. Dari studi dengan ukuran molekul yang berbeda, telah menghitung bahwa penghalang filtrasi glomerulus berperilaku sebagai meskipun yang ditembus oleh pori-pori berbentuk silindrik dari sekitar 7,5 sampai 10 nm diameter. Namun, tak seorang pun pernah melihat pori-pori ukuran ini di mikrograf elektron dari filtrasi glomerulus penghalang. Bentuk molekul mempengaruhi filterability makromolekul. Untuk berat molekul tertentu, yang ramping dan fleksibel molekul akan melewati penghalang filtrasi glomerular lebih mudah daripada molekul, bola nondeformable. Muatan listrik mempengaruhi bagian makromolekul melalui penghalang filtrasi glomerulus karena penghalang beruang muatan negatif tetap. Endotel glomerulus sel dan podocytes memiliki permukaan bermuatan negatif mantel (glycocalyx), dan membran basal glomerulus mengandung asam sialat bermuatan negatif, sialoproteins, dan heparan sulfat. Ini muatan negatif menghambat bagian ini makromolekul

bermuatan negatif oleh elektrostatik tolakan dan mendukung berjalannya bermuatan positif makromolekul oleh tarik elektrostatik. Hal ini didukung oleh temuan bahwa filterability dari dekstran yang terendah untuk anionik dekstran, menengah untuk netral dekstran, dan tertinggi untuk kationik dekstran (lihat Tabel 23.1).
Selain ukurannya yang besar molekul, negatif bersih muatan pada albumin serum pada pH fisiologis adalah penting Faktor yang mengurangi filterability nya. Dalam beberapa glomerulus penyakit, hilangnya muatan negatif tetap dari glomerulus yang penghalang filtrasi menyebabkan filtrasi peningkatan albumin serum. Proteinuria, jumlah abnormal protein dalam urin, hasil. Proteinuria merupakan ciri khas penyakit glomerular (Lihat Kotak Fokus Klinis 23,2 dan Studi Kasus).
Lapisan penghalang filtrasi glomerulus terutama bertanggung jawab untuk membatasi filtrasi makromolekul adalah menjadi bahan perdebatan. Membran basal mungkin penghalang ukuran-selektif utama, dan diafragma celah filtrasi membentuk penghalang kedua. Hambatan elektrostatik utama mungkin adalah lapisan yang paling dekat dengan lumen kapiler, fenestra lamina dan bagian terdalam dari basement membran.
GFR Apakah Ditentukan oleh Starling Forces
Laju filtrasi glomerulus tergantung pada keseimbangan hidrostatik dan tekanan osmotik koloid bertindak seluruh filtrasi glomerulus penghalang, pasukan Starling (lihat Bab 16), karena itu, ditentukan oleh faktor-faktor yang sama yang mempengaruhi pergerakan cairan di kapiler pada umumnya.
Pada glomerulus, kekuatan pendorong untuk penyaringan cairan adalah hidrostatik glomerulus tekanan kapiler (PGC). Tekanan ini akhirnya tergantung pada pemompaan darah oleh jantung, tindakan yang meningkatkan tekanan darah di sisi arteri dari sirkulasi. Filtrasi ditentang oleh tekanan hidrostatik dalam ruang Bowman kapsul (PBS) dan oleh tekanan osmotik koloid (COP) yang diberikan oleh protein plasma dalam kapiler glomerulus darah. Karena filtrat glomerular hampir proteinfree, kita mengabaikan tekanan osmotik koloid cairan dalam Kapsula Bowman. The gradien tekanan ultrafiltrasi bersih (UP) adalah sama dengan perbedaan antara tekanan mendukung dan menentang filtrasi:
GFR? Kf? UP? Kf? (PGC PBS? COP) (10)
mana Kf adalah koefisien ultrafiltrasi glomerulus. Perkiraan
rata-rata, nilai normal untuk tekanan dalam manusia
ginjal: PGC, 55 mm Hg, PBS, 15 mm Hg, dan COP, 30
mm Hg. Dari nilai-nilai ini, kami menghitung ultrafiltrasi bersih
gradien tekanan Hg 10 mm?.
Profil Tekanan Seiring glomerulus yang
Kapiler Apakah Unusual
Gambar 23.14 menunjukkan bagaimana tekanan berubah seiring panjang

dari glomerulus kapiler, berbeda dengan yang terlihat dalam kapiler
di tempat tidur vaskular lainnya (dalam hal ini, otot rangka).
Perhatikan bahwa tekanan hidrostatik kapiler rata di
glomerulus jauh lebih tinggi (55 vs 25 mm Hg) daripada di
otot rangka kapiler. Juga, kapiler tekanan hidrostatik
sedikit (mungkin Hg 1 sampai 2 mm) yang membentang sepanjang penurunan
dari glomerulus yang kapiler glomerulus karena mengandung
banyak (30 sampai 50) kapiler loop secara paralel, sehingga perlawanan
untuk aliran darah dalam glomerulus sangat rendah. Dalam
otot rangka kapiler, ada resistensi yang lebih tinggi
ke aliran darah, yang mengakibatkan penurunan yang cukup dalam kapiler
hidrostatik tekanan dengan jarak. Akhirnya, perhatikan bahwa di
glomerulus, tekanan osmotik koloid meningkat secara substansial
sepanjang kapiler karena volume besar
filtrat (sekitar 20% dari aliran plasma masuk) adalah
didorong keluar dari kapiler dan protein tetap berada di
sirkulasi. Peningkatan tekanan osmotik koloid menentang
gerakan luar cairan.
Dalam otot rangka kapiler, tekanan osmotik koloid
hampir tidak berubah dengan jarak, karena cairan bergerak sedikit
melintasi dinding kapiler. Dalam otot "rata-rata" tulang
kapiler, filtrasi luar terjadi pada ujung arteri dan
penyerapan terjadi pada ujung vena. Di beberapa titik di sepanjang
otot rangka kapiler, tidak ada gerakan fluida bersih;
ini adalah titik yang disebut keseimbangan tekanan filtrasi.
Filtrasi kesetimbangan tekanan mungkin tidak tercapai
dalam glomerulus manusia normal, dengan kata lain,

filtrasi luar cairan mungkin terjadi sepanjang
glomerular kapiler.
Faktor beberapa Dapat Mempengaruhi GFR
GFR tergantung pada besaran istilah yang berbeda
dalam persamaan 10. Oleh karena itu, GFR bervariasi dengan perubahan Kf,
tekanan hidrostatik di kapiler glomerulus dan kapsul Bowman, dan glomerular kapiler yang osmotik koloid
tekanan. Faktor-faktor ini akan dibahas selanjutnya.
The Koefisien Ultrafiltrasi glomerulus. Glomerular ini
Koefisien ultrafiltrasi (Kf) adalah setara glomerular
koefisien filtrasi kapiler dihadapi dalam
Bab 16. Hal ini tergantung pada kedua konduktivitas hidrolik
(Permeabilitas cairan) dan luas permukaan filtrasi glomerular
penghalang. Pada penyakit ginjal kronik, fungsi glomeruli
hilang, mengarah ke pengurangan luas permukaan yang tersedia untuk filtrasi
dan penurunan GFR. Akut, berbagai obat-obatan dan hormon
muncul untuk mengubah glomerulus Kf dan, dengan demikian, mengubah GFR,
tetapi mekanisme tidak sepenuhnya dipahami.
Glomerular Tekanan Hidrostatik kapiler. Glomerulus
hidrostatik tekanan kapiler (PGC) adalah kekuatan pendorong bagi
filtrasi, itu tergantung pada tekanan darah arteri dan
resistensi pembuluh darah hulu dan hilir. Karena
autoregulasi, PGC dan GFR dipertahankan pada relatif
konstan nilai ketika tekanan darah arteri yang bervariasi
Dari 80 sampai 180 mm Hg. Di bawah tekanan dari 80 mm Hg,
Namun, PGC dan penurunan GFR, dan GFR berhenti pada darah
tekanan sekitar 40 sampai 50 mm Hg. Salah satu tanda-tanda klasik
syok hemoragik atau kardiogenik adalah tidak adanya urin

output, yang disebabkan oleh PGC memadai dan GFR.
Kaliber arteriol aferen dan eferen dapat
diubah oleh berbagai hormon dan dengan simpatik
stimulasi saraf, menyebabkan perubahan di PGC, glomerular
aliran darah, dan GFR. Beberapa hormon bertindak istimewa
pada arteriol aferen atau eferen. Aferen arteriol dilatasi
meningkatkan aliran darah glomerulus dan PGC dan, karena itu,
menghasilkan peningkatan GFR. Aferen arteriolar
penyempitan menghasilkan efek sebaliknya. Eferen
dilatasi arteriol meningkatkan aliran darah glomerulus tetapi
menyebabkan penurunan GFR karena PGC menurun. Penyempitan
dari arteriol eferen meningkatkan PGC dan menurun
aliran darah glomerulus. Dengan arteriol eferen sederhana
penyempitan, GFR meningkat karena peningkatan PGC.
Dengan penyempitan arteriolar eferen ekstrim, bagaimanapun,
GFR menurun karena penurunan tajam dalam
aliran darah glomerulus.
Tekanan hidrostatik dalam Kapsul Bowman. Hidrostatik
tekanan dalam kapsul Bowman (PBS) tergantung pada input
dari filtrat glomerular dan tingkat pemindahan cairan ini dengan
tubula. Tekanan ini menentang filtrasi. Hal ini juga menyediakan
kekuatan pendorong bagi gerakan cairan ke dalam lumen tubulus.
Jika ada obstruksi di mana saja di sepanjang saluran kemih
saluran-misalnya, batu, obstruksi saluran kemih, atau prostat
Pembesaran-maka tekanan hulu ke blok meningkat,
dan GFR akibatnya jatuh. Jika tubular reabsorpsi
air terhambat, tekanan dalam sistem tubular

meningkat karena seorang kepala tekanan yang meningkat diperlukan untuk
memaksa aliran volume besar melalui loop of Henle dan
mengumpulkan saluran. Akibatnya, peningkatan besar dalam urin
Output yang disebabkan oleh obat diuretik dapat berhubungan dengan
kecenderungan GFR jatuh.
Glomerular kapiler Koloid Tekanan Osmotik. Itu
COP menentang filtrasi glomerulus. Dilusi
plasma protein (misalnya, dengan infus intravena besar
volume saline isotonik) menurunkan COP plasma dan
menyebabkan peningkatan GFR. Bagian dari alasan glomerulus
aliran darah memiliki efek penting pada GFR adalah bahwa
Profil COP berubah sepanjang glomerulus yang
kapiler. Perhatikan, misalnya, apa yang akan terjadi jika
glomerulus aliran darah yang rendah. Penyaringan volume kecil
keluar dari kapiler glomerulus akan menyebabkan kenaikan tajam
COP di awal sepanjang glomerulus. Sebagai
Akibatnya, filtrasi akan segera berhenti dan GFR akan
menjadi rendah. Di sisi lain, aliran darah tinggi akan memungkinkan
tingkat tinggi pembentukan filtrat dengan kenaikan minimal
COP. Secara umum, aliran darah ginjal dan GFR tangan perubahan
di tangan, tetapi hubungan yang tepat antara GFR dan ginjal
aliran darah tergantung pada besarnya faktor lain
yang mempengaruhi GFR.
Faktor beberapa Kontribusi GFR Tinggi
di Ginjal Manusia
Tingkat ultrafiltrasi plasma di glomerulus ginjal
(180 L / hari) jauh melebihi di semua tempat tidur kapiler lainnya, untuk

beberapa alasan:
1) Koefisien filtrasi yang sangat tinggi dalam
glomeruli. Dibandingkan dengan kapiler lainnya, yang
glomerular kapiler berperilaku seolah-olah mereka memiliki lebih
pori-pori per satuan luas permukaan, akibatnya, mereka memiliki biasa
konduktivitas hidrolik tinggi. The glomerulus Total
filtrasi daerah penghalang besar, sekitar 2 m2.
2) tekanan hidrostatik kapiler lebih tinggi dalam
glomeruli daripada di kapiler lainnya.
3) Tingginya tingkat aliran darah ginjal membantu mempertahankan tinggi
GFR dengan membatasi peningkatan tekanan osmotik koloid, mendukung
filtrasi sepanjang seluruh panjang glomerular kapiler.
Singkatnya, filtrasi glomerulus yang tinggi karena
darah kapiler glomerulus terkena permukaan berpori besar
dan ada gradien tekanan tinggi transmural.
TRANSPORT DI tubulus proksimal
Filtrasi glomerulus merupakan proses yang agak nonselektif, karena
zat baik berguna dan limbah yang disaring. Sebaliknya,
transportasi tubular selektif, zat yang berbeda diangkut
dengan mekanisme yang berbeda. Beberapa zat diserap,
lain disekresikan, dan yang lain keduanya diserap kembali
dan disekresikan. Untuk sebagian besar, jumlah yang diekskresikan dalam
urin tergantung ukuran besar pada besarnya tubular
transportasi. Transportasi zat terlarut berbagai dan air berbeda
di segmen nefron berbagai. Di sini kita menggambarkan transportasi
sepanjang nefron dan mengumpulkan sistem saluran, mulai
dengan tubulus proksimal rumit.

Tubulus proksimal rumit terdiri dari 60% pertama
dari panjang tubulus proksimal. Karena proksimal
tubulus lurus tidak bisa diakses untuk belajar di vivo, yang paling kuantitatif
informasi tentang fungsi pada hewan hidup
terbatas pada bagian berbelit-belit. Studi tentang terisolasi
tubulus in vitro menunjukkan bahwa kedua segmen proksimal
tubulus secara fungsional serupa. Tubulus proksimal bertanggung jawab
untuk reabsorbing semua glukosa disaring dan
asam amino; reabsorbing fraksi terbesar dari disaring
Na?, K, Ca2??, Cl?, HCO3
, Dan? Air dan mengeluarkan berbagai
organik anion dan kation organik.
The tubuler berbelit-belit proksimal menyerap kembali
Sekitar 70% dari Air Disaring
Persentase air disaring diserap kembali di sepanjang
nefron telah ditentukan dengan mengukur derajat
yang inulin terkonsentrasi dalam cairan tubular, menggunakan ginjal
micropuncture teknik di laboratorium hewan. Sampel
cairan tubulus dari nefron permukaan dikumpulkan dan dianalisis,
dan tempat pengumpulan diidentifikasi oleh microdissection nefron.
Karena inulin disaring tetapi tidak diserap kembali oleh
tubulus ginjal, karena air yang diserap, inulin menjadi
semakin terkonsentrasi. Misalnya, jika 50% dari disaring
air diserap kembali oleh titik tertentu di sepanjang tubulus ini, [inulin]
dalam cairan tubular (TFIN) akan menjadi dua kali plasma [inulin]
(PIN). Persentase air disaring diserap oleh
tubulus sama dengan 100? (SNGFR VTF?) / SNGFR, di mana SN

(Nefron tunggal) GFR memberikan laju filtrasi air dan
V ˙
TF adalah laju aliran cairan tubulus pada titik tertentu. Itu
SNGFR dapat diukur dari bersihan inulin nefron tunggal
dan sama dengan TFIN V ˙? TF / PIN. Dari hubungan ini:
% Air disaring? [1? 1 / (TFIN / PIN)]? 100 (11)
Gambar 23.15 menunjukkan bagaimana TFIN / PIN perubahan rasio bersama
nefron pada tikus normal. Dalam cairan yang dikumpulkan dari Bowman
kapsul, [inulin] adalah identik dengan yang dalam plasma (inulin
secara bebas filterable), sehingga rasio konsentrasi dimulai pada 1.
Pada akhir tubulus proksimal rumit, rasio adalah
sedikit lebih tinggi dari 3, menunjukkan bahwa sekitar 70% dari disaring
air diserap kembali dalam tubulus proksimal rumit.
Rasionya adalah sekitar 5 pada awal tubulus distal, menunjukkan
bahwa 80% dari air yang disaring diserap sampai dengan
titik ini. Dari pengukuran tersebut, kita dapat menyimpulkan bahwa
lengkung Henle diserap 10% dari air yang disaring. Itu
urin / plasma inulin konsentrasi rasio ureter adalah
lebih besar dari 100, menunjukkan bahwa lebih dari 99% dari disaring
air diserap. Persentase ini tidak
tetap, mereka bisa sangat bervariasi, tergantung pada kondisi.
Cairan Tubular proksimal Apakah dasarnya
Isoosmotik ke Plasma
Sampel cairan yang dikumpulkan dari proksimal rumit
tubulus selalu dasarnya isoosmotik dengan plasma, konsekuensi
dari permeabilitas air yang tinggi dari segmen ini (Gambar
23.16). Secara keseluruhan, 70% zat terlarut disaring dan air diserap

sepanjang tubulus proksimal rumit.
Na? garam adalah zat terlarut osmotik aktif utama dalam
plasma dan filtrat glomerular. Karena tidak osmolalitas
tidak berubah lumayan dengan panjang tubulus proksimal, tidaklah mengherankan bahwa [Na?] juga tidak berubah di bawah biasa
kondisi.
Jika jumlah yang cukup zat terlarut adalah nonreabsorbed
hadir (misalnya, gula alkohol manitol), proksimal tubular
cairan [Na?] jatuh ke nilai-nilai di bawah konsentrasi plasma.
Ini adalah bukti bahwa Na? dapat diserap kembali terhadap konsentrasi
gradien dan merupakan proses aktif. Penurunan
cairan tubulus proksimal [Na?] meningkatkan difusi Na?
ke dalam lumen tubulus dan hasil dalam Na bersih berkurang? dan
air reabsorpsi, menyebabkan peningkatan ekskresi Na?
dan air, sebuah diuresis osmotik.
Dua utama anion, Cl? dan HCO3
, Menemani? Na?
dalam plasma dan filtrat glomerular. HCO3
? adalah istimewa
diserap sepanjang tubulus proksimal rumit, memimpin
untuk penurunan cairan tubulus [HCO3
],? Terutama karena H?
sekresi (lihat Bab 25). Cl The? tertinggal; sebagai air
diserap kembali oleh tubuh, [Cl?] naik (lihat Gambar. 23,16). Hasilnya adalah tubular
Cairan-to-plasma konsentrasi gradien yang nikmat
Cl? difusi keluar dari lumen tubulus. Outward gerakan
Cl? dalam tubulus proksimal rumit akhir menciptakan
kecil (1-2 mV), potensi lumen-positif transepitelial

perbedaan yang nikmat reabsorpsi pasif Na?.
Gambar 23.16 menunjukkan bahwa [K?] Hampir tidak berubah sepanjang
tubulus proksimal rumit. Jika K? tidak diserap,
konsentrasinya akan meningkat sebanyak itu dari inulin.
Fakta bahwa rasio konsentrasi untuk K? tetap tentang
1 di segmen nefron menunjukkan bahwa 70% dari K disaring?
yang diserap bersama dengan 70% dari air yang disaring.
Konsentrasi glukosa dan asam amino jatuh
tajam dalam tubulus proksimal rumit. Segmen nefron
dan tubulus lurus proksimal bertanggung jawab untuk
menyelesaikan reabsorpsi zat ini. Yang terpisah, khusus
mekanisme menyerap kembali glukosa dan asam amino yang berbeda.
Rasio konsentrasi untuk urea naik sepanjang proksimal
tubulus, tetapi tidak sebanyak rasio konsentrasi inulin karena
sekitar 50% dari urea disaring diserap kembali oleh tubuh. Itu
konsentrasi rasio untuk PAH di proksimal meningkatkan cairan tubulus
lebih curam daripada rasio konsentrasi inulin karena
sekresi PAH.
Singkatnya, meskipun osmolalitas (konsentrasi zat terlarut total)
tidak terdeteksi berubah sepanjang proksimal
tubulus berbelit-belit, jelas bahwa konsentrasi individu
zat terlarut bervariasi. Konsentrasi dari beberapa
zat jatuh (glukosa, asam amino, HCO3
?), Yang lain meningkat
(Inulin, urea, Cl?, PAH), dan yang lain tidak berubah
(Na, K??). Pada akhir tubulus proksimal rumit,
hanya sekitar sepertiga dari Na disaring, air?, dan K? tetap;

hampir semua glukosa disaring, asam amino, dan
HCO3
? telah diserap, dan zat terlarut beberapa ditakdirkan
untuk ekskresi (PAH, inulin, urea) telah terkonsentrasi di
cairan tubular.
Na? Reabsorpsi Apakah Angkatan Mengemudi Mayor
untuk Reabsorpsi Zat terlarut dan Air di
Proksimal tubuler
Gambar 23.17 adalah model dari sel tubulus proksimal. Na? masuk
sel dari lumen melintasi membran sel apikal
dan dipompa keluar melintasi membran sel basolateral
oleh Na / K?-ATPase.? The Na? dan menyertai
anion dan air tersebut kemudian diambil oleh darah sekitarnya
tubulus, dan disaring Na? garam dan air
kembali ke sirkulasi.
Pada membran sel luminal (brush border) dari
tubulus proksimal sel, Na? memasuki sel bawah dikombinasikan
gradien potensial listrik dan kimia. Bagian dalam
sel adalah tentang? 70 mV dibandingkan dengan cairan tubulus, dan intraseluler
[Na?] Adalah sekitar 30 sampai 40 mEq / L dibandingkan dengan
cairan tubulus konsentrasi sekitar 140 mEq / L. Na? masuk
ke dalam sel terjadi melalui cotransporter beberapa antiport
mekanisme. Na? yang diserap bersama-sama dengan glukosa,
asam amino, fosfat, dan larutan lain dengan cara terpisah,
spesifik cotransporters. Menuruni bukit (penuh semangat
berbicara) pergerakan Na? ke dalam sel drive menanjak
transportasi zat terlarut. Dengan kata lain, glukosa, amino

asam, fosfat, dan sebagainya diserap oleh sekunder
aktif transportasi. Na? juga diserap seluruh luminal
membran sel dalam pertukaran untuk H?. Na / H? exchanger,
antiporter, adalah juga merupakan transpor aktif sekunder
Mekanisme, pergerakan menurun dari Na? ke dalam sel
energi pada sekresi menanjak H? ke lumen. Ini
Mekanisme penting dalam pengasaman urin (lihat
Bab 25). Cl? dapat masuk ke dalam sel dengan cara luminal
membran sel Cl?-basa (formate atau oksalat) exchanger.
Setelah masuk sel, Na? dipompa keluar basolateral
side oleh Na kuat? / K?-ATPase yang terus intraseluler
[Na?] Rendah. Ini membran ATPase pompa tiga Na? di luar
dari sel dan dua K? ke dalam sel dan membagi satu molekul ATP
untuk setiap siklus pompa. K? dipompa ke dalam sel
berdifusi keluar membran sel basolateral sebagian besar melalui
K a? channel. Glukosa, asam amino, dan fosfat, terakumulasi dalam sel karena transpor aktif seluruh
membran sel luminal, keluar seluruh sel basolateral
membran dengan cara terpisah, Na-independen? difasilitasi
difusi mekanisme. HCO3
? keluar bersama-sama dengan Na? oleh
mekanisme elektrogenik, pembawa mengangkut tiga
HCO3
? untuk setiap Na?. Cl? dapat meninggalkan sel dengan cara suatu
elektrik netral K-Cl cotransporter.
Reabsorpsi Na? dan zat terlarut yang menyertainya menetapkan
gradien osmotik di tubulus proksimal
epitel yang merupakan kekuatan pendorong untuk air reabsorpsi.

Karena permeabilitas air epitel tubulus proksimal
sangat tinggi, hanya gradien kecil (beberapa
mOsm / kg H2O) diperlukan untuk memperhitungkan tingkat yang diamati
reabsorpsi air. Beberapa bukti eksperimental menunjukkan
bahwa cairan tubulus proksimal sedikit hypoosmotic untuk
plasma, karena perbedaan osmolalitas sangat kecil, masih
tepat untuk mempertimbangkan cairan pada dasarnya isoosmotik untuk
plasma. Air melintasi epitel tubulus proksimal
melalui sel melalui saluran air (aquaporin-1) di
membran sel dan antara sel-sel (persimpangan ketat dan
lateral yang interselular spasi).
Langkah terakhir dalam reabsorpsi keseluruhan zat terlarut dan
air adalah penyerapan oleh kapiler peritubular. Mekanisme ini
melibatkan pasukan Starling biasa yang beroperasi di seluruh
kapiler dinding. Ingatlah bahwa darah kapiler peritubular
sebelumnya disaring dalam glomeruli. Karena protein-
bebas filtrat disaring keluar dari glomerulus, yang [protein]
(Maka, koloid tekanan osmotik) darah dalam peritubular
kapiler tinggi, menyediakan pendorong penting
memaksa untuk penyerapan cairan diserap. Hidrostatik The
tekanan di kapiler peritubular (tekanan yang menentang
penyerapan cairan kapiler) yang rendah karena darah
telah melewati pembuluh resistensi hulu. Keseimbangan
tekanan bertindak di nikmat peritubular kapiler
penyerapan cairan diserap dari ruang interstisial
sekitar tubulus.
The tubuler proksimal mengeluarkan Ion Organik

Tubulus proksimal, bagian kedua berbelit-belit dan lurus,
mengeluarkan berbagai macam anion organik dan organik
kation (Tabel 23.2). Banyak dari zat ini endogen
senyawa, obat-obatan, atau racun. Anion organik yang
terutama karboksilat dan sulfonat (karboksilat dan sulfonat
asam dalam bentuk terprotonasi mereka). Sebuah muatan negatif pada
molekul tampaknya menjadi penting untuk sekresi ini
senyawa. Contoh anion organik aktif disekresikan
dalam tubulus proksimal termasuk penisilin dan PAH. Organik
transportasi anion menjadi jenuh pada plasma organik tinggi
anion konsentrasi (lihat Gambar. 23,9), dan anion organik
bersaing satu sama lain untuk sekresi.
Gambar 23.18 menunjukkan model sel untuk sekresi aktif.
Sel tubulus proksimal aktif mengambil PAH dari sisi darah dengan pertukaran untuk sel-ketoglutarat?. Pertukaran ini adalah
dimediasi oleh transporter anion organik (OAT) disebut
OAT1. Sel-sel menumpuk?-Ketoglutarat dari metabolisme
dan karena membran sel Na-dependent? dicarboxylate
transporter. PAH terakumulasi dalam sel-sel pada
konsentrasi tinggi dan kemudian bergerak menurun ke tubular
urin dalam mode elektrik netral, dengan bertukar
untuk anion anorganik (misalnya, Cl?) atau anion organik.
Kation organik terutama amina dan amonium
senyawa dan disekresikan oleh transporter lain. Masuk
ke dalam sel melintasi membran basolateral disukai oleh
potensial membran dalam negatif dan terjadi melalui difasilitasi
difusi, dimediasi oleh transporter kation organik
(OCT). Keluarnya kation organik di seluruh luminal

membran dicapai oleh kation organik / H?
antiporter (exchanger) dan didorong oleh lumen-sel ke-
[H?] Gradien didirikan oleh Na? / H? pertukaran. Itu
transporter untuk anion organik dan kation organik menunjukkan
substrat yang luas dan spesifisitas mencapai sekresi
berbagai macam senyawa kimia beragam.
Selain menjadi aktif disekresikan, beberapa organik
senyawa pasif berdifusi melintasi epitel tubular.
Anion organik dapat menerima H? dan kation organik dapat melepaskan
H?, Sehingga biaya mereka dipengaruhi oleh pH. The terionisasi
(Bermuatan) bentuk, jika lipid-larut, dapat berdifusi
melalui lapisan ganda lipid dari membran sel ke konsentrasi
gradien. The terionisasi (dibebankan) membentuk pasif
menembus membran sel dengan susah payah.
Perhatikan, misalnya, asam karboksilat probenesid
(PKa 3.4?). Senyawa ini disaring oleh glomeruli dan
disekresikan oleh tubulus proksimal. Ketika H? disekresi ke
urin tubular (lihat Bab 25), bentuk anionik (A?) adalah
dikonversi ke asam terionisasi (HA). Konsentrasi
asam terionisasi juga meningkat karena reabsorpsi air.
Sebuah gradien konsentrasi untuk pasif reabsorpsi
di dinding tubulus dibuat, dan jumlah yang cukup
probenesid secara pasif diserap. Hal ini terjadi di sebagian besar
bagian dari nefron, tetapi terutama pada mereka pH di mana
gradien yang terbesar dan di mana air telah mengakibatkan reabsorpsi
dalam konsentrasi terbesar (yaitu, mengumpulkan para
saluran). Ekskresi probenesid ditingkatkan dengan membuat

urin lebih basa (dengan pemberian NaHCO3) dan oleh
meningkatkan output urin (dengan meminum air).
Akhirnya, sebuah anion organik sedikit dan kation juga aktif
diserap. Sebagai contoh, asam urat baik dikeluarkan dan diserap
dalam tubulus proksimal. Biasanya, jumlah
asam urat diekskresikan sama dengan sekitar 10% dari urat disaring
asam, sehingga reabsorpsi mendominasi. Dalam gout, kadar plasma
asam urat yang meningkat. Salah satu pengobatan untuk gout adalah untuk mempromosikan
kemih ekskresi asam urat dengan pemberian obat
yang menghambat reabsorpsi tubular nya.
TUBULAR TRANSPORT DALAM LOOP DARI Henle
Lengkung Henle meliputi segmen yang berbeda dengan beberapa
berbeda struktural dan fungsional sifat. Seperti disebutkan sebelumnya,
tubulus proksimal lurus memiliki sifat transportasi
mirip dengan tubulus proksimal rumit. Itu
tipis menurun, naik tipis anggota badan naik, dan tebal
dari loop Henle semua permeabilitas tampilan yang berbeda dan
transportasi properti.
Terbesar dan Terkecil Limbs Berbeda
Permeabilitas di Air
Cairan tubulus memasuki lengkung Henle adalah isoosmotik untuk
plasma, namun cairan meninggalkan loop adalah jelas hypoosmotic.
Cairan yang dikumpulkan dari bagian awal dari distal
tubulus berbelit memiliki osmolalitas sekitar 100
mOsm / kg H2O, dibandingkan dengan 285 mOsm / kg H2O di
plasma karena zat terlarut lebih dari air diserap kembali oleh
lengkung Henle. Lengkung Henle menyerap kembali sekitar 20% dari

disaring Na?, 25% dari K disaring, 30% dari Ca2 disaring??,
65% dari Mg2 disaring, dan? 10% dari air yang disaring. The menurun
dahan loop of Henle (kecuali untuk terminal
sebagian) sangat air-permeabel. The ascending limb adalah
air kedap. Karena zat terlarut diserap bersama
anggota badan naik dan air tidak bisa mengikuti, cairan sepanjang
ascending ekstremitas menjadi lebih dan lebih encer. Endapan
zat terlarut (terutama Na? garam) dalam ruang interstisial
ginjal medula sangat penting dalam pengoperasian kemih yang
berkonsentrasi mekanisme.
The Membran Luminal your dari
Limb Ascending tebal Mengandung
Na-K-2Cl Cotransporter
Gambar 23.19 adalah model dari sel tungkai tebal menaik. Na?
memasuki sel melintasi membran sel luminal oleh elektrik
netral Na-K-2Cl cotransporter yang khusus
dihambat oleh bumetanide diuretik obat "loop" dan
furosemide. Gerakan menurun dari Na? ke dalam sel
hasil dalam transpor aktif sekunder satu K? dan dua
Cl?. Na? dipompa keluar membran sel basolateral oleh
Na kuat / K?-ATPase.? K? mendaur ulang kembali ke lumen
melalui K membran sel luminal? channel. Cl? daun
melalui sisi basolateral oleh cotransporter K-Cl atau Cl?
channel. Membran sel luminal didominasi permeabel
untuk k, dan? membran sel basolateral didominasi permeabel terhadap Cl?. Difusi ion ini keluar
sel menghasilkan perbedaan potensial transepitelial,
dengan lumen sekitar 6 mV? dibandingkan dengan interstisial

ruang di sekitar tubulus. Ini drive beda potensial
kecil kation (Na, K??, Ca2?, Mg2?, dan NH4
?) Dari
lumen, antara sel-sel. Epitel tubular sangat
kedap air, tidak ada air terukur
reabsorpsi sepanjang ekstremitas naik meskipun besar
transepitelial gradien tekanan osmotik.
TUBULAR TRANSPORT DI nefron distal
Nefron disebut distal meliputi segmen berbeda:
distal berbelit-belit tubulus, tubulus menghubungkan, dan
kortikal meduler, luar, dan mengumpulkan meduler batin
saluran (lihat Gambar. 23,2). Perhatikan bahwa nefron distal meliputi
sistem duktus pengumpul, yang, tegasnya, tidak
bagian dari nefron, tetapi dari perspektif fungsional, ini
dibenarkan. Transportasi di nefron distal berbeda dari yang
dalam tubulus proksimal dalam beberapa cara:
1) The nefron distal menyerap kembali jumlah yang lebih kecil
garam dan air. Biasanya, nefron menyerap kembali distal
9% dari Na disaring? dan 19% dari air yang disaring, dibandingkan
dengan 70% untuk kedua zat dalam proksimal rumit
tubulus.
2) The nefron distal dapat membangun gradien curam untuk
garam dan air. Sebagai contoh, [Na?] Dalam urin akhir
mungkin serendah 1 mEq / L (versus 140 mEq / L dalam plasma) dan
osmolalitas urin dapat hampir sepersepuluh yang dari
plasma. Sebaliknya, tubulus proksimal menyerap kembali Na? dan
air sepanjang gradien kecil, dan [Na?] dan osmolalitas

cairan tubulus yang biasanya dekat dengan yang plasma.
3) The nefron distal memiliki "ketat" epitel, sedangkan
tubulus proksimal memiliki "bocor" epitel (lihat Bab
2). Hal ini menjelaskan mengapa nefron distal dapat membangun curam
gradien untuk ion kecil dan air, sedangkan proksimal
tubulus tidak bisa.
4) Na? dan air reabsorpsi di tubulus proksimal
biasanya erat digabungkan karena epitel air permeabilitas
selalu tinggi. Sebaliknya, Na? dan air reabsorpsi
dapat uncoupled di nefron distal karena
permeabilitas air mungkin rendah dan variabel.
Reabsorpsi Proksimal keseluruhan dapat dicirikan sebagai
kasar operasi yang menyerap kembali dalam jumlah besar garam dan
air sepanjang gradien kecil. Sebaliknya, reabsorpsi distal
adalah proses yang lebih halus.
Saluran pengumpul berada di akhir dari sistem nefron,
dan apa yang terjadi di sana sangat menentukan ekskresi
Na, K??, H?, dan air. Transportasi di dalam mengumpulkan
saluran ini tersetel oleh hormon. Secara khusus,
aldosteron meningkat Na? reabsorpsi dan K? dan H? sekresi,
dan vasopresin arginine meningkatkan reabsorpsi air
di situs ini.
The Membran Luminal your dari distal
Tubuler berbelit Berisi Na-Cl
Cotransporter
Gambar 23.20 adalah model dari sel tubulus distal berbelit-belit. Di
segmen nefron, Na? dan Cl? diangkut dari

lumen ke dalam sel oleh cotransporter Na-Cl yang menghambat
oleh diuretik thiazide. Na? dipompa keluar basolateral
side oleh Na? / K?-ATPase. Air permeabilitas
tubulus distal berbelit-belit rendah dan tidak diubah oleh
arginin vasopressin.
The Duct Mengumpulkan Cortical Adalah Penting
Pengaturan situs K? Pengeluaran
Dalam keadaan normal, sebagian besar K diekskresikan?
berasal dari K? disekresikan oleh saluran pengumpul kortikal.
Dengan K besar? berlebih (misalnya, diet tinggi-K?), yang kortikal
mengumpulkan saluran dapat mengeluarkan K begitu banyak? bahwa lebih K? adalah
diekskresikan dari yang disaring. Dengan K parah? deplesi, yang
saluran pengumpul kortikal reabsorb K?.
K? sekresi tampaknya menjadi fungsi utama dari
mengumpulkan sel utama saluran (Gambar 23.21). K? sekresi melibatkan
aktif serapan oleh Na / K??-ATPase di basolateral
membran sel, diikuti dengan difusi K? melalui
K membran luminal? saluran. Difusi lahiriah K?
dari sel yang disukai oleh gradien konsentrasi dan menentang
oleh gradien listrik. Perhatikan bahwa gradien listrik
menentang keluar dari sel yang lebih kecil di seluruh luminal
membran sel dari seluruh sel basolateral
membran, mendukung pergerakan K? ke lumen lebih
daripada kembali ke dalam darah. Potensi membran sel luminal
Perbedaan rendah (misalnya, 20 mV, sel di dalam negatif)
karena membran ini memiliki Na tinggi? permeabilitas dan
depolarized oleh Na? menyebar ke dalam sel. Ingat bahwa

masuknya Na? ke dalam sel menyebabkan depolarisasi membran
(Lihat Bab 3).
Besarnya K? sekresi dipengaruhi oleh beberapa
faktor (lihat Gambar 23.21.):
1) Kegiatan Na membran basolateral / K?? -
ATPase adalah faktor kunci yang mempengaruhi sekresi, semakin besar
pompa aktivitas, semakin tinggi tingkat sekresi. Sebuah tinggi
plasma [K?] mempromosikan K? sekresi. Peningkatan jumlah
Na? dalam lumen duktus pengumpul (misalnya, akibat dari penghambatan
Na? reabsorpsi oleh obat diuretik loop) mengakibatkan peningkatan
masuknya Na? ke dalam sel utama, peningkatan aktivitas
dari Na / K?-ATPase?, dan meningkatkan K? sekresi.
2) Potensi lumen-negatif listrik transepitelial
mempromosikan K? sekresi. 3) Peningkatan permeabilitas membran sel luminal
untuk k? nikmat sekresi.
4) Sebuah aliran tinggi cairan tingkat melalui lumen duktus pengumpul
mempertahankan gradien konsentrasi sel-to-lumen,
yang mendukung K? sekresi.
Hormon aldosteron mempromosikan K? sekresi oleh
beberapa tindakan (lihat Bab 24).
Na? masuk ke dalam sel duct mengumpulkan adalah dengan difusi
Na melalui suatu? channel (lihat Gambar. 23.21). Saluran ini memiliki
telah kloning dan sekuensing dan dikenal sebagai ENaC, untuk epitel
natrium (Na) channel. Masuknya Na? melalui
saluran ini adalah tingkat-membatasi untuk Na keseluruhan? reabsorpsi
dan meningkat aldosteron.
Sel diselingi tersebar di antara mengumpulkan duct

Sel-sel utama, mereka penting dalam asam-basa transportasi (lihat
Bab 25). A H / K??-ATPase hadir dalam sel luminal
membran-diselingi? sel dan berkontribusi terhadap ginjal
K? konservasi ketika asupan K? kekurangan