Diagnóstico de Laboratorio de Malaria o Paludismo de paludismo... · Algunos hematíes infectados...
Transcript of Diagnóstico de Laboratorio de Malaria o Paludismo de paludismo... · Algunos hematíes infectados...

Diagnóstico de Laboratorio de Malaria o
Paludismo Dra. Mercedes Subirats
S. Microbiología. H. Carlos III
Dra. Rocío Martínez S. Microbiología. H. U. Puerta de Hierro-Majadahonda

Paludismo
4+1 tipos de Plasmodium que preferentemente afectan al Humano
P. falciparum
P. vivax
P. ovale
P. malariae
+1: P. knowlesi (parásito del
mono que aparece en zonas boscosas
de Sudeste asiático)

Fiebre Paludismo = Malaria
Toda fiebre en un paciente procedente del Trópico es PALUDISMO
mientras no se demuestre lo contrario
La principal enfermedad del viajero y
del inmigrante procedente de países tropicales

“ Paciente procedente de Guinea. Fiebre y sospecha de pielonefritis. Enviamos orina para cultivo”
Nuestra respuesta:
1. “Vale, de acuerdo”
2. “Vale, pero enviadnos también una gota gruesa para descartar malaria”
La existencia de un proceso que
justifique la fiebre NO EXCLUYE EL
PALUDISMO
¡URGENCIA!

Diagnóstico parasitológico
Diagnóstico directo:
Muestra: sangre periférica
Tinción de Giemsa o Field de la gota gruesa y extensión o frotis fino
Visualización del parásito
Identificación de la especie
Cuantificación de la parasitemia
Monitorización del tratamiento
Técnicas de diagnóstico rápido: Inmunocromatografía
Técnicas de biología molecular: PCR
Diagnóstico indirecto: Serología

Recogida de la muestra
¿Cuándo?
Extracción durante el pico febril
¿Cómo?
Digitopunción
Venopunción, tubo con EDTA (= Hemograma).

Gota gruesa: > sensibilidad
Sangre con EDTA: Extenderla lo suficiente para poder ver a través de ella las manecillas del reloj.
Sangre capilar: Extenderla durante 1 minuto para eliminar la fibrina.
Dejar secar 30’ antes de teñir.
Extensión: diagnóstico de especie

Diagnóstico microscópico
El “gold standard” es la Gota Gruesa. Ventajas Sensibilidad: detección 5-50 parásitos/µl (gota gruesa) Especificidad: eficaz al dar la especie y fase del ciclo (extensión) Información útil clínicamente: cuantificación de parasitemia,
especie y fase del ciclo Control del tratamiento (ojo: gametocitos sólo) Barato
Inconvenientes Entrenamiento y experiencia Buen microscopio y tinciones

A B
Solución A
Solución B
(se diluye a 1/5
para la extensión)
AGUA pH 7’2
TINCIÓN DE FIELD


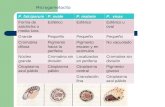
¿Cómo distinguimos las distintas especies?
Hematíe parasitado Tamaño
Presencia de granulaciones
Existencia de infecciones múltiples
Características del trofozoito Tamaño, forma y número de parásitos
Número de núcleos por anillo
Características del esquizonte Tamaño y forma
Número y disposición de los merozoitos
Forma y distribución del pigmento palúdico
Características de los gametocitos Tamaño y forma
Forma y distribución del pigmento palúdico

P. knowlesi Pv

P. falciparum
Aspecto de los hematíes:
Tamaño normal
Manchas de Maurer
Infecciones múltiples frecuentes
Infecta tanto los hematíes jóvenes como viejos.
Parasitemia puede ser >>2%
Trofozoitos:
Anillos jóvenes pequeños, delicados
1/6 del diámetro del hematíe
Frecuentemente con gránulos dobles de
cromatina
Algunos anillos en el borde del hematíe, forma
“accolé”

P. falciparum
Gametocitos:
Alargados o en forma de media luna o banana
Esquizontes: sólo en malaria cerebral
6-32 merozoitos (promedio 24)
Estadios encontrados en sangre periférica:
Anillos y/o gametocitos
Los pre-esquizontes y esquizontes se
desarrollan en los microcapilares
No se observan en sangre periférica
excepto en infecciones graves

Gota gruesa


Esquizontes de P falciparum secuestrados en
la microcirculación cerebral

Paludismo grave: P falciparum con esquizontes

P. malariae
Aspecto de los hematíes:
Tamaño normal o disminuido
Infecta a hematíes viejos.
Parasitemia normalmente < 1%
Raramente se observan puntos o manchas
de Ziemann
Trofozoitos:
Redondeados, compactos con citoplasma
denso, cromatina grande
Formas características:
Formas en “ojo de pájaro”
Trofozoitos en banda o acintados

P. malariae
Esquizontes:
6-12 merozoitos (promedio 8)
Esquizontes “en roseta” con el pigmento
palúdico en el centro
Gametocitos:
Redondo u ovalado, compacto. Casi ocupa
todo el hematíe
Estadios encontrados en sangre periférica:
Todos los estadios
Suelen observarse pocas formas “en anillo” o
gametocitos

P. malariae

P. vivax
Aspecto de los hematíes:
Tamaño aumentado o normal
Infecta hematíes jóvenes (reticulocitos).
Parasitemia normalmente <2%
Punteado de Schüffner: Punteado fino,
distribución uniforme en todo el hematíe
Presente en todos los estadios excepto formas
anulares iniciales
Trofozoitos:
Citoplasma irregular, anillo grueso ameboide,
aspecto difuso, irregular

Basofilia punctata
No hay parasito
No confundir

P. vivax
Esquizontes:
12-24 merozoitos (promedio 16).
Ocupa casi todo el hematíe
Gametocitos:
Redondo u ovalado. Casi ocupa todo el hematíe
Estadios encontrados en sangre periférica:
Todos los estadios
Amplia gama de fases visibles en un frotis

P. vivax

P. ovale
Aspecto de los hematíes:
Tamaño aumentado
Algunos hematíes infectados son ovales y/o
desflecados
Infecta hematíes jóvenes (reticulocitos).
Parasitemia normalmente < 2%
Punteado de Schüffner
Trofozoitos:
Redondeados, compactos, a veces ligeramente
ameboides
Los trofozoitos en desarrollo tienen una gran
masa cromatínica

P. ovale
Esquizontes:
6-14 merozoitos (promedio 8) rodeando al
pigmento malárico
Gametocitos:
Redondo u ovalado. Casi ocupa todo el
hematíe
Estadios encontrados en sangre
periférica:
Todos los estadios se pueden ver.
SINCRONIZACIÓN DE FASES: Todos son
trofozoítos o son esquizontes o son
gametocitos.
Se desincronizan cuando 2% parasitemia

Pre-esquizonte de P ovale


P. knowlesi
Aspecto de los hematíes:
Tamaño normal o disminuido
No son raras los eritrocitos
poliparasitados
Trofozoito:
Anillos jóvenes pequeños, delicados
1 o 2 puntos grandes de cromatina
Ocasionalmente, anillos en el borde del
hematíe, forma “accolé”
Trofozoito maduro:
Redondeados, compactos con
citoplasma denso y cromatina grande
Ocasionalmente trofozoitos en banda o
acintados

Esquizontes
P. knowlesi
Esquizontes:
Hasta 16 merozoitos
Esquizontes “en roseta” con el pigmento
palúdico en el centro
Gametocitos:
Redondo u ovalado, compacto. Casi ocupa
todo el hematíe
Estadios encontrados en sangre
periférica:
Todos los estadios

P. knowlesi
Trofozoito joven o anillo semejante al de P. falciparum
P. knowlesi P. falciparum

P. knowlesi Trofozoito maduro, esquizonte y gametocitos
semejantes a P. malariae
P. knowlesi
P. malariae

Trofozoitos
P. vivax
P. falciparum P. malariae
P. ovale

Esquizontes
P. vivax
P. falciparum P. malariae
P. ovale

Gametocitos
P. vivax
P. falciparum P. malariae
P. ovale

Cálculo de la parasitemia
Calcular el porcentaje de hematíes parasitados (en extensión fina):
1. Con el objetivo de inmersión, seleccionar un área de la extensión fina con una densidad aproximada de 100 hematíes/campo.
2. Contar 10 campos.
3. Dividir por 10 para calcular el porcentaje (%) de hematíes parasitados.

Inmunocromatografía Principio
Contiene anticuerpos monoclonales frente a antígenos especificos del Plasmodium
Diferencian P falciparum del resto de las especies, algunas diferencian P. vivax, pero no pueden diferenciar entre las demás
Antígenos de Paludismo detectados:
Enzimas metabólicas que se encuentran en todas las especies:
1. pLactato deshidrogenasa (pLDH)
2. Aldolasa
Proteína Rica en Histidina 2 (HRP 2) se encuentra sólo
en P falciparum

p-ALDOLASA y p-LDH
Enzimas metabólicas parasitarias que intervienen en la glucolisis
p-Aldolasa Dihidroxiacetona-P
Fructosa-1,6-diP +
Gliceraldehido-3-P
p-LDH
Lactato Piruvato

Inmunocromatografía Ventajas:
Fáciles de realizar
Rápidas
No precisan microscopio
No precisan personal entrenado
Útiles en el diagnóstico en gestantes debido al secuestro placentario de los parásitos (HRP-2)
Desventajas:
Falso N si parasitemia baja No miden la parasitemia Bien para P. falciparum. OJO:
Cuidado con P.ovale y con los P. malariae que no los detecta bien.
No distinguen todas especies Persisten(+) tras infección
aguda y tras tratamiento Falso P con factor reumatoide Precio alto Evitar humedad (Tª 2-30ºC)

Negativo Pl. no falciparum Pl. falciparum o
infección mixta
RESULTADOS
pLDH
o
Aldolasa
HRP 2

Inmunocromatografía RDT (rapid test diagnosis)


PCR
Ventajas:
5 parásitos / µl (0,0001%)
Identificación de especie
Mutaciones de resistencia
S y E ~ 100%
Inconvenientes:
Precio
Laboriosa
Resultado en horas
No distingue entre parásitos viables y no viables
Infecciones mixtas, monitorizar respuesta al tratamiento
y diagnóstico temprano de fallo terapéutico

Sensibilidad métodos diagnóstico malaria
• Gota gruesa: 5-100 parásitos/μL
• Extensión fina: 50-100 parásitos/μL
• Pruebas rápidas: 100 parásitos/μL
• PCR: 0,04-20 parásitos/μL



Resumiendo…

Gracias