Clones de Streptococcus pyogenes associados a elevada...
Transcript of Clones de Streptococcus pyogenes associados a elevada...

UNIVERSIDADE DE LISBOA
FACULDADE DE CIÊNCIAS
DEPARTAMENTO DE BIOLOGIA VEGETAL
Clones de Streptococcus pyogenes associados a
elevada frequência de colonização da orofaringe
Paula Maria Monteiro Fernandes
Mestrado em Microbiologia Aplicada
2011

UNIVERSIDADE DE LISBOA
FACULDADE DE CIÊNCIAS
DEPARTAMENTO DE BIOLOGIA VEGETAL
Clones de Streptococcus pyogenes associados a
elevada frequência de colonização da orofaringe
Paula Maria Monteiro Fernandes
Orientadora: Prof. Doutora Ilda Sanches (FCT-UNL/CREM) Orientadora Interna: Prof. Doutora Lélia Chambel (FCUL/BioFIG)
Mestrado em Microbiologia Aplicada
2011

Clones de Streptococcus pyogenes associados a
elevada frequência de colonização da orofaringe
Paula Maria Monteiro Fernandes
Tese de Mestrado
2011 Esta tese foi realizada no Centro de Recursos Microbiológicos (CREM/FCT-UNL) sob a orientação externa da Prof. Doutora Ilda Sanches e no Centro de Biodiversidade, Genómica Integrativa e Funcional (BioFIG/FCUL) sob a orientação interna da Prof. Doutora Lélia Chambel no âmbito do Mestrado em Microbiologia Aplicada da Faculdade de Ciências da Universidade de Lisboa.

“A maior parte das gaivotas não se querem
incomodar a aprender mais que os rudimentos
do voo, como ir da costa à comida e voltar. Para
a maior parte das gaivotas, o que importa não é
saber voar, mas comer. Para esta gaivota, no
entanto, o importante não era comer, mas voar”.
Richard Bach

AGRADECIMENTOS Pela contribuição para a realização do presente trabalho, gostaria de manifestar os meus agradecimentos: À Professora Doutora Ilda Sanches, orientadora externa desta tese de Mestrado, pela disponibilidade, ensinamentos, críticas, sugestões e incentivo demonstrados ao longo do decorrer da minha Tese. À Professora Doutora Lélia Chambel, orientadora interna desta tese de Mestrado, pela sua disponibilidade, saber, experiência, sugestões e incentivo demonstrados ao longo do decorrer da minha Tese. Ao Professor Doutor Rogério Tenreiro, Coordenador do Mestrado de Microbiologia Aplicada, pelo incentivo e por ter disponibilizado as condições necessárias à realização da parte inicial do trabalho desta Tese, no Instituto de Ciência Aplicada e Tecnologia - ICAT. À Professora Doutora Teresa Semedo, pela integração e apoio concedido no início do trabalho de presente Tese, no ICAT. À Doutora Sandra Chaves, pelos esclarecimentos pontuais na fase inicial laboratorial do meu trabalho, no ICAT. Às companheiras de trabalho e de almoço no ICAT: Joana e Lara. Ao Renato Pires, pela prontidão e esclarecimentos acerca do meu trabalho laboratorial desenvolvido na FCT/UNL e por me ter facultado os seus resultados ainda não publicados, no âmbito da sua Tese de Doutoramento, na qual está incluída esta Tese de Mestrado. Ao Doutor João Carriço, Ana Friães e Catarina Silva Costa da Unidade de Microbiologia Molecular e Infecção do Instituto de Medicina Molecular (IMM) (responsável: Prof. Doutor Mário Ramirez), todo o apoio na utilização do “software” BioNumerics. À Márcia Rato, pelos esclarecimentos prestados enquanto desenvolvia o meu trabalho prático na FCT/UNL. Ao Renato Pires, à Márcia Rato e à Joana Ministro, pelo companheirismo demonstrado no trabalho de Laboratório da FCT/UNL e nas pausas de almoço e lanche. À Drª Maria da Luz Antunes, Documentalista da Escola Superior de Tecnologia de Lisboa, pela prontidão na facilitação de artigos científicos para a redacção da presente Tese. Às colegas do IPS, pelas trocas de turnos de serviço, de forma a conciliar o serviço e o trabalho laboratorial desta Tese. Aos amores da minha vida, José e Magda, por todo o amor e carinho que me dedicaram durante esta etapa da minha vida. Aos meus pais, José e Noémia, pela compreensão, apoio e toda ajuda prestada.

Resumo
Os estudos de prevalência ou transversais epidemiológicos de Streptococcus do Grupo A são
muito frequentes, quando os isolados são associados a diversas infecções no entanto, estudos
deste tipo são raros quando os isolados são associados a colonização.
Pretendeu-se identificar os clones de S. pyogenes por métodos genotípicos (“Pulsed Field Gel
Electrophoresis”- PFGE, emm “typing”, “Multilocus Sequence Type”- MSLT) em 420 isolados de
colonização da cavidade orofaringea de crianças, funcionários e familiares de dez Creches/Jardins
de Infância, associados a uma elevada taxa de colonização (14%).
O PFGE, sendo um método de elevado poder discriminatório, revelou uma heterogeneidade de
padrões, a maior parte (397 isolados) com relação clonal.
Os tipos emm mais frequentes nos isolados de colonização foram o emm 1, 3 e 12 que,
comummente, se encontram associados a isolados invasivos (emm 1 e 3) e não invasivos (emm
12). O PFGE, o emm “typing” e o “Multilocus Sequence Type” definiram as linhagens de S.
pyogenes. Algumas delas encontram-se amplamente disseminadas pelo mundo (ST 36, ST 39 e
ST 46), outras apresentam uma grande longevidade (ST 15, ST 28, ST 36, ST 55) e todas
associadas a infecção, sugerindo que os portadores assintomáticos podem ser reservatório de
estirpes virulentas e que podem disseminá-las na comunidade.
Palavras chave: Streptococcus pyogenes; colonização; portadores assintomáticos saudáveis;
clones; linhagens genéticas.

Abstract
The epidemiological prevalence studies of the Lancefield group A streptococci (GAS) are
frequently related with infections isolates but are rare among colonization isolates.
The aim of our study was to identify the S. pyogenes clones by genotypic methods (Pulsed Field
Gel Electrophoresis- PFGE, emm typing and Multilocus Sequence Type- MLST) among the 420
colonization isolates collected from the oropharyngeal cavity of healthy child and contact groups
that attend to Day Care Centers, associated with high colonization rates (14%).
The heterogeneity patterns revealed by PFGE are an omen of its high discriminatory power and
allowed to verify that, from the 420 isolates, 397 were clonally related. The emm types emm 1,
emm 3 and emm 12 were the most prevalent in colonization isolates and, usually, emm 1 and 3
are associated an invasive infection while emm 12 is associated with noninvasive infection.
The genetic lineages of S. pyogenes were defined by PFGE, emm typing and MLST. Some of
them are world widely disseminated (Sequence Type- ST 36, ST 39 and ST 46) and others persist
for long decades (ST 15, ST 28, ST 36, ST 55). All ST were associated with infection, suggesting
that the asymptomatic carriers may be considered virulent strains reservoirs and can spread them
in the community.
Keywords: Streptococcus pyogenes; colonization; healthy asymptomatic carriers; clones; genetic
lineages.

Índice 1- Introdução 1
1.1- Características do género Streptococcus 1
1.2- Caracterização da espécie Streptococcus pyogenes 1
1.3- Patologias associadas a Streptococcus do Grupo A 2
1.3.1- Infecções supurativas 2
1.3.2- Infecções não supurativas ou sequelas 3
1. 4- Constituintes celulares e factores de virulência de S. pyogenes 3
1.4.1- Constituintes celulares intrínsecos: 3
1.4.1.1- Proteína M 3
1.4.1.2- Proteína T 4
1.4.1.3- Ácido hialurónico 5
1.4.2- Proteínas extracelulares 5
1.4.3- As exotoxinas pirogénicas 5
1. 5- Transmissão da infecção 6
1.6- Objectivos deste estudo 6
2- Material e Métodos 7
2.1- Participantes/Amostra 7
2.2- Conservação das estirpes bacterianas 7
2.3- Estirpes bacterianas e condições de crescimento 8
2.4- Identificação presuntiva de Streptococcus pyogenes 8
2.4.1- Testes Serológicos 8
2.4.1.1- Hidrólise do L-pirrolidonil-β-naftil-amido (PYR) 8
2.4.1.2- Determinação do grupo A de Lancefield 8
2.4.1.3- T-“typing” 8
2.4.2- Teste de susceptabilidade à bacitracina 8
2.5- Métodos genotípicos 9
2.5.1- Electroforese em Gel de Agarose por Campo Pulsado- “Pulsed
Field Gel Electrophoresis, PFGE” 9
2.5.1.1- Propagação das culturas 9
2.5.1.2- Lavagem celular e ajuste da concentração celular 9
2.5.1.3- Preparação dos discos de agarose 10
2.5.1.4- Lise celular 10
2.5.1.5- Desproteinização 10
2.5.1.6- Lavagem para remoção da proteinase K 11
2.5.1.7- Restrição do DNA com a enzima SmaI 11
2.5.1.8- Preparação do gel com os discos de DNA 11
2.5.1.9- Coloração do gel e digitalização da imagem 11
2.5.1.10- Análise dos perfis de PFGE 11

2.5.2- emm “typing” 12
2.5.3- MLST- “Multilocus Sequence Typing” 12
2.5.3.1- Análise das sequências no “software DNAStar- SeqMen” 12
2.5.3.2- Análise dos dados de MLST- “eBURST” 13
2.5.4- Inferência Estatística 13
3- Resultados 14
3.1- Amostra 14
3.2- Taxa de colonização 14
3.3- Teste de sensibilidade à bacitracina 15
3.4- T “typing” 15
3.5- Critérios para avaliação dos métodos de tipificação 16
3.5.1- Tipabilidade 16
3.5.2- Reprodutibilidade 16
3.5.3- Poder discriminatório/ Índice de Simpson/ Intervalos de Confiança 16
3.6- PFGE- “Pulsed Field Gel Electrophoresis” 17
3.6.1- Tipabilidade 17
3.6.2- Prevalência dos padrões de PFGE nos DCCs e sua localização
Geográfica 17
3.6.3- Reprodutibilidade de PFGE 19
3.6.4- Dendrograma 20
3.7- emm-“typing” 22
3.7.1- Tipabilidade 22
3.7.2- Diversidade dos tipos emm 22
3.7.3- Distribuição dos tipos emm, de 2000 a 2007 23
3.7.4- Análise da distribuição dos tipos emm na Primavera, no Outono
e no Inverno 24
3.8- Determinação do Coeficiente de Wallace 25
3.9- MLST- “Multilocus Sequense type” 26
3.9.1. Tipabilidade 26
3.9.2- “eBURST” 26
3.9.3- Comparação de isolados de colonização de S. pyogenes
com os da base de dados do MLST 27
3.10- Linhagens Genéticas 30
3.11- Poder Discriminatório e Intervalos de Confiança de PFGE, emm “typing” e MLST 31
3.12- Inferência Estatística 31
3.12.1-Teste de independência do Qui-Quadrado- simulação de Monte-Carlo 31
4- Discussão/Conclusão 34
5- Referências 37

6- Anexos 40
Anexo I 40
Anexo II 43
Anexo III 44
Anexo IV 46
Anexo V 46
Anexo VI 46
Anexo VII 47
Anexo VIII 49
Anexo IX 50
Anexo X 51

1
1- Introdução
1.1- Características do género Streptococcus
Actualmente existem 17 géneros diferentes de cocos Gram positivos, sendo um deles o género
Streptococcus (1), o qual vai ser objecto do nosso estudo.
Os cocos agrupam-se em cadeias, e apresentam outras características, tais como: catalase negativa (não
hidrolisam o peróxido de hidrogénio devido à ausência de catalase), anaeróbios facultativos, imóveis e não
formam esporos.
Têm como seu habitat preferido o Homem e os Animais, podendo causar-lhes infecções.
A classificação das espécies do género Streptococcus, clinicamente significativas, foi difícil devido à falta de
características fenotípicas decisivas (3). Em 1994, Stackebrandt, E. & Goebel, B.M. (2) descobriram que as
relações filogenéticas das espécies procariotas podem ser estabelecidas com base na sequência do 16S
rRNA para níveis de homologia inferiores a 97% e o seu posicionamento taxonómico pode ser confirmado
por hibridização DNA-DNA, quando a homologia é superior a 97% (3).
Assim, em 2002, Facklam, R.R. (1) apresenta a árvore filogenética de 55 espécies incluídas no género
Streptococcus, baseada na análise da sequência do 16S rRNA.
1.2- Caracterização da espécie Streptococcus pyogenes
Segundo Facklam, R.R. (1) a hemólise das colónias em agar de sangue ajuda na classificação do género
Streptococcus ao nível da espécie. As colónias de S. pyogenes têm diâmetro superior a 0,5 mm, variam
entre o transparente e o translúcido, convexas, circulares, brilhantes, rodeadas por uma ampla β-hemólise
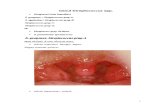
em agar suplementado com de sangue de carneiro como se pode observar na fig.1. A hemólise parcial,
muitas das vezes apresenta a coloração verde em torno das colónias em meio com sangue e designa-se
por α-hemólise, ao passo que γ-hemólise corresponde à ausência de hemólise em torno das colónias em
agar de sangue. Esta característica fenotípica é muito usada em Microbiologia Médica (4).
Figura 1- β-Hemólise de S.pyogenes.
(http://spyogenes.mlst.net/)
Outra característica fenotípica da espécie é a presença, na parede celular de S. pyogenes, de um
polissacárido antigénico constituído por N-acetil-β-D-glucosamina ligada a um polímero de ramnose, cuja

2
reactividade serológica permite classificar esta espécie como pertencente a Streptococcus do Grupo A
(GAS) (5).
Até à data conhecem-se doze genomas de S.pyogenes: dois M1, um M2, dois M3, um M4, um M5, um M6,
dois M12, um M18 e um M28 (6). Também se sabe que o teor de G+C das espécies piogénicas do GAS
varia entre os 38,5% e os 38,6% e que o seu genoma varia entre os 1,85-1,9 Mb (7).
A espécie mais patogénica deste género é S. pyogenes, descrevendo-se de seguida as doenças mais
características desta espécie.
1.3- Patologias associadas a Streptococcus do Grupo A
Streptococcus do Grupo A (GAS) coloniza1 a garganta e a pele, podendo vir a ser responsável por inúmeras
infecções supurativas e não supurativas (sequelas).
Madigan, M.T., et al., (8) refere que a microbiota de um indivíduo depende bastante das condições a que se
encontra exposto e que é muito diversificada, podendo diferir bastante entre indivíduos e até mesmo numa
dada população, como se pode observar na tabela 1.
Tabela 1– Géneros representativos da microbiota humana.
Madigan, M.T., et al., (8).
1.3.1- Infecções supurativas
Nas infecções supurativas existem as infecções piogénicas (faringite e tonsilite), a celulite, o impétigo, a
erisipela, a escarlatina, a fasceíte necrosante (NF- “Necrotizing Fasciitis”), a síndrome do choque tóxico
estreptocócico (STSS- “Streptococcal Toxic Shock Syndrome”) e a miosite estreptocócica. Esta diversidade
de infecções envolve as membranas das mucosas, a pele e os tecidos mais profundos, variando as
mesmas entre o moderado e o extremamente severo.
1 Colonização- proliferação de um microorganismo após anexação aos tecidos do hospedeiro ou outras superfícies.
Madigan, et al. (8).

3
A faringite afecta as crianças em idade escolar, dos 5 aos 15 anos (5) e também adultos como os recrutas
no Texas (10), devido à facilidade que Streptococcus apresenta em se espalhar por entre as multidões,
nomeadamente através da tosse e espirros. A faringite associada à febre reumática ocorre na Primavera e
Inverno, ao passo que as infecções da pele ocorrem no Verão, e podem estar associadas à glomerulonefrite
aguda (5).
Os serótipos mais frequentes de S. pyogenes associados à faringite e à febre reumática são os M1, 3, 5, 6,
14, 18, 19 e 24. Os serótipos M que causam impétigo (infecção da pele) são diferentes destes.
Quanto às infecções da pele (impétigo, erisipela e celulite) podem ser causadas pelo GAS, mas no caso da
erisipela e da celulite também podem ser causadas pelos grupos B, C e G. A erisipela afecta as camadas
superficiais da pele, enquanto que a celulite afecta os tecidos sub-cutâneos. Nestes casos, a porta de
entrada do GAS é as queimaduras e outros tipos de lesões na pele.
Por outro lado, a fasceíte necrosante e a STSS são infecções invasivas. A primeira, destrói a gordura peri-
muscular e a fascia ou bainha muscular, apresentando elevada taxa de mortalidade, e a segunda, afecta
vários órgãos (10).
1.3.2- Infecções não supurativas ou sequelas
As sequelas deixadas por S. pyogenes são a febre reumática e a glomerulonefrite.
A febre reumática pressupõe a presença de alguns dos seguintes sinais: poliartrite, lesão cardíaca. Os
serótipos mais frequentes são M5, 6 e 18.
Na glomerulonefrite aguda (GNA), os serótipos envolvidos diferem conforme a infecção tenha surgido na
faringe ou na pele. A GNA pós-angina aparece em crianças e jovens, ao passo que a GNA pós-cutânea
surge em todas as idades.
Nas sequelas, o isolamento de GAS não é possível. O diagnóstico é feito com base na etiologia imunológica
por síntese de anticorpos antiestreptocócicos que reconhecem antigénios semelhantes no coração ou no
rim (10).
1.4- Constituintes celulares e factores de virulência de S. pyogenes
O conhecimento dos factores de virulência é o primeiro passo para a descoberta de vacinas e fármacos, daí
a sua importância em os descrever (11).
1.4.1- Constituintes celulares intrínsecos:
1.4.1.1- Proteína M
A proteína M é um factor major de virulência de Streptococcus do Grupo A e está associada a resistência à
fagocitose e adesão às células (12).
Durante décadas, a determinação serológica da proteína M foi o modelo adoptado, baseado na diversidade
antigénica desta proteína. Em 1962, Lancefield desenvolveu um método para preparar extractos de
Streptococcus para tipagem serológica. Desde então outros métodos têm sido desenvolvidos, o que
permitiu identificar 124 genótipos M diferentes (7).

4
A proteína M exibe na sua superfície fímbrias (5). Cada fímbria consiste numa só molécula dimera, com 50
a 60 nm de comprimento, não sendo composta por múltiplas sub-unidades como no caso dos pili das
bactérias Gram negativas (13).
Por outro lado, a sequência completa da proteína M6 (emm6) permitiu compreender a sequência amino
acídica desta proteína. A proteína M é composta por duas cadeias polipeptídicas com uma conformação α-
hélice (7). O segmento C terminal é composto por animoácidos hidrofóbicos, ancorado na membrana celular
que atravessa a camada de peptidoglicano, sendo este rico em prolina e glicina. Segue-se uma região
central que tolera uma vasta variação de sequências de amino ácidos. A região N-terminal desempenha um
papel importante na actividade biológica da molécula uma vez que leva à produção de anticorpos pelo
hospedeiro. Esta região designa-se por hipervariável, como se pode observar na figura 2.
É de referir ainda que a proteína M49 não possui o segmento N-terminal (14).
Figura 2- Modelo da proteína M6, da estirpe D471, baseado em dados da estrutura e da sequência da proteína. A
sequência nucleotídica da região N-terminal tem aproximadamente 11 aminoácidos e denomina-se hipervariável por
variar muito entre estirpes de S. pyogenes.
Fischetti, V.A. (13).
No Homem, a proteína M liga-se a proteínas do hospedeiro (por exemplo, o factor H e o fibrinogénio),
inactivando a via alternativa do complemento evitando assim a fogocitose e a morte por linfócitos
polimorfonucleares (PMN) (7).
1.4.1.2- Proteína T
A proteína T não está relacionada com a virulência, no entanto possui especificidade pelo que permite a
diferenciação laboratorial dos diferentes serótipos (15). Dos constituintes celulares intrínsecos também
fazem parte o ácido hialurónico, o ácido lipoteicóico, a proteína F e o factor de opacidade do soro (OF) que
são responsáveis pela adesão, colonização e invasão das membranas das mucosas e da pele no Homem
(16).

5
1.4.1.3- Ácido hialurónico
A cápsula do GAS é composto por ácido hialurónico, um polímero de elevado peso molecular constituído
por N-acetilglucosamina e ácido glucorónico.
Também se sabe que o tamanho da cápsula não é o mesmo em todas as estirpes deste género. As
colónias com um aspecto mucóide, quando cultivadas em agar de sangue, possuem uma “cápsula maior”.
Assim, verificou-se que as estirpes encapsuladas resistem mais facilmente à fagocitose quando
comparadas com as não capsuladas (7).
Em 1992, Johnson, D. R. et al., (17) referem que o aspecto mucóide das colónias em 3% de Streptococcus
do Grupo A verifica-se em casos com faringite, em 21% dos isolados com origem em doenças invasivas e
em 42% dos isolados, em doentes com febre reumática aguda.
1.4.2- Proteínas extracelulares
Deste grupo de proteínas extracelulares fazem parte: a estreptolisina O; a estreptolisina S; as DNAses A, B,
C e D; a hialuronidase; a estreptoquinase; a exotoxina estreptocócica pirogénica B (Spe B- protease
cisteina) e a C5a peptidase.
O GAS, em geral produz as duas hemolisinas: a estreptolisina O e S, no entanto só a O é antigénica.
Quer a estreptolisina O, quer a S danificam as membranas dos PMN, das plaquetas e dos organelos
celulares. Têm ainda em comum o facto de não serem inibidas na presença de oxigénio.
As DNAses degradam o DNA; a hialuronidase degrada o ácido hialurónico dos tecidos; a estreptoquinase
dissolve os coágulos, através da conversão do plasminogénio em plasmina; a Spe B é uma protease e a
peptidase C5a cliva a ligação deste factor do complemento aos PMN (7).
A proteína Sic (“Streptococcal inhibitor of complement”) é secretada pelas estirpes M1 inibindo uma fracção
do complemento e a lise da bactéria (18, 19).
1.4.3- As exotoxinas pirogénicas
As exotoxinas pirogénicas actuam como superantigénios capazes de se ligarem ao Complexo de
Histocompatibilidade Major II e a receptores específicos das células T. Esta ligação desplota a activação
rápida de enumeras células T, levando à secreção de citocinas (por exemplo, Interleucina-2, interferon γ),
responsáveis por falência de múltiplos órgãos, o que caracteriza a STSS (19). Na figura 3 podem observar-
se os factores de virulência de S. pyogenes.

6
Figura 3- Factores de virulência de S. pyogenes.
Mitchell, T.J. (19).
1. 5- Transmissão da infecção
A transmissão ocorre de humano para humano por contacto com secreções oriundas do nariz, da garganta,
tosse, espirros ou por lesões na pele. Os portadores assintomáticos são menos contagiantes do que os que
manifestam a infecção. O período de incubação é curto, entre 1 a 3 dias. O tratamento com antibiótico, por
exemplo a penicilina, evita a propagação da infecção.
Num estudo com o objectivo de detectar o tempo que demora a negativar a presença de S. pyogenes em
crianças, os autores descobriram que 24 h após o início da terapêutica, menos de 20% das culturas eram
positivas (20).
1.6- Objectivos deste estudo
- Identificar os clones de Streptococcus pyogenes com mais de 80% de semelhança de perfis de macro-
restrição do DNA obtidos por PFGE e linhagens genéticas com base em polimorfismos do gene emm (emm
“typing”) e de genes nativos (“Multilocus Sequence Typing”-
MLST)
- Avaliar a distribuição espaço-temporal dos clones e inferir a sua associação com “Day Care Centers-DCC”
e estação do ano.

7
2 - Material e Métodos
2.1- Participantes/Amostra
Neste estudo foi colhido um total de 1026 exsudados orofaríngeos de portadores assintomáticos de S.
pyogenes, provenientes de dezasseis Creches/Jardins-de-Infância do Concelho de Oeiras e duas Escolas
do Distrito de Lisboa, abrangendo 10 578 participantes. Englobou funcionários, pais e crianças dessas
Instituições. O período de recolha foi de 2000-2007.
Os participantes responderam a um questionário e assentiram a confidencialidade dos dados (em anexo I).
A percentagem média de colonização foi de 9,7% (1026/10 578) (22), evidenciada na figura 4.
Figura 4- Percentagem de colonização de S. pyogenes em crianças portadoras no Concelho de Oeiras (2000-2007). A
linha a preto representa a percentagem média de colonização.
Sanches, I., et al., 2009. (21).
Com uma taxa de colonização inferior a 10% registaram-se 307 isolados e com uma taxa entre os 10 e os
14%, registaram-se 299 isolados. Os dados apresentados nesta tese referem-se a 420 isolados com uma
taxa de colonização igual ou superior a 14%. Estes isolados advêm de portadores assintomáticos de S.
pyogenes pertencentes a 10 Creches/Jardins-de-Infância (codificados por DCC- “Day Care Centres”) do
Concelho de Oeiras e a duas Escolas de Lisboa, colhidos entre 2000 e 2007. Os 420 isolados foram
colhidos num total de 1822 participantes (anexo II).
Das 420 estirpes em estudo, o operador B desenvolveu o seguinte trabalho laboratorial: 53 amostras para
“Pulsed Field Gel Electrophoresis” (PFGE), 105 amostras para emm “typing” e 20 amostras para “Multilocus
Sequence Typing” (MLST). O restante foi efectuado pelo operador A.
2.2- Conservação das estirpes bacterianas
Todas as estirpes foram conservadas a -80ºC em tubos de criopreservação contendo 1,8 ml de meio líquido
“Brain Heart Infusion” suplementado com 20% de glicerol.
8
11 11
15
6
17
13 13
810 10
12
15
7 8
18
02
46
81012
1416
1820
2000/2001(n=1012)
2001/2002(n=1134)
2002/2003(n=1204)
2003/2004(n=1335)
2004/2005(n=736)
2006(n=819)
2007(n=725)
Outubro Fevereiro
Maio
% C
olo
niz
açã
o

8
2.3- Estirpes bacterianas e condições de crescimento
As estirpes bacterianas advêm de exsudados da cavidade orofaringea de humanos (crianças e adultos).
As estirpes cresceram em meio sólido “Triptic Soy Agar” (TSA) suplementado com 5% de sangue
desfibrinado de carneiro (Probiologica, U.E.).
2.4- Identificação presuntiva de Streptococcus pyogenes
2.4.1- Testes Serológicos
Os testes serológicos são testes de aglutinação em lâmina entre o composto/reagente e várias colónias de
colónias de S. pyogenes, retiradas com uma ansa de 10 µl.
2.4.1.1- Hidrólise do L-pirrolidonil-β-naftil-amido (PYR)
As estirpes que hidrolisam este composto exibem uma cor rosa, o que significa que possuem a enzima
pirrolidonil peptidase. O teste do PYR efectuou-se a isolados resistentes à bacitracina.
2.4.1.2- Determinação do grupo A de Lancefield
O teste usado foi o de “Slidex ® Strepto A, bioMérieux®, Marcy l´Etoile, France”. A aglutinação significa a
presença do carbohidrato do grupo A e a não aglutinação significa ausência desse carbohidrato.
2.4.1.3- T-“typing”
Os soros utilizados foram comprados ao “ Swedish Institute for Infectious Disease- Smittskyddinstitutet”.
Cinco eram polivalentes e vinte eram monovalentes. Quando há uma aglutinação com um dos soros
polivalentes, passa-se aos soros monovalentes para determinar o(s) tipo(s) T. Quando não há nenhuma
aglutinação com os soros polivalentes, a estirpe é considerada “non typeable” (NT).
2.4.2- Teste de susceptabilidade à bacitracina
O teste de susceptabilidade à bacitracina consiste no teste de difusão do disco com 0,04 U de bacitracina-
BBLTM, “Becton Dickinson, Le Pont de Claix, France”. A ausência de halo de inibição à volta do disco de
bacitracina corresponde a estirpes resistentes à bacitracina, enquanto que a presença do halo de inibição
significa estirpes susceptíveis à bacitracina.

9
2.5- Métodos genotípicos
2.5.1- Electroforese em Gel de Agarose por Campo Pulsado- “Pulsed Field Gel
Electrophoresis, PFGE”
Este método consiste no corte do DNA cromossomal utilizando enzimas de restrição de corte raro. Os
fragmentos obtidos são de massa molecular elevada, por isso são sujeitos a uma electroforese de campo
pulsado de modo a separar os fragmentos de DNA produzidos pela restrição, obtendo-se um padrão
característico para cada estirpe. O método utilizado foi adaptado de Chung, M., et al., (23), a que
designámos Método A, executado pelo operador A. Como houve outro operador- operador B- que introduziu
outras alterações, designámos por Método B. A descrição dos materiais usados nesta electroforese
encontram-se no anexo III.
2.5.1.1- Propagação das culturas
Os isolados conservados a -80ºC foram semeados em meio de “Trytic Soy Agar- TSA” com sangue de
carneiro. Incubaram a 37ºC durante 24 h.
Depois, inocularam-se algumas colónias em meio líquido “Todd-Hewitt” (Método A) ou meio líquido “Brain
Heart Infusion” (Método B), a 37ºC durante 24h.
2.5.1.2- Lavagem celular e ajuste da concentração celular
Pipetar 2 ml de cada cultura anterior para tubos “eppendorf”. Centrifugar a 13000 rpm durante 20 min.
Conversar as culturas em gelo. Decantar o sobrenadante. Ressuspender o “pellet” em 1 ml de PIV e
centrifugar a 13000 rpm, durante 25 min. Decantar e adicionar 200 µl de PIV.
Para ajustar a concentração das suspensões celulares de cada isolado, pipetou-se 1 ml de PIV para uma
“cuvette” do espectrofotómetro e 5 µl da suspensão celular. Mediu-se a absorvância a 620 nm. Os valores
de absorvância obtidos devem variar entre 0,025 cm-1 e 0,15 cm-1, caso contrário todas as etapas anteriores
devem ser repetidas. Após a leitura da absorvância adicionou-se o volume de PIV necessário para que a
densidade óptima final fosse 5,0. O volume de PIV adicionado foi calculado pela fórmula seguinte:
Vadd (µl)= (DOx 40x 210) – 210
Vadd- volume (µl) de PIV a adicionar à suspensão celular
DO- valor da densidade óptica a 620 nm
40- Quociente resultante da divisão do factor de diluição (200) pelo valor da densidade óptica óptima (5,0)
A quantidade de PIV a adicionar é aferida tendo em conta que o volume de suspensão celular no tubo é de
aproximadamente 210 µl e tendo em atenção que o valor da absorvância registado corresponde a uma
diluição de 5 µl de suspensão em 1 ml de PIV.

10
2.5.1.3- Preparação dos discos de agarose
Colocar em “eppendorfs” 150 µl (Método A) ou 500 µl (Método B) da suspensão celular a 42ºC e adicionar
150 µl da solução de agarose “Seaplaque” (Método A) ou 500 µl da solução de agarose “Low Melting Point”
(Método B), à mesma temperatura.
No Método A, pipetar 12 vezes 20µl da mistura para uma placa de vidro (forrada com “parafilm” e pré-lavada
com etanol a 70ºC). Colocar por cima dessas gotas uma lâmina de vidro (pré-lavada com etanol a 70ºC),
achatando-as, obtendo-se os discos.
Colocar este preparo 5 min a -20ºC e depois 10 min à temperatura ambiente. Retirar a lâmina e com o
auxílio de uma ansa transferir os discos para um tubo “Falcon” de 15 ml (figura 5).
No Método B, encher uma seringa de insulina (com a ponta cortada) com a mistura descrita. Colocá-la em
cima de gelo, 10 min. Depois com uma lamela cortar os discos para um tubo “Falcon” previamente
identificado (figura 6).
Figura 5- Discos de DNA obtidos pelo Método A. Figura 6- Discos de DNA obtidos pelo Método B.
Chung, M., et al., (23 ). Tenreiro, R. P. A. (24).
2.5.1.4- Lise celular
Aos tubos Falcon contendo os discos, adicionar 1 ml de solução de lise (solução EC+ 1 mg/ml Lisozima+ 5
U/µl de Mutanolisina) (Método A) ou 4 ml no Método B. Incubar durante a noite a 37ºC.
2.5.1.5- Desproteinização
Decantar a suspensão anterior e adicionar 1 ml ou 4 ml de solução ESP (Tampão ES+ 1 mg/ml Proteinase
K) (Método A ou Método B). Incubar a 50ºC durante 17 h (Método A) ou 24 h (Método B).

11
2.5.1.6- Lavagem para remoção da proteinase K
Decantar a solução ESP. Suspender em 12 ml de tampão TE 1X. Colocar os tubos em agitação, 30 min.
Decantar e resuspender em TE 1X. Repetir este passo 8 vezes. Armazenar os discos a 4ºC em 1 ml ou 4 ml
(Método A ou B) de TE 1X.
2.5.1.7- Restrição do DNA com a enzima SmaI
Este passo deve realizar-se, de preferência, no dia ou um dia antes da corrida electroforética.
Incubar à temperatura ambiente durante 40 min um disco com 150 µl de tampão pré-SmaI (“Invitrogen”-
Método A, “Takara”- Método B). Decantar e adicionar 50 µl do tampão com 20 U/µl ou 10 U/µl de SmaI
(Método A ou B). Para parar a restrição adicionar 5 µl de azul de bromofenol 6x e armazenar os discos.
2.5.1.8- Preparação do gel com os discos de DNA
Preparar um gel de agarose “Seakem” a 2% em TBE a 0,5X e guardar a 50ºC. Montar as peças do suporte
do gel e de seguida colocar os discos nos dentes do pente com a ajuda de uma ansa e lamela. Nas
extremidades do pente colocar um disco de marcador DNA lambda de massa molecular conhecida. Colocar
o pente no suporte e cuidadosamente verter a agarose, arrefecida, sem que haja movimentação dos discos
colocados no pente. Selar os poços com agarose e deixar solidificar. Por fim, retirar o aparato de moldagem
e colocar o gel no aparelho de PFGE onde previamente se colocou 2 l de TBE a 0,5X. Iniciar a corrida
electroforética com: temperatura 11,3ºC, tempo inicial de pulso 5 s, tempo final de pulso 35 s, voltagem
6V/cm, ângulo 120º, tempo de corrida 23 h.
2.5.1.9- Coloração do gel e digitalização da imagem
Retirar o gel do aparelho e colocá-lo na solução de brometo de etídeo, em agitação suave, durante 40 min.
Depois descorar o gel em 300 ml de água bidestilada autoclavada, em agitação suave durante 10 min. Em
seguida captar a imagem do gel num sistema fotográfico.
2.5.1.10- Análise dos perfis de PFGE
A análise dos padrões de bandas de DNA cromossomal foi por inspecção visual. Os DNAs produziram 9 ou
mais fragmentos, pelo que, uma banda de diferença foi o critério para definir os diferentes padrões de PFGE
(atribuindo uma letra diferente a um padrão diferente).
Estes padrões também foram comparados através da construção de um dendrograma utilizando o “software
BioNumerics 6.5- Applied Maths”. Os clusters foram definidos para grupos de estirpes que partilham entre si
80% ou mais de semelhança.

12
2.5.2- emm “typing”
O protocolo do emm “type” encontra-se descrito no “site” do “Centers for Disease Control and Prevention”
[online] (25).
O primeiro passo deste protocolo consiste na preparação do lisado bacteriano. O operador B obteve o
lisado de outra forma: colocou um disco guardado em TE 1X a 4ºC num “eppendorf” contendo 450 µl de TE
1X. Depois colocou-o num termobloco a 65ºC, 10 min (30). No entanto, em alguns casos foi necessário
proceder conforme descrito no protocolo do CDC. Para visualizar os amplicões resultantes do PCR e os
fragmentos de restrição por RFLP (“Restriction Fragment Length Polymorphism”), prepararam-se géis de
agarose a 1% e a 3% em Tris Acetato EDTA, respectivamente. Depois da gelose derreter adicionou-se 25µl
de “GelRed, Biotium”.
Utilizaram-se dois marcadores: “1Kb DNA ladder, New England, Biolabs” para os amplicões de PCR e o
“O´geneRuler 100 bp DNA ladder, Fermentas” para os fragmentos obtidos por RFLP.
A atribuição do tipo emm foi estabelecida mediante comparação com padrões representativos, existentes no
laboratório. Os que diferiam dos padrões representativos foram purificadas pelo “Kit Jet Quick PCR
purification, Genomed” e sequenciados pela Empresa STABVida. As sequencias obtidas foram editadas no
programa “BioEdit” e depois submetidas no “Blast 2.0 server” do CDC [online] (26) que nos indicou o tipo
emm da estirpe, via correio electrónico.
2.5.3- MLST- “Multilocus Sequence Typing”
Em 2006, (27) tinham sido publicados 35 esquemas de MLST, 33 dos quais acessível via “internet”. Assim,
no “site” do MLST [Online] (28) encontram-se as Sequências Tipo (ST) de Streptococcus pyogenes, ou seja,
as sequências nucleotídicas de múltiplos loci que codificam os 7 genes “housekeeping” (genes nativos)
desta espécie: gki, gtr, mutI, mutS, recP, xpt, yqiL, com 434 a 498 bp.
As condições de PCR encontram-se descritas no “site” MLST [online]. O marcador de massa molecular
usado na electroforese foi o “O´geneRuler 100 bp DNA ladder, Fermentas”.
Os amplicões foram purificados pelo “Kit Jet Quick PCR purification, Genomed” e sequenciados pela
Empresa STABVida, no equipamento ABI3730XL (“AppliedBiosystems”), que utiliza o método de Sanger e a
química “Bigdye Terminator V3.1, AppliedBiosystems”.
É de notar que na sequenciação de produtos de PCR por MLST são usados ambos os “primeres”, sendo
sequenciadas as duas cadeias de DNA. As sequências obtidas devem ter 100% de precisão, de forma a
evitar que um alelo conhecido seja convertido num alelo novo.
2.5.3.1- Análise das sequências no “software DNAStar- SeqMen”
As sequências resultantes são analisadas pelo programa informático “DNAStar-SeqMen”. A sequência
resultante designa-se sequência “consensus”2. Depois, aceder ao endereço electrónico do MLST [online] e
2 Sequência “consensus”- sequência de ácidos nucleicos, na qual, a base numa dada posição é a base mais frequentemente
encontrada quando se comparam sequências experimentalmente obtidas. Madigan, M. T., et al., (8).

13
seleccionar “Locus Query” e escolher “Single Locus”. O passo seguinte consiste em copiar a sequência
“consensus” do alelo pretendido, colá-lo no espaço destinado e o “site” atribui o número do alelo, caso haja
100% de correspondência entre o alelo e as sequências existente no “site”. Caso contrário, a sequência terá
de ser re-analisada ou mesmo re-sequenciada. Seguidamente, para obter a sequência tipo (ST), clicar em
“Profile Query” e depois em “Allelic”. Introduzir o número de cada um dos sete alelos e seleccionar “Query
entire base” e o número da ST da estirpe é atribuído.
2.5.3.2- Análise dos dados de MLST- “eBURST”
O “eBURST” é um “software” que tem implícitas duas questões: como é que os clones de bactérias surgem
e como se diversificam?
O “eBURST” foca-se na identificação de grupos de isolados intimamente relacionados, dentro da população;
na identificação do ancestral ou do “founder genotype” de cada grupo e nos caminhos evolutivos dos
descendentes, desde o “founder” até aos restantes membros desse grupo (num curto espaço de tempo)
(29)
Assim, ao introduzirem-se os dados dos perfis alélicos obtidos por MLST no “eBUST”, a árvore resultante
corresponderá, eventualmente, a variantes que diferem em um ou dois dos sete loci, designando-se “Single
Locus Variant- SLV” ou “Double Locus Variant- DLV”, respectivamente.
Outra definição importante é a de complexo clonal, um conjunto de isolados com origem no ancestral ou no
“founder” da ST e com múltiplos “SLVs” (30).
2.5.4- Inferência Estatística
Para avaliar a distribuição dos clones e inferir a sua associação com os DCCs (hipótese 1) e com as
estacões do ano (hipótese 2), elaboraram-se duas tabelas, uma com os clusters e os DCCs e a outra com
os clusters e as estações do ano.
O programa de tratamento de dados usado foi o SPSS versão 18.0 para Windows.

14
3 - Resultados
3.1- Amostra
Dos 420 isolados, 10 (2,4%) são de adultos femininos: 2 provêm de familiares (mães) cujos filhos frequentam
os respectivos “Day Care Centers- DCC”, 6 provêm de Auxiliares de Acção Educativa, 1 provém duma
Cozinheira e o outro de uma funcionária cuja actividade Não foi Determinada (ND) no questionário como se
pode verificar na figura 7.
0
1
2
3
4
5
6
7
Auxiliares de Acção
Educativa
Cozinheira Familiares ND
Nº
de A
dulto
s
DCC 3 DCC 6 DCC 6
DCC 2 DCC 3 DCC 11
DCC 7 DCC 8 DCC 12
Figura 7– Número de adultos (familiares/funcionários) por DCC.
As idades dos adultos oscilavam entre os 19 e os 68 anos de idade.
410 isolados advêm de crianças, sendo 168 (40,2%) do sexo feminino e 242 (59,0%) do sexo masculino. As
idades variaram entre 1 e 6 anos de idade.
A figura 8 ilustra o predomínio do sexo masculino em todos os DCCs, à excepção no DCC 2 em que o
número de crianças do sexo masculino é igual ao do sexo feminino.
0
5
10
15
20
25
30
35
40
45
50
DCC 1 DCC 2 DCC 3 DCC 4 DCC 5 DCC 6 DCC 7 DCC 8 DCC 11 DCC 12
Nº
de
Cri
ança
s
M F
Figura 8– Prevalência do género das crianças em cada DCC, entre 2000 e 2007.
3.2- Taxa de colonização
No nosso estudo, a taxa de colonização por S. pyogenes é igual ou superior a 14%, como se pode observar
na figura 9.

15
Figura 9- Taxa de colonização nos diferentes DCCs, no período de 2000-2007. A linha a preto assinala os 14%.
3.3- Teste de sensibilidade à bacitracina
O teste da susceptibilidade à bacitracina foi realizado em todos os isolados provenientes de adultos e de
crianças. No entanto, em 2006, no DCC 11 identificaram-se dois isolados resistentes à bacitracina, em
crianças com 2 e 4 anos de idade, com o padrão de PFGE-F e em 2007, no DCC 5, identificaram-se três
isolados resistentes à bacitracina em crianças com 5 anos de idade e com o padrão de PFGE-AC.
Os cinco isolados eram emm 28 e em relação à resistência a macrólidos por S. pyogenes o fenótipo
encontrado foi o cMLSB (mecanismo de resistência a Macrólidos, Lincosamidas e Estreptogramina B
constitutivo) em todos eles (anexo IV).
A resistência diz-se constitutiva quando a bactéria produz metilases mesmo na ausência de um indutor.
Essas metilases, designadas “Erm” são responsáveis pela metilação da adenina A2058 da sub-unidade 23S
do rRNA alvo, comprometendo a ligação do antibiótico ao seu alvo e desta forma o microorganismo resiste
(31).
3.4- T “typing”
Entre 2000 e 2006 foram analisados, por T-“typing”, 231 isolados provenientes de crianças e 7 provenientes
de adultos. No total, os 238 isolados correspondem a 14 tipos T diferentes. Verificou-se que 53 (22,3%)
isolados eram T 12 (2002-05), 44 (18,5%) eram NT (“Non Typeable”) (2001-05), 32 (13,4%) eram T 1 (2000-
04) e 30 (12,6%) eram T 3/13/B3264 (2001-03), como se pode observar na figura 10.
0
10
20
30
40
50
60
Out.2
000
Mar
.200
1
Abr.2
001
Mai.2
001
Jun.
2001
Jun.
2001
Jun.
2001
Fev.20
02
Fev.20
02
Fev.20
02
Maio
.2002
Out.2002
Out.2002
Out.2003
Fev.20
03
Fev.20
03
Maio.
2003
Maio
.2003
Maio
.2003
Out.2003
Maio
.2004
Maio.2
004
Maio.2
004
Fev.20
05
Mar.2
006
Mar.2
006
Mar
.200
7
Mar
.200
7
Ta
xa
de
Co
lon
iza
çã
o (
%)
DCC1 DCC2
DCC3 DCC4
DCC5 DCC6
DCC7 DCC8
DCC11 DCC12

16
0
5
10
15
20
25
30
35
40
45
50
55
60
T 1 NT
T 12 T2
T2/28
T 28
T 3
T 3/1
3
T 3/1
3/B32
64 T 4
T 5/1
1/12
/27/
44
T 8/2
5/Im
p19
T 4/2
8
T 5/2
7/44 T6
Nº
de I
sola
dos
2006
2005
2004
2003
2002
2001
2000
Figura 10- Tipos T de 238 isolados de S. pyogenes (2000-2006).
3.5- Critérios para avaliação dos métodos de tipificação
A avaliação da eficiência dos métodos de tipagem baseia-se nos seguintes critérios: tipabilidade,
reprodutibilidade e poder discriminatório (32, 33).
3.5.1- Tipabilidade
A tipabilidade de um método é a percentagem de tipos atribuídos a diferentes isolados bacterianos (32).
3.5.2- Reprodutibilidade
A reprodutibilidade reflecte a atribuição do mesmo tipo a um isolado testado em diferentes ocasiões. Para
haver reprodutibilidade intra e inter-laboratorial tem de haver protocolos padrão e pessoal com treino.
3.5.3- Poder discriminatório/ Índice de Simpson/ Intervalos de Confiança
O poder discriminatório de um método de tipificação indica a probabilidade de duas estirpes não
relacionadas, extraídas de uma população, pertencerem a tipos diferentes (32).
Hunter, P.R. & Gaston, M.A. (32), propuseram o índice de diversidade de Simpson´s (D) para calcular o
poder discriminatório dos métodos de tipificação.
O índice de diversidade de Simpson´s pode ser calculado pela seguinte fórmula:
Onde, N é o número total de isolados; S é o número total de tipos obtido e nj é o número de isolados
pertencentes aos tipos j.
Para os autores (32), índices discriminatórios superiores a 0,90 representam um valor aceitável na
interpretação dos resultados.
Para, Van Belkum, A., et al., (33), o valor de (D) deve ser, idealmente, 1 mas na prática deve ser na ordem
de 0,95 para métodos de tipificação, tendo em conta que a probabilidade de erro é de 5%.
Por isso, é importante determinar os Intervalos de Confiança (I.C.) para os índices de Simpson´s de cada
método de tipificação, permitindo uma melhor avaliação dos mesmos (34).
Os intervalos de confiança são usados para indicar a confiança que se pode depositar numa estimativa
(http://pt.wikipedia.org/wiki/Intervalo_de_confian%C3%A7a).

17
3.6- PFGE- “Pulsed Field Gel Electrophoresis”
Os fragmentos de DNA do nosso estudo, obtidos por PFGE oscilaram entre 48,5 e 485 Kb e representam
um “fingerprint” identificativo e de diferenciação de estirpes bacterianas.
3.6.1- Tipabilidade
De acordo com o histograma apresentado na figura 11, os três padrões de PFGE com maior percentagem
são: o padrão AB com 22,6% (n=95), o padrão X com 16,2% (n=68) e o padrão AP com 12,6% (n=53). Os
padrões restantes apresentam percentagens inferiores e iguais a 7%.
0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95
Pa
drõ
es d
e P
FG
E
AKAUBDBFBJBLCECYDNEDEMENEOEPERESETEXFZGA
NABBI
DFDMDXELF
ACCXDKFWEKEHBMCZEQBCBEAJBHADBKEFBGAP
XAB
Nº de Isolados
Figura 11– Histograma de barras de 49 padrões de PFGE de 420 isolados.
3.6.2- Prevalência dos padrões de PFGE nos DCCs e sua localização geográfica
Na figura 12-a) pode observar-se a prevalência dos 49 padrões de PFGE em cada “Day Care Center” e na
figura 12-b) pode-se observar a sua distribuição geográfica.

18
Figura 12- a) Prevalência dos padrões de PFGE nos “Day Care Censtres”, entre 2000 e 2007.
DCC 1
0
5
10
15
20
25
X AP GA e FZ A
Padrões PFGE
Nº
de
Iso
lado
s
DCC 2
0
5
10
15
AP BH Heterogénio
Padrões de PFGE
Nº
de
Iso
lad
os
DCC 3
0
5
10
15
20
25
30
AB BM Heterogénio
Padrões de PFGE
Nº
de I
so
lado
s
DCC 5
0
10
20
30
40
50
AB X BE BC Heterogénio
Padrões de PFGE
Nº
de I
so
lado
s
DCC 12
0
5
10
15
20
EF AB
Padrões de PFGE
Nº
de Isola
dos
DCC 11
0
2
4
6
8
10
12
14
16
BK AJ Heterogénio
Padrões de PFGE
Nº
de I
sola
do
s
DCC 6
0
5
10
15
BG Heterogénio
Padrões de PFGEN
º d
e Iso
lad
os
DCC 7
0
5
10
15
20
25
AB X BG AD Heterogénio
Padrões de PFGE
Nº
de
Is
ola
dos
DCC 8
0
5
10
15
20
25
30
AB BG X Heterogénio
Padrões de PFGE
Nº d
e I
sola
dos
DCC 4
0
2
4
6
8
10
12
14
AP X EQ Heterogénio
Padrões de PFGE
Nº
de Iso
lados

19
Figura 12- b) Localização geográfica dos DCCs no Concelho de Oeiras. A heterogeneidade de padrões de PFGE pode ser apresentada pela seguinte por ordem decrescente:
DCC 3 (n=26) > DCC 7 (n=21) > DCC 6 (n=13) > DCC 5 (n=11) > DCC 4 (n=8) > DCC 2 e 8 (cada com n=5)
> DCC 11 (n=3).
3.6.3- Reprodutibilidade de PFGE
Para o estudo da reprodutibilidade do PFGE testaram-se 9,3% (n=39/420) estirpes em duas ocasiões
diferentes.
Como referido no capítulo Material e Métodos, a preparação dos discos de agarose do PFGE diferiu: entre
placa de vidro e lâmina (Método A executado pelo o operador A) ou através de uma seringa e lamela
(Método B executado pelo o operador B). A cada isolado testado em duplicado corresponde uma
percentagem de semelhança e quando esta se encontra acima de 80%, pode-se afirmar que houve
reprodutibilidade do método de PFGE.
Dos 39 isolados testados, houve dois cuja percentagem de semelhança foi inferior a 80%. Embora este
resultado ocorresse no Método B, convém referir que a causa mais provável se deva a uma restrição
incompleta do DNA com a enzima SmaI e não à forma de preparação dos discos de agarose. No que se
refere aos demais isolados, os valores das percentagens de semelhança denotam ter havido
reprodutibilidade do PFGE, quer pelo Método A quer pelo método B (tabela 2).
Tabela 2- Estudo da reprodutibilidade de PFGE para 39 estirpes testadas pelos métodos A/B. As percentagens de semelhança acima dos 80 % indicam haver reprodutibilidade para o Método de PFGE.
% Semelhança (BioNumerics 6.5)
Isolados testados em duplicado (n=39)
Método (A/ B)
< 80% (a)
2 B
[80,90]% 9 B
100% 1 B
80% 3 B
]80,90]% 8 B
]90,100]% 7 B
95% 4 A
100% 5 A
(a)Causa provável: restrição enzimática incompleta
DCC 12
DCC 3
DCC 1 DCC 2
DCC 4
DCC 5
DCC 8
DCC 7
DCC 6
DCC 11

20
3.6.4- Dendrograma
O dendrograma, elaborado no programa “BioNumerics versão 6.5- Applied Maths”, Bélgica, permite-nos
distinguir 23 clusters (grupos clonais), correspondendo a 397 isolados (388 de crianças e 9 de adultos)
clonalmente relacionados. Na figura 13, os clusters são representados por numeração romana, sendo o
cluster I o que regista maior número de isolados (n=99) e o cluster XXIII menor número de isolados (n=2).
Para tal, foi preciso ter em conta os critérios de tipificação de estirpes bacterianas, segundo os quais as
estirpes que diferem 2 a 3 fragmentos de DNA são consideradas relacionadas e as que diferem entre 4 a 6
fragmentos são consideradas possivelmente relacionadas (35), ou seja, as estirpes são consideradas
clonalmente relacionadas se apresentarem uma percentagem de semelhança superior a 80 % (linha azul da
figura 13).
Nota-se que há clusters característicos de dados DCCs. Por exemplo, o cluster X é característico do DCC 2,
o cluster VIII é característico do DCC 12.

21

22
3.7- emm-“typing”
3.7.1- Tipabilidade
De acordo com o histograma apresentado na figura 14 os três tipos emm que apresentam maior
percentagem são: emm 12 com 40,5% (n=170/420), emm 1 com 18,3% (n=77/420) e o emm 3 com 12,4%
(n=52/420). Os restantes tipos emm apresentam percentagens inferiores a 8 %.
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170 180
Tip
os e
mm
st4050
st1815
emm 64
emm 94
emm 78
emm 48
emm 22
emm 77
emm 4
emm 28
emm 89
emm 6
emm 2
emm 75
emm 3
emm 1
emm 12
Nº de Isolados
Figura 14- Histograma de barras de 420 isolados que ilustra a prevalência dos 17 tipos emm.
3.7.2- Diversidade dos tipos emm
A análise de 420 isolados de S. pyogenes revelou 17 tipos emm diferentes. A distribuição da diversidade
destes tipos emm pelos 10 “Day Care Centers” (DCC) encontra-se na tabela 3.

23
Tabela 3 - Distribuição dos tipos emm pelos 10 DCCs (2000-2007).
Tipos emm DCC
1 DCC
2 DCC
3 DCC
4 DCC
5 DCC
6 DCC
7 DCC
8 DCC 11
DCC 12
12 X X X X X X X X X X
1 X X X X X X X X X
75 X X X X X X
3 X X X X X
2 X X X X
4 X X X X
28 X X X X
6 X X X
22 X X
78 X X
89 X X
94 X X
48 X
64 X
77 X
st40.50 X
st18.15 X
Tendo em conta os dados da figura 14 e os da tabela 3, verificou-se que o emm 12 foi identificado em todos
os DCCs, o emm 1 em nove DCCs e o emm 3 em cinco DCCs.
Passando à análise da tabela 3, a maior diversidade dos tipos emm registou-se no DCC 3 (nove tipos emm
diferentes), seguido do DCC 6 e DCC 7 (ambos com oito tipos emm diferentes).
O DCC 5 e o DCC 8 apresentam sete tipos emm diferentes. O DCC 4 apresenta seis tipos emm diferentes,
o DCC 2 apresenta quatro tipos emm diferentes e os DCCs 1, 11 e 12 com três tipos emm diferentes.
A diversidade dos tipos emm nos DCCs pode ser apresentada por ordem decrescente:
DCC 3> DCC 6, DCC 7> DCC 5, DCC 8> DCC 4> DCC 2> DCC 1, DCC 11, DCC 12.
3.7.3- Distribuição dos tipos emm, de 2000 a 2007
A análise da figura 15 permite-nos afirmar que o tipo emm mais frequente (emm 12) teve o seu expoente
máximo em 2003, com 59 isolados. No ano seguinte desceu para 21 isolados, mantendo-se dentro destes
valores até 2007.
Em relação ao emm 1 e emm 3, o maior número de tipos emm 1 (n=21) verificou-se em 2004 e o maior
número de tipos emm 3 (n=27) verificou-se em 2001.
Para os tipos emm 64, st1815, st4050 só se registou um caso de cada, em 2005, 2002 e 2003,
respectivamente.

24
0
10
20
30
40
50
60
70
2000 2001 2002 2003 2004 2005 2006 2007
Nº
de E
stir
pe
s
emm 1
emm 2
emm 3
emm 4
emm 6
emm 12
emm 22
emm 28
emm 48
emm 64
emm 75
emm 77
emm 78
emm 89
emm 94
st1815
st4050
Figura 15- Distribuição dos tipos emm de S. pyogenes em isolados de colonização, de 2000-07.
3.7.4- Análise da distribuição dos tipos emm na Primavera, no Outono e no Inverno
Durante 8 anos foram colhidos 209 exsudados orofaringeos no Inverno, 122 na Primavera e 89 no Outono.
No Inverno, os tipos emm com maior prevalência foram o emm 12 (n=99, predominante no DCC 8), o emm
75 (n=31, predominante no DCC 12), o emm 1 (n=25, predominante no DCC 1), o emm 3 (n=22,
predominante no DCC 11) e o emm 6 (n=15, predominante no DCC 7) como se pode observar na tabela 4.
Tabela 4- Tipos emm identificados no Inverno (2001-03 e 2005-07).
2001 2002 2003 2005 2006 2007
DCC2
DCC4
DCC6
DCC7 DCC4 DCC6 DCC8 DCC2 DCC3 DCC4 DCC7 DCC11 DCC12 DCC1 DCC5 Total
n=isolados
emm 1 1 6 5 1 12 25
emm 3 10 12 22
emm 28 2 2 3 7
emm 78 1 1
emm 6 3 2 10 15
emm 94 1 1 2
emm 2 3 3
emm 75 7 2 1 2 19 31
emm 12 1 21 2 13 8 18 16 1 1 18 99
emm 4 1 1
emm st1815 1 1
emm 89 1 1
emm 64 1 1
Total n=isolados 1 9 13 10 8 5 23 2 15 9 29 30 20 14 21 209
Na Primavera, os tipos emm com maior prevalência foram o emm 1 (n=34, predominante no DCC 8), o emm
12 (n=32, predominante no DCC 1), o emm 3 (n=30, predominante no DCC 8) e o emm 89 (n=10, no DCC
5), como se pode observar na tabela 5.

25
Tabela 5- Tipos emm identificados na Primavera (2001-04 e 2007).
2001 2002 2003 2004 2007
DCC3
DDC4
DCC7 DCC8 DCC4 DCC5 DCC6 DCC1 DCC5 DCC8 DCC12 Total
n=isolados
emm 1 3 4 8 18 1 34
emm 3 7 10 13 30
emm 28 2 1 3
emm 78 1 1
emm 6 2 2
emm 94 0
emm 2 1 1 2
emm 75 1 1
emm 12 3 6 2 21 32
emm 89 10 10
emm 22 4 4
emm 4 2 1 3
Total n=isolados 13 6 11 17 6 10 6 21 11 20 1 122
No Outono, os tipos emm com maior prevalência foram o emm 12 (n=40, predominante no DCC 5), o emm
1 (n=18, predominante no DCC 7) e o emm 2 (n=12, no DCC 2), como se pode observar na tabela 6.
Tabela 6- Tipos emm identificados no Outono (2000, 2002 e 2003).
2000 2002 2003
DCC2 DCC2 DCC3 DCC5 DCC7 Total
n=isolados
emm 2 12 12
emm 1 2 4 12 18
emm 48 2 2
emm 12 9 29 2 40
emm 22 1 1
emm 4 5 5
emm 75 1 1 2
emm st4050 1 1
emm 77 8 8 Total
n=isolados 16 9 12 37 15 89
Também foram identificados dois novos sub-tipos emm, o emm 3.51 (cluster V) e o emm st4050 (cluster VI)
(anexo V).
3.8- Determinação do Coeficiente de Wallace
O cálculo do coeficiente de Wallace visa comparar os tipos atribuídos e explorar a concordância entre os
métodos de tipificação (41). Para comparar os métodos de PFGE e emm “typing” de 397 isolados
clonalmente relacionadas, submeteram-se os padrões/tipos no “site” www.comparingpartitions.info e os
resultados do coeficiente de Wallace (para um Intervalo de Confiança de 95%) demonstram que duas
estirpes que pertencem ao mesmo cluster têm 99,7% de probabilidade de terem o mesmo tipo emm
(Coeficiente de Wallace PFGE→emm= 0,997) e que duas estirpes com o mesmo tipo emm têm 47,9% de
probabilidade de pertencerem ao mesmo cluster (Coeficiente de Wallace emm→PFGE= 0,479) (anexo VI).

26
3.9- MLST- “Multilocus Sequense type”
3.9.1. Tipabilidade
O esquema de MLST para Streptococcus pyogenes para os 7 genes nativos (consultar Material e Métodos)
foi determinado para 44 isolados tendo-se obtido 12 sequências tipo diferentes, sendo a ST 36 a que
apresenta maior prevalência, n=12 (27,3%) como se pode observar na figura 16.
0 2 4 6 8 10 12
Nº de Isolados
ST 36
ST 150
ST 382
ST 28
ST 55
ST 46
ST 52
ST 15
ST 406
ST 39
ST 161
ST 408
Sequência
s T
ipo (
MLS
T)
Figura 16- Histograma de barras de 44 isolados que ilustra a distribuição das 12 ST.
3.9.2- “eBURST”
As ST do nosso estudo já eram conhecidas na base de dados do MLST [online] (28). Depois foram
analisadas pelo “software eBURST”- uma abordagem da sua filogenia.
No anexo VII encontra-se o relatório do “eBURST v3” (http://eburst.mlst.net/v3/mlst_datasets/) que
corresponde à análise de 2098 isolados, agrupados em 77 grupos e com 527 ST. Um grupo é um conjunto
de ST que partilham 6 ou mais alelos num total de 7, não podendo haver sobreposição das ST em grupos
diferentes.
No nosso estudo existe o complexo clonal 15, CC15, em que a ST 406 representa um SLV (“Single Locus
Variant”) do “predicted founder”3 ST 15, porque a ST 406 apresenta uma alteração de posição do alelo gtr,
ou seja, o alelo gtr da ST 406 ocupa a posição 29 e o da ST 15 ocupa a posição 6 (anexo VIII).
As ST 150, 52, 36, 55, 39, 28 e 46 correspondem aos próprios ancestrais (“predicted founder”),
respectivamente aos grupos G18, G13, G7, G41, G6, G2 e G8.
Quanto à ST 382 e à ST 408 correspondem, respectivamente, a um SLV do ancestral ST 37 e a um DLV
(“Double Locus Variant”) do ancestral ST 407.
3 “Predicted founder”- é a Sequência Tipo com maior número de SLVs e DLVs, ou seja, a ST “predicted founder” é aquela a partir da
qual se diversificam as ST que diferem em um ou dois dos 7 alelos. Regra geral a ST “predicted founder” é a que apresenta maior prevalência, maior valor “bootstrap” e menor distância em relação a todas as outras ST do grupo. Feil, E. J., et al., (29).

27
Por último, a ST 161 corresponde a um “singleton”, ou seja, uma sequência tipo que não se enquadra na
definição de grupo (figura 17).
A frequência (n=isolados) com que as ST foram identificadas no nosso trabalho apresenta a seguinte ordem
decrescente:
ST 36 (n=12) > ST 150 (n=6) > ST 28 (n=5), ST 382 (n=5) > ST 55 (n=4) > ST 46 (n=3) > ST 15 (n=2), ST
52 (n=2), ST 406 (n=2) > ST 39 (n=1), ST 161 (n=1), ST 408 (n=1).
3.9.3- Comparação de isolados de colonização de S. pyogenes com os da base de dados do
MLST
O aspecto mais importante é que as ST do nosso estudo correspondem a isolados da cavidade orofaringea
de crianças portadoras assintomáticas de S. pyogenes e as ST de S. pyogenes descritas no “site” do MLST
correspondem a isolados de outros produtos biológicos, como o sangue, as feridas, o tracto aéreo superior,
o líquido cefalo raquidiano, entre outras, ocorrendo em crianças e/ou adultos (36).
A tabela 7 resume a data, os locais e o tipo emm das ST encontradas no nosso estudo e no resto do
mundo. Também se indicam os fenótipos/genotipos de resistência a macrólidos detectados em estudos
portugueses.
Singleton
G41 G7
G6
G13
G18
G28
G9
G1
G8
G2
ST150/PFGE-ET/emm 75/Cluster XIII/ n=1 ST150/PFGE-EH,EQ/emm 75/Cluster XIV/ n=2 ST150/PFGE-EF/emm 75/Cluster VIII/ n=1 ST52/PFGE-ED,EL/emm 28/Cluster XIX/ n=2
ST382/PFGE-AD/emm 1 e 6/Cluster IX/ n=2 ST382/PFGE-DX, N/emm 6/Cluster IX/n=2
ST15/PFGE-BM,EM/emm 3/Cluster VI/ n=2 ST406/PFGE-BG/emm 3/Cluster V/ n=2
ST408/PFGE-AJ/emm 3/Cluster VI/ n=1
ST46/PFGE-A,B/emm 22/Cluster XVI/ n=2 ST46/PFGE-AU/emm 22/Cluster XXI/ n=1
ST28/PFGE-EK/emm 1/Cluster III/ n=1 ST28/PFGE-X/emm 1/Cluster IV/ n=3 ST28/PFGE-CX/emm 1/Cluster XX/ n=1
ST36/PFGE-AB, AP, BK, FW/emm 12/Cluster I/ n=7 ST36/PFGE-AB,AP/emm 12/Cluster II/ n=2 ST36/PFGE-DM/emm 12/Cluster XXIII/ n=1
CC 15
ST55/PFGE-BH/emm 2/Cluster X/ n=2 ST55/PFGE-DX/emm 2/Cluster XVIII/ n=1 ST55/PFGE-ES/emm 2/Cluster XXI/ n=1
ST39/PFGE-DF/emm 4/Cluster XII/ n=1
Figura 17 – Diagrama obtido pelo “software eBURSTv3“(http://eburst.mlst.net) que compara as Sequências Tipo da base de dados de MLST de Streptococcus pyogenes com os 44 isolados do nosso estudo. Os círculos maiores preenchidos a azul e a preto designam os “predicted founder” do grupo (G). Os círculos menores preenchidos a preto designam “SLV”. O círculo de cor amarelo designa um subgrupo. A seta a vermelho assinala as 12 ST encontradas no nosso estudo. CC15 designa o complexo clonal 15. Dos 44 isolados analisadas pelo eBURST apenas 39 apresentam mais de 80% de semelhança (dado obtido do dendrograma). As linhagens destes 39 isolados encontram-se apresentadas junto a cada grupo G correspondente.

28
Assim, a ST 36, com maior número de isolados identificados no nosso estudo, encontra-se distribuída por 4
continentes (tabela 7), enquanto que a ST 39, embora se encontre disseminada pelos 5 continentes, surge
num isolado do nosso estudo.
A ST 408 é a única que se confina a Portugal e com diferentes tipos emm: um isolado de um líquido cefalo
raquidiano (37) e outro encontrado no nosso estudo.
Em algumas ST, os tipos emm alteram no contexto espaço temporal, caso das ST 28, 36, 39, 52, 382, 406 e
408, como se pode observar na tabela 7.

29
Tabela 7- Localização geográfica das ST encontradas no nosso estudo.
ST Localização Geográfica
Data/Local/emm "type" (1ª Descrição) Década 90 Séc. XXI
Resistência a macrólidos (Portugal)
15
Europa, América e Egipto 1942/ EUA/ 3 Alemanha, Brasil, Egipto RC, Portugal
28
Euroásia e América do Norte 1932/ RU/ 1
Alemanha, Suécia, Finlândia, China, Japão, Taiwan, EUA
Nepal, Portugal, Polónia, RC, Alemanha(emm3,4, 28) Fenótipo M
a
36
Euroásia, Oceania e América 1956/ EUA/ 12
Alemanha(emm77), Polónia, Bélgica, Irlanda, Finlândia, Suíça, Itália, Etiópia, Turquia, China, Japão, Taiwan, Coreia do Sul, Brasil, Argentina, Peru, Chile, Canadá
Portugal, Índia, Grécia, Polónia, RC (emm44, 75)
Fenótipo/Genótipo
MLSB/ermB c
39
Euroásia, Oceania, América e África do Sul 1994/ EUA/ 4
Canadá, Taiwan (emm sts104), Suécia, Finlândia, Polónia, Alemanha, Itália
Espanha, Portugal, RU, RC, Hungria, Japão, África do Sul, Coreia do Sul, Nepal Fenótipo M
a
46
Eroásia, América e África do Sul 1986/ EUA/ 22
Portugal, Alemanha, Bélgica, França, Itália, Canadá, Brasil, Taiwan, Irlanda, RU, México
Portugal, Espanha, RU, RC Fenótipo MLSB
a
52
Euroásia e América do Norte 1995/ EUA/ 28
Alemanha, Canadá, Áustria, França, Hungria, Polónia, RC, Túrquia, Coreia do Sul
Portugal, Espanha(emm77), Grécia, RU, Alemanha, Polónia,
RC, Suécia b
Fenótipo MLSB e resistência
bacitracina a e
isolados
colonização d
55
Europa e América do Norte 1938/ RU/ 2 Bélgica, Alemanha, EUA Espanha, Portugal, RC,
150 Europa e Oceania 1993/ Espanha/ 75
Polónia, Alemanha, RU, RC, Austrália Portugal, Espanha, RC
161
Península Ibérica e México 1967/ Taiwan/ 48 México, Espanha, Portugal
382 Euroásia 1999/Espanha,Áustria/Rússia/ 6 Portugal(emm1 e 3), RC, Alemanha(emm1)
406 Europa 1999/ Alemanha/ 3 Portugal (emm107) Alemanaha, Espanha, Portugal
408 Portugal 2004/ Portugal/ 89 e Portugal (emm3)
EUA- Estados Unidos da América; RU- Reino Unido; RC- Repúplica Checa; Portugal- detectado em Portugal, em crianças portadoras assintomáticas de S. pyogenes.
a Silva-Costa, et al., 2006. Clin Microb Infect. 12: 513-518
b Eriksson, BK, et al., 2003. Clin Infect Dis. 37:1189-1193
c Siva-Costa, et al., 2008. Clin Microb Infect. 14: 1152-1159
d Pires, R., et al., 2009. FEMS Microb Lett. 296: 235-240
e Friães, A., et al., 2007. J Clin Microb. 45: 2044-2047

30
3.10- Linhagens Genéticas
Tendo por base 397 isolados com mais de 80% de semelhança dos perfis de macro-restrição do DNA,
obtidos por PFGE e com base em polimorfismos do gene emm (emm “typing”) e de genes nativos
(“Multilocus Sequence Typing”- MLST), definiram-se as linhagens genéticas, de acordo com a estação do
ano.
Assim, no Outono obtiveram-se cinco linhagens com mais de cinco isolados (n) nos respectivos DCCs:
→ PFGE-AB, AP/ emm 12/ ST 36, n=39, DCCs: 2, 5,7
→ PFGE-X/ emm 1/ ST 28, n=18, DCCs: 2, 3, 7
→ PFGE-BH/ emm 2/ ST 55, n=12, DCC 2
→ PFGE-BC/emm 77, n=5, DCC 5
→ PFGE-CZ, DF/ emm 4, n=5, DCC 3
E quatro linhagens, cada uma com um isolado, no respectivo DCC:
→ PFGE-B/ emm 22, DCC 3
→ PFGE-BM/ emm st4050, DCC 3
→ PFGE-DF/ emm 75/ ST 39, DCC 3
→ PFGE-ET/ emm 75/ ST 150, DCC 7,
No Inverno obtiveram-se sete linhagens com mais de três isolados (n) nos respectivos DCCs:
→ PFGE-AB, AP, BK, DM, FW, FZ/ emm 12/ ST 36, n=97, DCCs: 1, 2, 3, 4, 5, 6, 7, 8, 11, 12
→ PFGE-EF, EH, EQ/ emm 75/ ST 150, n= 28, DCCs: 3, 4, 6, 8, 12
→ PFGE-EK, X/emm 1/ ST 28, n= 25, DCCs: 1, 2, 4, 6, 7, 12
→ PFGE-AJ, BG/ emm 3/ ST 408, n= 21, DCCs: 6, 11
→ PFGE-AD, DX, N/ emm 6/ ST 382, n= 14, DCCs: 4, 6, 7
→ PFGE-AC, EL/ emm 28/ ST 52, n= 5, DCCs: 5, 7
→ PFGE-DK/ emm 2/ ST 55, n= 3, DCC 7
E quatro linhagens, cada uma com um isolado, no respectivo DCC:
→ PFGE-AD/ emm 1/ ST 382, DCC4
→ PFGE-EH/ emm st1815, DCC 8
→ PFGE-BE/ emm 89, DCC 4
→ PFGE-EP/ emm 94, DCC 4,
Na Primavera obtiveram-se oito linhagens com mais de dois isolados (n) nos respectivos DCCs:
→ PFGE-CX, X/ emm 1/ ST 28, n=33, DCCs: 3, 4, 5, 8
→ PFGE-AB, AP, DM/ emm 12/ ST 36, n=32, DCCs: 1, 4, 6, 8
→ PFGE-BG, BM, EM, ER/ emm 3/ ST 15, n=29, DCCs: 3, 7, 8
→ PFGE-BE, BF/ emm 89, n= 10, DCC 5
→ PFGE-A, AU, B/ emm 22/ ST 46, n=4, DCC 6
→ PFGE-CZ/ emm 4, n= 3, DCCs: 5, 8
→ PFGE-AD/ emm 6, n= 2, DCC 4
→ PFGE-BJ, ES/ emm 2/ ST 55, n=2, DCCs: 5, 8

31
E duas linhagens, cada uma com um isolado, no respectivo DCC:
→ PFGE-ED/ emm 28/ ST 52, DCC 7
→ PFGE-EH/ emm 75, DCC 8.
3.11- Poder Discriminatório e Intervalos de Confiança de PFGE, emm “typing” e MLST
A partir do “site” www.comparingpartitions.info é possível obter os histogramas, o índice de Simpson e os
Intervalos de Confiança (I.C.) para cada um dos métodos de tipificação.
Foram calculados os índices de diversidade de Simpson´s e os respectivos intervalos de confiança de 44
isolados de colonização para os três métodos de tipificação: PFGE, emm “typing” e MLST (tabela 8). A
comparação dos intervalos de confiança, para um nível de confiança de 95%, indicam que o emm “typing”
e o MLST apresentam um poder discriminatório muito semelhante, porque os intervalos de confiança
quase que se sobrepõem, enquanto que o PFGE apresenta um I.C. maior e consequentemente um maior
poder discriminatório. Comparando estes três métodos pode-se dizer que o emm “typing” e o MLST
possuem índices de diversidade semelhantes (0,875 e 0,881, respectivamente), enquanto que o PFGE
possui um índice de diversidade de Simpson´s maior (0,982). Quer isto dizer que duas estirpes, escolhidas
aleatoriamente, têm 98% de hipóteses de pertencerem a tipos diferentes, no caso do PFGE e 88% no
caso do emm “typing” e do MLST.
Tabela 8– Índice de Diversidade de Simpson´s (D), Intervalos de Confiança (I.C) e número de tipos obtidos por PFGE,
emm “typing” e MLST para 44 isolados de colonização por Streptococcus pyogenes.
Métodos Genotípicos D I.C. (95%) Nº de tipos PFGE 0,982 (0,967-0,997) 33 emm type 0,875 (0,824-0,926) 11 MLST 0,881 (0,828-0,933) 12
3.12- Inferência Estatística
3.12.1-Teste de independência do Qui-Quadrado- simulação de Monte-Carlo
Para responder a duas hipóteses diferentes: H1: não existe associação entre os clusters e os “Day Care
Centers- DCCs”, H2: não existe associação entre os clusters e as estações Primavera, Outono e Inverno
recorreu-se ao valor do teste exacto de Fisher que é consonante com a simulação de Monte-Carlo (38),
uma vez que os pressupostos do Qui-quadrado não se encontravam satisfeitos, nomeadamente o
pressuposto de que não deve haver mais do que 20% das células das frequências esperadas inferiores a
5 (anexo IX e X). Como referido anteriormente, o número total de estirpes clonalmente relacionadas foi de
397.
Assim, constata-se que a distribuição dos clusters varia consoante os DCCs, χ2 = 604,503, p=0,000
(anexo IX) e que a distribuição dos clusters varia consoante as estações da Primavera, Outono e Inverno,
χ2 = 275,313 p=0,000 (anexo X). A análise das diferenças foi efectuada com o apoio nos resíduos

32
ajustados estandardizados (39) aos quais corresponde uma prevalência. Por exemplo, na figura 18 pode-
se verificar que há uma proporção de estirpes mais elevada no cluster II e III do que o esperado no DCC 1
e na figura 19 verificou-se que há uma proporção de estirpes mais elevada nos clusters II, IV, X, XII e XV
do que o esperado no Outono.
DCC 1 DCC 2
Cluster II (58,8%, n=20), III (35,3%, n=12) Cluster X (46,2%, n=12)
DCC 3 DCC 4
Cluster VI (20,6%, n=7), XII (17,6%, n=6), XX (8,8%, n=3) Cluster IX (14,7%, n=5), XIII (14,7%, n=5),
DCC 5 XXII (2,9%, n=1), XXIII (5,9%, n=2)
Cluster II (26,7%, n=20), VII (12%, n=9), XI (12%, n=9) DCC 6
XV (6,7%, n=5), XVII (4%, n=3) Cluster V (42,9%, n=9), XIV (9,5%, n=2)
DCC 7 XVI (14,3%, n=3), XXI (4,8%, n=1)
Cluster IV (18,8%, n=12), V (15,6%, n=10), IX (15,6%, n=10) DCC 8
XVIII (3,1%, n=2), XIX (4,7%, n=3) Cluster III (21,7%, n=13), V (21,7%, n=13)
DCC 11 XIV (5%, n=3)
Cluster I (53,6%, n=15), VI (42,9%, n=12) DCC 12
Cluster VIII (90,5%, n=19) Figura 18- O(s) cluster(s) indicado(s) por baixo de cada DCC são aquele(s) cuja prevalência é significativamente
diferente dos demais clusters presentes nesse DCC. A prevalência e o nº de isolados do cluster encontram-se
indicados entre parêntesis. A robustez do teste do Qui-Quadrado foi melhorada com a simulação de Monte-Carlo
tendo-se utilizado o intervalo de confiança de 99 %.
DCC 12
DCC 3
DCC 1 DCC 2
DCC 4
DCC 5
DCC 8
DCC 7
DCC 6
DCC 11

33
Figura 19- Os clusters indicados em cada uma das três estações do ano são aqueles cuja prevalência é
significativamente diferente dos demais clusters presentes nessa estação. A prevalência e o nº de isolados do cluster
encontram-se indicados entre parêntesis. A robustez do teste do Qui-Quadrado foi melhorada com a simulação de
Monte-Carlo tendo-se utilizado o intervalo de confiança de 99 %
Outono Clusters: II (25,3%, n=21), IV (21,7%, n=18), X (14,5%, n=12), XII (7,2%, n=6), XV (6,0%, n=5)
Primavera Clusters: II (17,1%, n=20), III (14,5%, n=17), V (19,7%, n=23), XI (7,7%, n=9), XVI (2,6%, n=3), XX (2,6%, n=3), XXI (1,7%, n=2)
Inverno
Clusters: I (37,6%, n=74), VIII (9,6%, n=19), VII (8,1%, n=16),
IX (7,6%, n=15), XVII (2,0%, n=4)

34
4 - Discussão/Conclusão
A elevada taxa de colonização observada neste trabalho (14%) também foi observada num estudo com
crianças saudáveis, em idade escolar, na Turquia e segundo os autores pode ser devido ao contacto
prolongado entre as crianças de uma mesma escola e sala (40). Os mesmos autores (40) referem ainda
outros factores de risco para a disseminação de Streptococcus do Grupo A, tais como, o uso de
antibióticos, as condições sanitárias e o contacto das crianças com os funcionários e familiares.
Este facto pode explicar-se tendo em conta os padrões de PFGE, uma vez que dos 420 isolados de
colonização, 397 (94,5%) são clonamente relacionados. Apenas 23 isolados (5,5%) não apresentam
qualquer relação clonal.
A análise entre os padrões de PFGE que formam clusters (397 isolados) e os tipos emm é extremamente
importante. A determinação do coeficiente de Wallace PFGE→emm type demonstrou que se duas estirpes
pertencem ao mesmo cluster, definido por PFGE, há 99,7% de probabilidade de terem o mesmo tipo emm
(41).
Atendendo aos histogramas de tipabilidade de PFGE, de emm “type” e de MLST, o padrão, o tipo emm e a
ST mais frequente é o padrão AB, o emm 12 e a ST 36 que se encontram no cluster I, II e VII, num total de
95 isolados, correspondendo a 24% (n=95/397) de todos os isolados clonalmente relacionados. O cluster
E do estudo de Friães, A., et al., (37) corresponde ao cluster I, II e VII do nosso estudo. O cluster E é,
segundo os autores, mais frequente entre os isolados de doentes pediátricos, com doença invasiva e com
idades ≤ 18 anos. Por outro lado, em Tóquio, o tipo emm 12 corresponde ao tipo M 12, mais abundante
em crianças saudáveis em idade escolar (42). Nos clusters I, II e VII também se detectou o padrão AP e o
tipo emm 12, num total de 51 isolados (13%).
Com a segunda frequência mais elevada surge o padrão X e o tipo emm 1 que se encontram no cluster III
e IV, num total de 68 isolados (17%) e com a terceira frequência mais elevada surge um conjunto
heterogéneo de padrões de PFGE (BG, ER/ AJ, BM, EM) e o tipo emm 3, detectados nos clusters V e VI,
num total de 50 isolados o que corresponde a 13% de todos os isolados clonalmente relacionados. Neste
caso, há a salientar que no cluster V, a ST 406/PFGE-BG/emm 3 e no cluster VI, a ST 15/PFGE-EM,
BM/emm 3 formam o complexo clonal 15 (figura 17), o que significa que a maior parte dos tipos emm
define os clones ou complexos clonais (41, 43). As diferenças entre os padrões de PFGE observadas
neste complexo clonal podem ser devidas a inserções ou a delecções ou a mutações de DNA (35). A este
respeito, os autores (44) referem as ST relacionadas em que há alteração num só alelo dos 7 genes
nativos deverá ser analisada, no sentido de distinguir se o “Single Locus Variant” [ST 406] ocorreu por
recombinação ou mutação. Enright, M.C, et al., (43) acrescentaam que as mutações nos genes nativos
são amplamente assumidas como selectivamente neutras.
À excepção da ST 408, as demais ST encontradas neste estudo correspondem ao ancestral de cada
complexo clonal.
Quando se recorre à base de dados do MLST (http://spyogenes.mlst.net) pode-se comparar as ST com os
tipos emm e a sua distribuição pelo mundo.

35
A ST 382 detectada pela primeira vez em 1999, na Euroásia, com o tipo emm 6 em doenças do tracto
aéreo superior, no nosso estudo surge com o tipo emm 6 (3 estirpes), emm 3 (1 estirpe) e emm 1 (1
estirpe) (anexo VIII). Esta heterogeneidade do gene emm e das suas proteínas M antigénicas reflecte o
impacto do sistema imunitário de hospedeiro na diversificação dos tipos emm de S. pyogenes (43, 44). A
ST 382, com o tipo emm 1 também foi identificada na Alemanha em doente com celulite.
Algumas ST que se encontram no nosso estudo foram encontradas há muitas décadas atrás. Por
exemplo, a ST 28 e a ST 55 já haviam sido encontradas no Reino Unido na década de 30, bem como a ST
15 e a ST 36, encontradas nos EUA, associadas a patologias do tracto aéreo superior, nas décadas de 40
e 50, respectivamente.
Em relação à ST 408, os dados do “site” do MLST indicam só ter sido encontrada em Portugal: em 2004
num líquido cefalo-raquidiano, com o tipo emm 89 (37) e em 2006 no nosso estudo, com o tipo emm 3. A
comparação dos géis de PFGE destas duas estirpes revelou padrões de PFGE diferentes com a mesma
ST 408, o que pode estar relacionado com fenómenos de delecção, de inserção ou de mutação de DNA
(35).
Das ST encontradas no nosso estudo, a ST 39 é a única que se encontra distribuída mundialmente.
A comparação das 12 ST do nosso estudo com as referenciadas no “site” do MLST permite-nos afirmar
que as nossas ST são as únicas associadas a colonização.
A inferência estatística demonstrou haver relação entre os clusters e os “Day Care Centers” DCCs
(hipótese 1) e entre os clusters e as três estações do ano (hipótese 2).
Os DCCs podem ser considerados um conjunto de hospedeiros onde há permanentemente introdução de
novos clones e onde os mais aptos persistem e se disseminam (45).
No caso do DCC 5, o comportamento epidemiológico das estirpes PFGE-AC/emm 28 resistentes à
bacitracina, em isolados de colonização, tal como foi detectado no estudo de Pires, R. et al., (22) sugere a
existência de elementos genéticos móveis, considerados a principal fonte de factores de virulência de
Streptococcus do Grupo A (46). Na linhagem emm 28/ ST 52, dos autores (22) detectaram a presença do
gene SpeC e a ausência do gene SpeA que são exotoxinas pirogénicas que se localizam em elementos
genéticos móveis.
Um estudo de prevalência como o nosso torna-se importante. Por exemplo, a frequência dos tipos emm é
extremamente útil no cálculo da eficácia de uma vacina multivalente (“26-valent vacine”) para o
Streptococcus do Grupo A, como descrito por O´Loughlin, R.E., et al. (47).
Em relação ao desenvolvimento duma vacina para prevenir a infecção pelo GAS, os mesmos autores (47)
referem que esta deveria incluir os tipos emm 1, 3 e 12. Dos 26 tipos emm incluídos na vacina, 11 deles
foram encontrados no nosso estudo (emm 1, 2, 3, 6, 12, 22, 28, 75, 77, 89, 94).
Pensamos que este estudo tenha contribuído para o conhecimento mais aprofundado do estado de
portador de S. pyogenes, em particular em crianças e grupos de contacto, no entanto, no sentido de
melhor compreender os factores responsáveis pela elevada taxa de colonização observada nas
Creches/Jardins de Infância do nosso estudo, seria importante realizar um estudo longitudinal numa só

36
Creche/Jardin de Infância, em crianças, durante um ano e empregando os métodos fenotípicos e
genotípicos recomendados para isolados de S. pyogenes.

37
5 - Referências
1. Facklam, R. R. 2002. What happened to the Streptococci: overview of taxonomic and nomenclature changes.
Clinical Microbiology Reviews. 15: 613-630.
2. Stckebrandt, E., Goebel, B.M. 1994. Taxonomic note: a place for DNA-DNA reassociation and 16S rRNA
sequence analysis in the present species definition in bacteriology. Int. J. Syst. Bacteriol. 44: 846-849.
3. Kawamura, Y., Hou, X-G., Sultana, F., Miura, H., Ezaki, T. 1995. Determination of 16S rRNA sequences of
Streptococcus mitis and Streptococcus gordonii and phylogenetic relationships among members of the genus
Streptococcus. International Journal of Systematic Bacteriology. 45: 406-408.
4. Cruickshank, R., Duguid, J.P., Marmion, B.P., Swain, R.H. 1975. Microbiologia Médica. 5ª Edição. Fundação
Calouste Gulbenkian. p.721.
5. Cunningham, M. W. 2000. Pathogenesis of group A streptococcal infections. Clinical Microbilogy Reviews. 13:
470-511.
6. Virulence Factors of Pathogenic Bacteria. (http://www.mgc.ac.cn/cgi-
bin/VFs/genus.cgi?Genus=Streptococcus#S.pyogenes-genes).
7. Bisno, A. L., Brito, M. O., Collins C. M. 2003. Molecular basis of group A streptococcal virulence. The Lancet
Infectious Diseases. 3: 191- 200.
8. Madigan, M. T., Martinko, J. M., Dunlap, P.V., Clark, D. P. 2009. Brock- Biology of Microorganisms. Pearson
Benjamin Cummings.
9. Hoe, N.P., Fullerton, K.E., Liu, M., Peters, J. E., Gackstetter, G.D., Adams, G.J, Musser, J.M. 2003. Molecular
genetic analysis of 675 Group A Streptococcus isolates in a carrier study at Lackland Air Force Base, San Antonio,
Texas. Journal of Infectious Diseases. 188: 818-827.
10. Pádua, M. M. 2009. Patologia Clínica para Técnicos. Tomo I- Bacteriologia. Lusociência. Edições Técnicas e
Científicas, Lda.
11. Wu, H-J., Wang, H-J. A. & Jennings, M. P. 2008. Discovery of virulence factors of pathogenic bacteria. Chemical
Biology. 12:1–9.
12. Nir-Paz, R.,Korenman, Z., Ron, M., Michael-Gayego, A., Cohen-Poradosu, R., Valinsky, L., Beall, B., Moses,
A.E. 2010. Streptococcus pyogenes emm and T types within a decade, 1996-2005: implications for epidemiology
and future vaccines. Epidemiol. Infect. 138: 53-60.
13. Fischetti, V. A. 1989. Streptococcal M protein: molecular design and biological behaviour. Clinical Microbiology
Reviews. 2: 285-314.
14. Khandke, K. M., Fairwell, T., Acharya, A.S., Trus, B.L., Manjula, B.N. 1988. Complete amino acid sequence os
streptococcal PepM49 protein, a nephritis associated serotype: conserved conformational design sequentially
distinct M protein serotypes. J. Biol. Chem. 263: 5075-5082.
15. Ferreira, W., Sousa, J. 2000. Microbiologia. Lidel Editora. 2: 51-62.
16. Steer, A. C., Danchin, M. H., Carapetis, J. R. 2007. Group A streptococcal infections in children. Journal of
Paediatrics and Child Health. 43: 203-213.
17. Johnson, D. R., Stevens, D. L., Kaplan, E. L. 1992. Epidemiologic analysis of group A streptococcal serotypes
associated with severe systemic infections, rheumatic fever, or uncomplicated pharyngitis. J. Infect Dis. 166: 374-
382.
18. Fernie-King, B.A., Seilly, D.J., Davies, A., Lachmann, P.J. 2002. Streptococcal inhibitor of complement inhibits
two additional components of the mucosal innate immune system: secretory leukocytes proteinase inhibitor and
lysozyme. Infect Immun. 70: 4908-4916.
19. Mitchell, T. J., 2003. The pathogenesis of streptococcal infections: from tooth decay to meningitis. Microbiology.
Reviews. Vol 1: 219-230.

38
20. Snellman, L.W., Stang, H.J., Stang, J. M., Johnson, D.R., Kaplan, E.L. 1993. Duration of positive throat cultures
for group A streptococci after initiation of antibiotic therapy. Pediatrics. 91(6):1166-1170.
21. Sanches, I., Pires, R., Rolo, D., Esteves, F., Almeida, J.F., Mato, R., Valadares, I., Ramos, T., Gameiro, C.,
Andrade, C., Lopes, A., Rosas, J., Ferreira, E., Romeiro, L., Vaz, F., Morais, A., Brito-Avô, A., Gonçalo-
Marques, J.,2009. Oropharyngeal colonization by Group A Streptococci in Portugal: eight-year surveillance study
(2000-20007). Poster. 19 th European Congress of Clinical Microbiology and Infectious Diseases (ECCMID). 16-
19 May. Helsinki/Finland.
22. Pires, R., Rolo, D., Mato, R., Almeida, J.F., Johansson, C., Henriques-Normark, B., Morais, A., Brito-Avô, A.,
Gonçalo-Marques, J., Sanches, I.S. 2009. Resistance to bacitracin in Streptococcus pyogenes from
orofharyngeal colonization and noninvasive infections in Portugal was caused by two clones of distint virulence
genotypes. FEMS Microbiol Lett. 296: 235-240.
23. Chung, M., Lencastre, H., Matthews, Peter., Tomasz, A., Adamsson, I., Sousa, M.A., Camou, T., Cocuzza,
C., Corso, A., Couto, I., Dominguez, A., Gniadkowski, M., Goering, R., Gomes, A., Kikuchi, K., Marchese, A.,
Mato, R., Melter, O., Oliveira, D., Palácio, R., Sá-Leão, R., Sanches, I., Song, J-H., Tassios, P.T., Villari, P.
2000. Molecular typing of methicillin resistant Staphylococcus aureus by pulsed field gel electrophoresis:
comparison of results in a multilaboratory effort using identical protocols and MRSA strains. Microb. Drug Resist 6:
189-198.
24. Tenreiro, R. P. A. 1995. Análise Taxonómica em Leuconostoc oenos- uma perspectiva polifásica. Dissertação de
Doutoramento em Microbiologia, pela Faculdade de Ciências da Universidade de Lisboa. p.297.
25. Centers for Disease Control e Prevention. [Online]. 2006. CDC emm sequence database.
(http://www.cdc.gov/ncidod/biotech/strep/protocol_emm-type.htm).
26. Centers for Disease Control and Prevention. [Online]. . (http://www.cdc.gov/ncidod/biotech/stre/strepblast.htm).
27. Maiden, M. C. J., 2006. Multilocus sequence typing of Bacteria. Annual Review of Microbiology. 60: 561-588.
28. MLST- Multilocus Sequence Typing. [Online]. (http://spyogenes.mlst.net)
29. Feil, E. J., Li, B. L., Aanensen, D.M., Hanage, W.P., Spratt, B. G. 2004. eBURST: Inferring patterns of
evolutionary descent among clusters of related bacterial genotypes from Multilocus Sequence Typing data. Journal
of Bacteriology.186: 1518-1530.
30. Tibayrenc, M. 2007. Encyclopedia of infectious diseases: modern methodologies. John Wiley & Sons, Inc.,
Hoboken, New Jersey. p.496-508. (disponível: http://books.google.pt/books?id=8iVnEZe-
zzkC&pg=PA502&lpg=PA502&dq=eBURST&source=bl&ots=xlWZZcOLbW&sig=Zy3B4pVJB22l5v_QYug3Z5emC
L8&hl=ptPT&ei=INOTd3GLsyFhQfGuvnuDg&sa=X&oi=book_result&ct=result&resnum=6&ved=0CDEQ6AEwBTg
K#v=onepage&q=eBURST&f=false).
31. Leclercq, R. 2002. Mechanisms of resistance to macrolides and lincosamides: nature of the resistance elements
and their clinical implications. Clinical Infectious Diseases. 34: 482-492.
32. Hunter, P.R., Gaston, M.A. 1988. Numerical index of the discriminatory ability of typing systems: an application of
Simpson´s index of diversity. Journal of Clinical Microbiology. 26: 2465-2466.
33. Van Belkum, A., Tassios, P.T., Dijkshoorn, L., Haeggman, S., Cookson, B., Fry, N.K., Fussing, V., Green, J.,
Feil, E., Gerner-Smidt, P., Brisse, S., Struelens, M. 2007. Guidelines for the validation and application of typing
methods for use in bacterial epidemiology. Clinical Microbiology and Infectious Diseases. 13: 1-46.
34. Grundmann, H., Hori, S., Tanner, G. 2001. Determining confidence intervals when measuring genetic diversity
and the discriminatory abilities of typing methods. Journal of Clinical Microbiology. 39: 4190-4192.
35. Tenover, F. C., Arbeit, R.D., Goering, R.V., Mickelsen, P. A., Murray, B. E., Persing, D.H., Swaminathan, B.
1995. Interpretation chromosomal DNA restriction patterns produced by Pulsed Field Gel Electroforesis: criteria for
bacterial strain typing. Journal of Clinical Microbiology. 33: 2233-2239.

39
36. Young, U., Hwang, G.Y., Jang, I.H., Cho, H.M., Noh, S.M., Kim, H.Y., Kwon, O. 2007. Macrolide resistance
trends in β-hemolytic streptococci in a tertiary Korean hospital. Yonsei Med J. 48: 773-778.
37. Friães, A., Ramirez, M., Melo-Cristino, J. 2007. Nonoutbreak surveillance of group A streptococci causing
invasive diseases in Portugal identified internationally disseminated clones among members of a genetically
heterogeneous population. Journal of Clinical Microbiology. 45: 2044-2047.
38. Marôco, J. 2007. Análise estatística com utilização do SPSS, Edições Sílabo, 3ª edição, Lisboa.
39. Pestana, M.H. e Gageiro, J.N. 2008. Análise de dados para ciências sociais- a complementaridade do SPSS,
Edições Sílabo, 5ª edição, Lisboa.
40. Durmaz, R., Durmaz, B., Bayraktar, M.., Ozerol, I.H., Kalcioglu, M.T., Akatas, E., Cizmeci, Z. 2003. Prevalence
of Group A Streptococcal carriers in asymptomatic children and clonal relatedness among isolates in Malatya,
Turkey. Journal of Clinical Microbiology. 41: 5285–5287.
41. Carriço, J.A., Silva-Costa, C., Melo-Cristino, J., Pinto, F.R., de Lencastre, H., Almeida, J.S., Ramirez, M.
2006. Illustration of a common Framework for relating multiple typing methods by application to macrolide-resistant
Streptococcus pyogenes. J. of Clin. Microbiology. 44: 2524-2532.
42. Iimura, T., Kashiwagi, Y., Endo, M., Amano, Y. 2006. Prevalence and persistence of certain serologic types of
Streptococcus pyogenes in metropolitan Tokyo. J. Infect. Chemother. 12: 53-62.
43. Enright, M. B., Spratt, B.G., Kalia, A., Cross, J.H., Bessen, D.E. 2001. Multilocus sequence typing of
Streptococcus pyogenes and the relationships between emm type and clone. Infect. Immun. 69: 2416-2427.
44. McGregor, K.F., Spratt, B.G., Kalia, A., Bennett, A., Bilek, N., Beall, B., Bessen, D.E. 2004. Multilocus
Sequence Typing of Streptococcus pyogenes representing most known emm types and distinctions among
subpopulation genetic structures. Journal of Bacteriology. 186: 4285-4294.
45. Sá-Leão, R., Nunes, S., Brito-Avô, A., Alves, C.R., Carriço, J.A., Saldanha, J., Almeida, J.S., Santos-
Sanches, I., Lencastre, H. 2008. High rates of transmission of and colonization by Streptococcus pneumoniae
and Haemophilus influenzae within a Day Care Center revealed in a longitudinal study. Journal of Clinical
Microbiology. 46: 225-234.
46. Beres, S.B., Musser, J.M., 2007. Contribution of Exogenous Genetic Elements to the Group A Streptococcus
Metagenome. PLoS One. 2(8):e800.
47. O’Loughlin, R.E., Roberson, A., Cieslak, P.R., Lynfield R., Gershman, K., Craig, A., Albanese, B.A., Farley,
M.M., Barrett, N.L., Spina, N.L., Beall, B., Harrison, L.H., Reingold, A., Beneden, C.V., for the Active
Bacterial Core Surveillance Team. 2007. The Epidemiology of Invasive Group A Streptococcal Infection and
Potential Vaccine Implications: United States, 2000–2004. Clinical Infectious Diseases. 45:853–862.

40
6 – Anexos

41

42

43
Anexo II
Tabela 1- Nº de portadores, de participantes e taxas de colonização de 10 “Day Care Centers” (DCC). MÊS
ANO DCC Nº Portadores Nº
Participantes Taxa de
colonização (%)
Out 2000 2 16 49 33
Mar 2001 4 9 39 23
Abr 2001 6 13 47 28
Mai 2001 7 11 76 14
Jun 2001 3 13 61 21
Jun 2001 4 6 33 18
Jun 2001 7 11 62 18
Fev 2002 6 5 25 20
Fev 2002 8 23 112 21
Fev 2002 4 8 55 15
Maio 2002 8 17 95 18
Out 2002 7 15 61 25
Out 2002 2 9 52 17
Out 2003 5 37 79 47
Fev 2003 3 16 55 29
Fev 2003 4 9 45 20
Maio 2003 6 6 26 23
Maio 2003 5 10 65 15
Maio 2003 4 6 37 16
Out 2003 3 12 82 15
Maio 2004 1 22 74 30
Maio 2004 5 12 55 22
Maio 2004 8 19 92 21
Fev 2005 7 29 59 49
Mar 2006 11 30 89 34
Mar 2006 12 20 127 16
Mar 2007 5 21 74 28
Mar 2007 1 15 96 16
Total 420 1822

44
Anexo III
Materiais usados na Electroforese em Gel de agarose por Campo Pulsado
Meios de Cultura
Propagação das culturas: Meio sólido TSA (“Trytic Soy Agar”, Difco, Becton, França) suplementado com 5% de sangue de carneiro (Probiológica, Portugal) -Pesar 30,4 g de TSA -Adicionar 760 ml água desmineralizada - Autoclavar a 120ºC durante 20 min - Armazenar a 50ºC - Adicionar 40 ml de sangue de carneiro - Distribuir 20 ml de meio de cultura por cada placa - Após solidificação do meio, conservá-las a 4º C. Meio líquido BHI (“Brain Heart Infusion Broth”, Biokar Diagnostics) - Pesar 37 g de BHI - Adicionar 1 l de água desmineralizada - Autoclavar a 121ºC durante 15 min - Armazenar à temperatura ambiente Meio líquido “Todd-Hewitt” (Oxoid) - Preparado em frascos Schott, de acordo com as instruções do fabricante - Autoclavar a 120ºC, 20 min - Guardar à temperatura ambiente
Tampões e Soluções
Tampão PIV: 10 mM Tris pH 8, 0; 1 M NaCl (Chung et al., 2000) Para preparar 500 ml de PIV - Adicionar 5 ml de 1 M Tris pH 8,0 - Pesar 29, 2 g de Nacl (Merck) - Adicionar água bidestilada até perfazer 500 ml - Autoclavar a 121ºC durante 15 min 1 M Tris pH 8,0 (1 l) - Pesar 121,1 g de Trizma - Adicionar 800 ml de água destilada - Ajustar o pH a 8,0, adicionando 42 ml de HCl. - Perfazer com água destilada até 1 l - Autoclavar a 121ºC durante 15 min Solução stock de TE 10X - 10 ml de 1 M Tris pH 7,5 para obter a concentração final de 100 mM Tris pH 7,5 - 2 ml de 0,5 M EDTA a pH 8,0 para obter a concentração final de 10 mM EDTA pH 8,0 - Adicionar 988 ml de água bidestilada e autoclavar Solução de TE 1 X - Para obter as concentrações finais de 10 mM Tris a pH 7,5 e 1 mM EDTA a pH 8,0, adicione - 100 ml de TE 10X e 900 ml de água bidestilada e autoclavar. 0,5 M EDTA pH 8,0 (1l) - Pesar 186,1 g de EDTA (sal dissódico, massa molecular 372,2) - Adicionar 800 ml de água destilada - Ajustar o pH a 8,0, adicionando 20 g de NaOH - Adicionar água bidestilada até perfazer 1l - Autoclavar Solução EC Preparar 500 ml de EC: Concentração final Concentração stock 6 mM Tris pH 8,0 3 ml, 1M Tris pH 8,0 1 M NaCl (Merck) 29,2 g NaCl 100 mM EDTA pH 8,0 100 ml, 0,5 M EDTA pH 8,0 0,2% Sarcosil (Sigma-Aldrich) 1 g, Na desoxicolato 0,5% Sarcosil (Sigma-Aldrich) 2,5 g Sarcosil 0,5% Brij 58 (Sigma-Aldrich) 2,5 g Brij 58 - Adicionar água bidestilada até perfazer 500 ml e autoclavar

45
Solução EC+ Lisozima+ Mutanolisina+ RNAse Lisozima a 1 mg/ml em TE 1X Concentração final Concentração stock 1 mg/ml 10 mg/ml A solução de Lisozima (Sigma-Aldrich) é preparada em TE 1X, filtrada com um filtro Milipore 0,45 µm) e armazenada em alíquotas a -20ºC. Mutanolisina a 5 U/ml Concentração final Concentração stock 5 U/µl 5 U/ml A mutanolisina é ressuspendida em tampão fosfato de potássio a 0,1 M (Sambrook et al., 1989) e armazenada em alíquotas a -20ºC. RNAse a 50 µg/ml Concentração final Concentração stock 50 µg/ml 10 mg/ml A RNAse (sigma-Aldrich) é preparada em água bidestilada, aqecida a 100ºC durante 15 min, arrefecida à temperatura ambiente, distribuída em alíquotas e armazenada a -20ºC. Solução ES+ Proteinase K Solução ES Para preparar 500 ml de ES: - Adicionar 5 g de lauril-sarcosinato de sódio (Sigma- Aldrich) a 500 ml de EDTA Na2 pH 9,0 - Perfazer com água destilada e autoclavar Proteinase K a 1 mg/ml (Roche) - Pesar e adicionar à solução ES só no próprio dia de uso Equilíbrio dos discos de DNA em tampão pré-SmaI - Diluir a 1/10: um volume de tampão pré-SmaI 10x T (Takara) com 9 volumes de água mili-Q autoclavada - Adicionar, na proporção 6,3 µl de β-mercaptoetanol (Sigma-Aldrich) para 15 ml de tampão 10x T (Takara). Nota: A diluição do tampão pré-SmaI da Invitrogen é a mesma (1/10) Tampão TBE 0,5X A 110 ml de TBE 10X (BioRad) adicionar 2090 ml de água bidestilada e autoclavar a solução Solução de coloração do gel Em 300 ml de água bidestilada autoclavada adicionar 25 µl de solução stock de Brometo de etídeo a 10 mg/ml (BioRad). Conservar a 4ºC na ausência de luz. Solução de Azul de Bromofenol 0,25% de Azul de Bromofenol 40% (W/V) de sacarose (Merck) em água bidestilada Solução para coloração do gel - Pipetar 25 µl de solução stock de Brometo de Etídeo a 10 mg/ml (BioRad) - Adicionar 300 ml de água bidestilada autoclavada - Conservar a solução na ausência de luz
Endonuclease de restrição - SmaI 10 U/µl (Takara) - SmaI 20 U/µl (Invitrogen)
Marcador de peso molecular - Lambda Ladder PFGE Marker, 50 µg/ml (New England BioLabs)
Agaroses Preparação dos discos de agarose: Agarose LMP (“Low Melting Point”, Sigma) a 1,5% - Pesar 1,5 g de agarose LMP - Adicionar 100 ml de PIV - Colocar no microondas até dissolver a agarose (1 a 2 min) e conversar a 42ºC Agarose Seaplaque (Cambrex) a 1,5% - Pesar 1,5 g de agarose Seaplaque - Adicionar 100 ml de PIV - Colocar no microondas até dissolver a agarose (1 a 2 min) e conversar a 42ºC Preparação do gel para colocação dos discos de DNA: Agarose Seakem LE (Cambrex) - Pesar 2 g de agarose Seakem LE - Adicionar 200 ml de TBE a 0,5% autoclavado - Colocar no microondas até dissolver a agarose (1 a 2 min) - Arrefecer e distribuir pelo tabuleiro do aparelho de PFGE

46
Anexo IV
Tabela 1-Estirpes resistentes à bacitracina
Strain code Our code Adult/ Child
Sex Age Room Month Year Bac Macrolides emm-type T-type Sma I DCC
GAP 634 CSO 7127 Child F 2 11G Mar. 2006 R cMLSb emm 28.0 T 28 F DCC 11
GAP 650 CSO 7176 Child M 4 11I Mar. 2006 R cMLSb emm 28.0 T 28 F DCC 11
GAP 1005 CSO 7279 Child M 5 5Z Mar. 2007 R cMLSb emm 28 AC DCC 5
GAP 1006 CSO 7281 Child F 5 5Z Mar. 2007 R cMLSb emm 28 AC DCC 5
GAP 1007 CSO 7284 Child F 5 5Z Mar. 2007 R cMLSb emm 28 AC DCC 5
Anexo V
Tabela 1- Novos sub-tipos emm identificados no DCC 8.
Strain code
Our code Adult/ Child
Sex Age Room month Year Bac emm-type T-type Sma I DCC
GAP 933
CSO 2424 Child F 4 8D May. 2002 S emm 3.51 T 3,13 ER DCC 8
GAP 919
CSO 1865 Child M 5 8E Feb. 2002 S emm st1815.0 EH DCC 8
Anexo VI
Tabela 1- Determinação do Coeficiente de Wallace de 397 isolados (www.comparingpartitions.info)
Wallace and 95% CI
Sma I emm
Wi 0.116 0.242
Sma I 0.997 (0.995-1.000)
emm 0.479 (0.432-0.525)

47
Anexo VII
eBURST Report - Tue Jan 11 20:35:07 GMT 2011 No. isolates = 2098 | No. STs = 527 | No. re-samplings for bootstrapping = 1000 No. loci per isolate = 7 | No. identical loci for group def = 6 | No. groups = 77 Group 1: No. Isolates = 84 | No. STs = 15 | Predicted Founder = 407 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 407 4 7 6 1 0 1.57 95% 96% 101 45 4 7 3 0 1.92 25% 53% 77 4 3 7 3 1 2.14 8% 1% 253 10 3 6 4 1 2.21 6% 20% 408 1 3 3 6 2 2.5 10% 12% 384 4 2 8 4 0 2.14 0% 0% 76 1 2 8 3 1 2.21 0% 0% 568 1 2 4 6 2 2.57 0% 0% 79 1 2 3 6 3 2.78 0% 0% 390 1 1 6 7 0 2.42 0% 0% 78 1 1 6 6 1 2.5 0% 0% 466 1 1 5 7 1 2.57 0% 0% 142 8 1 3 8 2 2.78 0% 0% 409 1 1 2 6 5 3.14 0% 0% 553 1 1 2 4 7 3.35 0% 0% Group 2: No. Isolates = 198 | No. STs = 14 | Predicted Founder = 28 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 28 183 6 2 3 2 2.07 84% 87% 225 1 4 4 5 0 2.07 46% 37% 530 1 2 8 3 0 2.07 0% 0% 415 1 2 6 3 2 2.38 0% 0% 567 1 2 5 2 4 2.61 0% 0% 542 1 2 5 2 4 2.61 0% 0% 93 3 2 4 5 2 2.53 1% 0% 106 1 2 3 4 4 2.76 0% 0% 107 1 2 2 5 4 2.84 0% 0% 94 1 2 1 3 7 3.30 6% 0% 445 1 1 6 3 3 2.76 0% 0% 440 1 1 5 2 5 3.0 0% 0% 443 1 1 3 5 4 2.92 0% 0% 372 1 1 2 3 7 3.38 0% 0% (…) Group 6: No. Isolates = 161 | No. STs = 8 | Predicted Founder = 39 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 39 134 6 1 0 0 1.14 98% 94% 38 13 2 5 0 0 1.71 0% 0% 423 7 2 4 1 0 1.85 0% 0% 373 2 2 4 1 0 1.85 0% 0% 566 1 2 4 1 0 1.85 0% 0% 422 1 2 4 1 0 1.85 0% 0% 421 1 1 5 1 0 2.0 0% 0% 391 2 1 1 5 0 2.57 0% 0% Group 7: No. Isolates = 112 | No. STs = 8 | Predicted Founder = 36 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 36 103 7 0 0 0 1.0 99% 99% 543 1 2 5 0 0 1.71 0% 0% 425 1 2 5 0 0 1.71 0% 0% 436 1 2 5 0 0 1.71 0% 0% 366 1 2 5 0 0 1.71 0% 0% 551 2 1 6 0 0 1.85 0% 0% 465 2 1 6 0 0 1.85 0% 0% 467 1 1 6 0 0 1.85 0% 0%
Group 8: No. Isolates = 52 | No. STs = 7 | Predicted Founder = 46 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 46 44 6 0 0 0 1.0 99% 94% 328 2 2 4 0 0 1.66 0% 0% 389 1 2 4 0 0 1.66 0% 0% 45 2 1 5 0 0 1.83 0% 0%

48
540 1 1 5 0 0 1.83 0% 0% 387 1 1 5 0 0 1.83 0% 0% 368 1 1 5 0 0 1.83 0% 0% Group 9: No. Isolates = 71 | No. STs = 7 | Predicted Founder = 15 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 15 50 5 1 0 0 1.16 79% 74% 406 11 4 2 0 0 1.33 41% 34% 413 1 3 3 0 0 1.5 3% 1% 18 1 3 3 0 0 1.5 5% 2% 315 6 1 4 1 0 2.0 0% 0% 16 1 1 4 1 0 2.0 0% 0% 560 1 1 3 2 0 2.16 0% 0% (…) Group 13: No. Isolates = 135 | No. STs = 6 | Predicted Founder = 52 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 52 118 5 0 0 0 1.0 96% 80% 458 4 2 3 0 0 1.6 1% 0% 457 1 2 3 0 0 1.6 0% 0% 244 6 1 4 0 0 1.8 0% 0% 456 5 1 4 0 0 1.8 0% 0% 459 1 1 4 0 0 1.8 0% 0% (…) Group 18: No. Isolates = 24 | No. STs = 5 | Predicted Founder = 150 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 150 18 4 0 0 0 1.0 94% 49% 383 3 1 3 0 0 1.75 0% 0% 564 1 1 3 0 0 1.75 0% 0% 563 1 1 3 0 0 1.75 0% 0% 463 1 1 3 0 0 1.75 0% 0% (…) Group 28: No. Isolates = 43 | No. STs = 4 | Predicted Founder = 37 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 37 23 2 1 0 0 1.33 28% 0% 382 18 2 1 0 0 1.33 28% 0% 411 1 1 2 0 0 1.66 0% 0% 374 1 1 2 0 0 1.66 0% 0% (…) Group 41: No. Isolates = 26 | No. STs = 3 | Predicted Founder = 55 Average ST Bootstrap ST FREQ SLV DLV TLV SAT Distance Group Subgrp 55 24 2 0 0 0 1.0 28% 0% 396 1 1 1 0 0 1.5 0% 0% 414 1 1 1 0 0 1.5 0% 0% Singletons: size 232 161

49
Anexo VIII
Tabela 1- O perfil dos 7 genes nativos das 12 ST de isolados de colonização
Alelo
Código do Isolado DCC PFGE emm Type gki gtr murI mutS recP xpt yqiL ST
Complexo Clonal (CC) Grupo
Criança/adult
o DCC Bac Macrólidos
GAP 871 3 EM 3 2 6 8 5 2 3 2 15 15 9 C 3 S
GAP 689 3 BM 3 2 6 8 5 2 3 2 15 15 9 C 3 S
GAP 383 6 BG 3 2 29 8 5 2 3 2 406 15 9 C 6 S
GAP 376 6 BG 3 2 29 8 5 2 3 2 406 15 9 C 6 S
GAP 865 7 X 1 4 3 4 4 4 2 4 28 28 2 C 7 S
GAP 852 4 X 1 4 3 4 4 4 2 4 28 28 2 C 4 S
GAP 8 3 CX 1 4 3 4 4 4 2 4 28 28 2 C 3 S M
GAP 75 7 X 1 4 3 4 4 4 2 4 28 28 2 C 7 S
GAP 411 3 X 1 4 3 4 4 4 2 4 28 28 2 C 3 S
GAP 68 2 AP 12 5 2 2 6 6 2 2 36 36 7 C 2 S M
GAP 659 11 BK 12 5 2 2 6 6 2 2 36 36 7 C 11 S
GAP 615 1 AP 12 5 2 2 6 6 2 2 36 36 7 C 1 S
GAP 537 7 FW 12 5 2 2 6 6 2 2 36 36 7 C 7 S
GAP 518 7 AB 12 5 2 2 6 6 2 2 36 36 7 C 7 S
GAP 515 7 AB 12 5 2 2 6 6 2 2 36 36 7 C 7 S
GAP 359 5 BD 12 5 2 2 6 6 2 2 36 36 7 C 5 S
GAP 340 5 AB 12 5 2 2 6 6 2 2 36 36 7 C 5 S
GAP 320 5 AB 12 5 2 2 6 6 2 2 36 36 7 C 5 S
GAP 145 4 DM 12 5 2 2 6 6 2 2 36 36 7 C 4 S M
GAP 1446 1 FZ 12 5 2 2 6 6 2 2 36 36 7 C 1 S
GAP 144 4 AP 12 5 2 2 6 6 2 2 36 36 7 C 4 S M
GAP 295 3 DF 4 5 11 8 5 15 2 1 39 39 6 C 3 S M
GAP 163 6 A 22 9 8 1 1 1 3 4 46 46 8 C 6 S cMLSb
GAP 162 6 BH 22 9 8 1 1 1 3 4 46 46 8 C 6 S cMLSb
GAP 161 6 B 22 9 8 1 1 1 3 4 46 46 8 C 6 S cMLSb
GAP 861 7 EL 28 11 6 14 5 9 17 19 52 52 13 C 7 S
GAP 690 7 ED 28 11 6 14 5 9 17 19 52 52 13 C 7 S
GAP 857 7 DK 2 11 9 1 9 2 3 4 55 55 41 C 7 S
GAP 710 8 ES 2 11 9 1 9 2 3 4 55 55 41 C 8 S
GAP 396 2 BH 2 11 9 1 9 2 3 4 55 55 41 A 2 S
GAP 387 2 BH 2 11 9 1 9 2 3 4 55 55 41 C 2 S
GAP 902 4 EQ 75 11 2 1 3 50 8 7 150 150 18 C 4 S
GAP 891 6 EH 75 11 2 1 3 50 8 7 150 150 18 C 6 S
GAP 76 7 ET 75 11 2 1 3 50 8 7 150 150 18 C 7 S M
GAP 153 3 DN 75 11 2 1 3 50 8 7 150 150 18 C 3 S M
GAP 152 3 CY 75 11 2 1 3 50 8 7 150 150 18 C 3 S M
GAP 1397 12 EF 75 11 2 1 3 50 8 7 150 150 18 C 12 S
GAP 401 2 BI 48 16 41 2 29 2 25 7 161 singleton C 2 S
GAP 679 4 AD 1 5 52 5 5 5 4 3 382 37 28 C 4 S
GAP 540 7 AD 6 5 52 5 5 5 4 3 382 37 28 C 7 S
GAP 517 7 DX 6 5 52 5 5 5 4 3 382 37 28 C 7 S
GAP 404 6 BL 3 5 52 5 5 5 4 3 382 37 28 C 6 S
GAP 4 4 N 6 5 52 5 5 5 4 3 382 37 28 C 4 S cMLSb
GAP 655 11 AJ 3 16 2 8 3 82* 13 3 408 407 1 C 11 S
Nota: o Gestor da base de dados ([email protected]) informou que o número pelo qual o complexo clonal deve ser designado corresponde ao número do “predicted fouder” do grupo ao qual a ST pertence.
*Em Portugal, foi encontrado, pela primeira vez, um novo alelo recP 82 para a ST 408. (Estudo de: Friães, A., 2007. J Clin Microbiol. 45: 2044-2047
Isolados que não pertencem a nenhum cluster

50

51